Алкали метали. Структура, физичка и хемијска својства, примена
Алкалијски метали - заједнички назив елемената прве групе периодичног система хемијских елемената. Његов састав: литијум (Ли), натријум (На), калијум (К), рубидијум (Рб), цезијум (Цс), францијум (Фр), и хипотетски елемент - унуненијум (Ууе). Назив групе потиче од имена растворљивих натријум и калијум хидроксида, који имају алкалну реакцију и укус. Размотрите опште структурне карактеристике атома елемената, својства, производњу и употребу једноставних супстанци.
Застарела и нова групна нумерација
Према застарелом систему нумерисања, алкални метали који заузимају крајњу леву вертикалну колону периодног система припадају групи ИА. 1989. године, Међународна хемијска унија (ИУПАЦ) предложила је другу опцију (дуготрајну) као главну. Алкалијски метали у складу са новом класификацијом и континуираним нумерисањем припадају 1. групи. Представник другог периода - литијум - отвара овај агрегат, употпуњује свој радиоактивни елемент седмог периода - Француску. Сви метали прве групе у спољној љусци атома садрже један с-електрон, који се лако дају (обнављају).
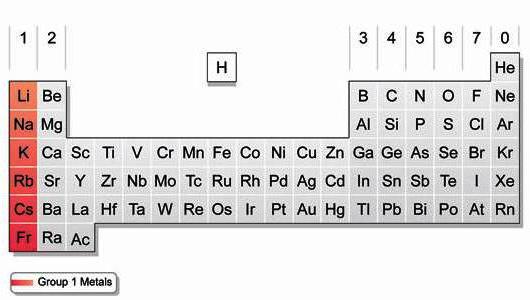
Структура атома алкалних метала
Елементе прве групе карактерише присуство другог енергетског нивоа, понављајући структуру претходног инертног гаса. Литијум има 2 електрона у последњем слоју и 8 електрона у другима. Код хемијских реакција, атоми лако одају спољашњи с-електрон, стичући енергетски повољну конфигурацију племенитог гаса. Елементи прве групе имају мале вредности енергије јонизације и електронегативности (ЕО). Они лако формирају појединачно набијене позитивне ионе. Приликом преласка из литијума у Француску, повећава се број протона и електрона, полупречник атома. Рубидијум, цезијум и францијум лакше донирају спољни електрон него елементи који им претходе у групи. Према томе, у групи од врха до дна, способност смањења се повећава.
Садржај у кори
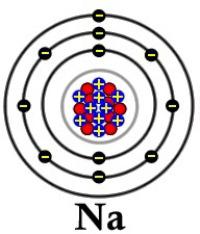 Лака оксидабилност алкалних метала доводи до чињенице да елементи прве групе постоје у природи у облику једињења њихових појединачно набијених катиона. Садржај у земљиној кори натријум - 2,0%, калијум - 1,1%. Остали елементи у њему су у малим количинама, нпр. У Француској - 340 г. Натријум хлорид растворен у морској води, сланој води соли и естуаријима, формира наслаге камена или сол. Заједно са халитом нађени су силвинит НаЦл • КЦл и силвин КЦл. Фелдспар формира се калијум алуминосиликатом К2 [Ал2Си6О16]. У води се раствара више језера натријум карбонат и сулфатне резерве елемента су концентрисане у Каспијском мору (Кара-Богаз-Гол). Постоје депозити натријум нитрат ин Цхиле (Цхилеан салтпетер). Постоји ограничен број природних литијумских једињења. Рубидијум и цезијум су пронађени као нечистоће у једињењима прве групе елемената, а францијум се налази у саставу уранових руда.
Лака оксидабилност алкалних метала доводи до чињенице да елементи прве групе постоје у природи у облику једињења њихових појединачно набијених катиона. Садржај у земљиној кори натријум - 2,0%, калијум - 1,1%. Остали елементи у њему су у малим количинама, нпр. У Француској - 340 г. Натријум хлорид растворен у морској води, сланој води соли и естуаријима, формира наслаге камена или сол. Заједно са халитом нађени су силвинит НаЦл • КЦл и силвин КЦл. Фелдспар формира се калијум алуминосиликатом К2 [Ал2Си6О16]. У води се раствара више језера натријум карбонат и сулфатне резерве елемента су концентрисане у Каспијском мору (Кара-Богаз-Гол). Постоје депозити натријум нитрат ин Цхиле (Цхилеан салтпетер). Постоји ограничен број природних литијумских једињења. Рубидијум и цезијум су пронађени као нечистоће у једињењима прве групе елемената, а францијум се налази у саставу уранових руда.
Алкали Метал Дисцовери Секуенце
Британски хемичар и физичар Г. Деви 1807. године спровео је електролизу алкалних талина, прво примајући натријум и калијум у слободној форми. Године 1817. шведски научник Јоханн Арфведсон открио је елемент литијума у минералима, а 1825. Г. Деви је издвојио чисти метал. Рубидијум је први пут открио 1861. године Р. Бунсен и Г. Кирцххофф. Немачки истраживачи анализирали су састав алуминосиликата и добили у спектру црвену линију која одговара новом елементу. Године 1939., запосленик Париског института за радиоактивност Маргарита Пере установио је постојање изотопа Француске. Она је такођер именовала елемент у част своје домовине. Унуненниус (ека-франциа) је пробни назив нове врсте атома са серијским бројем 119. Хемијски симбол Ууе се привремено користи. Од 1985. године истраживачи су покушали да синтетишу нови елемент, који ће бити први у осмом периоду, седми у 1. групи.
Физичке особине алкалних метала
 Готово сви алкални метали имају сребрно-белу боју и металик сјај на свежем резу (цезијум има златно жуту боју). Блистање се затамни у ваздуху, појављује се сиви филм, на литијуму је зеленкасто-црн. Овај метал има највећу тврдоћу међу суседима у групи, али је инфериорнији од талка - најмекшег минерала који отвара Мохову скалу. Натријум и калијум се лако савијају, могу се сећи. Рубидијум, цезијум и францијум у чистом облику представљају пастозну масу. Отапање алкалних метала се одвија на релативно ниској температури. За литијум достиже 180,54 ° Ц. Натријум се топи на 97,86 ° Ц, калијум на 63,51 ° Ц, рубидијум на 39,32 ° Ц, цезијум на 28,44 ° Ц. Густина алкалних метала је мања од сродних супстанци. Литиј лебди у керозину, подиже се на површину воде, у њему плутају калијум и натријум.
Готово сви алкални метали имају сребрно-белу боју и металик сјај на свежем резу (цезијум има златно жуту боју). Блистање се затамни у ваздуху, појављује се сиви филм, на литијуму је зеленкасто-црн. Овај метал има највећу тврдоћу међу суседима у групи, али је инфериорнији од талка - најмекшег минерала који отвара Мохову скалу. Натријум и калијум се лако савијају, могу се сећи. Рубидијум, цезијум и францијум у чистом облику представљају пастозну масу. Отапање алкалних метала се одвија на релативно ниској температури. За литијум достиже 180,54 ° Ц. Натријум се топи на 97,86 ° Ц, калијум на 63,51 ° Ц, рубидијум на 39,32 ° Ц, цезијум на 28,44 ° Ц. Густина алкалних метала је мања од сродних супстанци. Литиј лебди у керозину, подиже се на површину воде, у њему плутају калијум и натријум.
Кристално стање
Кристализација алкалних метала јавља се у кубичној сингони (центрираној ка телу). Атоми у свом саставу имају проводни појас, до којег слободни нивои могу да преносе електроне. Те активне честице носе посебну хемијску везу - металну. Заједничка структура енергетских нивоа и природа кристалних решетки објашњавају сличност елемената прве групе. Приликом преласка из литијума у цезијум, масе атома елемената се повећавају, што доводи до регуларног повећања густине, као и до промене других својстава.
Хемијска својства алкалних метала
Једини спољни електрон у атомима алкалних метала је слабо привучен језгром, тако да они имају ниску енергију јонизације, негативан или близак електронски афинитет. Елементи прве групе, који имају редукциону активност, практично нису способни за оксидацију. У групи одозго надоле, активност у хемијским реакцијама се повећава:
- Натријум, калијум и литијум са благим светлом на ваздуху. За прва два метала, карактеристично је формирање пероксида и перпероксида у овој реакцији, а за литијум, оксид Ли 2 О. Рубидијум и цезијум у ваздуху се самозапаљају.
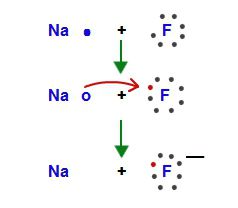 Алкални метали могу чак и да смање водоник. Када се загревају, ступају у интеракцију са атомима најлакшег елемента и враћају га у негативно набијени Х - ион. У реакцији су добијени хидриди, на пример, НаХ, КХ.
Алкални метали могу чак и да смање водоник. Када се загревају, ступају у интеракцију са атомима најлакшег елемента и враћају га у негативно набијени Х - ион. У реакцији су добијени хидриди, на пример, НаХ, КХ. - Једноставне супстанце које одговарају елементима прве групе ступају у интеракцију са водом и формирају алкалије, на пример, ЛиОХ, НаОХ, КОХ. Процес је праћен ослобађањем гасовитог водоника, који се самозапаља или експлодира. 2На + 2Х2О = 2НаОХ + Х2 . Рубидијум и цезијум реагују чак и са ледом. Складиштење алкалних метала је дозвољено под слојем минералног уља, у керозину, у затвореним стакленим судовима.
- Метали прве групе активно реагују са халогенима, реакција са флуором и хлором је посебно снажна, а када се загрева - са сумпором и фосфором. Већина добијених соли има добру растворљивост.
- Реакција високог квалитета - разградња соли алкалних метала у пожару гасног горионика. Парови боје пламен у одређеној боји.
- Када су алкални метали у интеракцији са алкохолима, добијају се алкохолати, при чему карбонске киселине дају одговарајуће соли, на пример, формијат натријума.
Припрема и употреба алкалних метала
Метали прве групе су индустријски произведени електролизом талина њихових халида и других природних једињења. Након разградње под дејством електричне струје, позитивни јони на катоди придају електроне и редукују се на слободан метал. Анион се оксидира на супротној електроди.
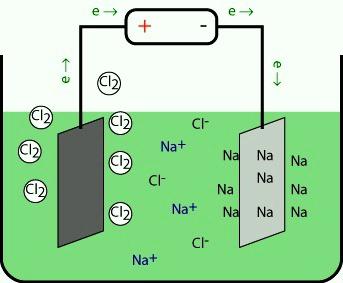
Током електролизе растопа хидроксида на аноди, ОХ - честице се оксидирају, развија се кисеоник и добија се вода. Други метод је термичка редукција алкалних метала из растопљених соли калцијума. Једноставне супстанце и једињења елемената прве групе су од практичног значаја. Литиј се користи као сировина у атомској енергији која се користи у ракетној технологији. У металургији се користи за уклањање остатка водоника, азота, кисеоника и сумпора. Хидроксид је допуњен електролитом у алкалним батеријама.

Натријум је неопходан за нуклеарну енергију, металургију, органску синтезу. Цезиј и рубидијум се користе у производњи фотонапонских ћелија. Хидроксиди и соли, посебно хлориди, нитрати, сулфати, карбонати алкалних метала, су у широкој употреби. Катиони имају биолошку активност, а натријум и калијум јони су посебно важни за људско тело.