Алуминијум сулфат и друга једињења алуминијума у природи и људском животу
У свакодневном животу, свако од нас се сваког минута суочава са количином хемикалија које одузимају дах, како природним тако и самим човеком. Осврнимо се на два хемијска једињења: алуминијум сулфат, алуминијум хидроксид. Шта је то и зашто бисте требали обратити пажњу на њих?
Да се сретнеш, треба да се приземљиш
Алуминијум сулфат (глиница), заједно са алуминосиликатима и различитим врстама глине, чини главнину земљине коре. Ово омогућава алуминијима да заузму прво место међу металима у смислу преваленције на Земљи. У природи, алуминијум сулфат, формула у којој је Ал2 (СО4) * 18Х2О, кристални хидрат и бели растворљив кристал растворљив у води са сивом, плавом или ружичастом нијансом.
Ad

За разлику од алуминијум сулфата, његов хидроксид је бела чврста материја, нерастворљива у води. Алуминијум сулфат, алуминијум хидроксид, каолинит су широко распрострањени. Рудници се копају у Сибиру, Криму, Кини, Јапану, као иу земљама Централне и Јужне Америке.
Зри у епрувети
Да бисмо сазнали истину, утврдићемо које хемијске особине имају сулфат и хидроксид Ал. Да парафразирамо фразу Козме Пруткова "Погледај у корен!" У прагматичнију: "Погледај у епрувету!"
 Почнимо са Ал хидроксидом, који представља ову супстанцу на слици Јанус са два лица. Веома мало хемијских једињења може истовремено да реагује са киселинама и алкалијама. Таква "дволичност" у хемији се зове амфотерна. Дакле, у реакцијама алуминијум хидроксида са киселином добијамо средње соли.
Почнимо са Ал хидроксидом, који представља ову супстанцу на слици Јанус са два лица. Веома мало хемијских једињења може истовремено да реагује са киселинама и алкалијама. Таква "дволичност" у хемији се зове амфотерна. Дакле, у реакцијама алуминијум хидроксида са киселином добијамо средње соли.

Узимајући у обзир интеракцију алуминијум хидроксида Ал (ОХ) 3 са алкалијама, ми ћемо бити пажљиви и узети у обзир услове под којима се реакција одвија. Финални производи ће зависити од њих:

Сам Ал (ОХ) 3 хидроксид се добија у лабораторији индиректним средствима, тј. Не из оксида и воде, што је у овом случају немогуће, већ из соли алуминијума. Да бисте то урадили, узмите раствор алуминијум сулфата и реагујте на њега алкалијама, као што је каустична сода, пажљиво сипајте у капи.
Ad
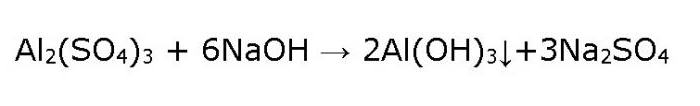
Као резултат, бели желатинозни талог, Ал (ОХ) 3, формира се у епрувети.

Сумирајући све горе наведене реакције, доказујући амфотерни алуминијум хидроксид, закључујемо: у киселој средини хемијска равнотежа се помера ка формирању Ал соли, и у алкалном правцу, према формирању метаалумината или хидроксиалумината.
Подржавајућа традиција
Узмимо паузу од потешкоћа "дуплитета" амфотерног алуминијум хидроксида и окренемо се традиционалној средњој соли - алуминијум сулфату. Нема одступања од правила. Раствори средњих соли реагују са алкалијама, са киселинама, са другим солима, са металима који стоје у серији Бекетов (метални стресни низ) до метала, чији се ион налази у молекулу соли. На пример, алуминијум сулфат у раствору ће реаговати са литијумом, калијумом, калцијумом, натријумом и магнезијумом. Потврдите то помоћу једначина реакције.
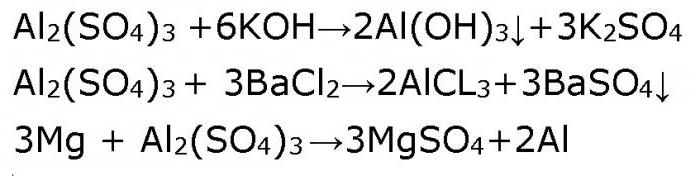
Алуминијум сулфат, чија је формула Ал2 (СО4) 3, производ је интеракције слабе алуминијум хидроксидне базе Ал (ОХ) 3 и јаке сулфатне киселине Х2С04. Због тога се лако хидролизује у воденом раствору. Вишак водониких јона Х + детектује се помоћу лакмус-индикатора, који мијења његову плаву боју у отопини алуминиј-сулфата до црвене. Дакле, утврдили смо да је раствор алуминијум сулфата кисели.
Ad

Било би могуће да се и даље бавимо детаљима ове теме која су била пријатна и узбудљива за хемичара-естета, ако је сумњиво скептична особа са питањем: "Па шта ћу ја имати?"
Доћи ће у помоћ
Да бисмо отклонили све недоумице, рецимо да већ имате много корисних, па и виталних ствари, захваљујући таквим једињењима као што су алуминијум сулфат, алуминијум хидроксид и други реагенси који садрже алуминијум. Прво, Ал (ОХ) 3 се користи за чишћење тврде воде. После овог процеса, вода постаје транспарентнија и лакша и ослобађа се соли које га чине тешким.
Лосиони, гелови, тоници нам помажу да будемо увек лепи и лепо одгојени. Али они такође садрже алуминијум сулфат. Широко рекламирана иновација у индустрији антиперспирантне дезодоранса која се зове "кристали свјежине" није ништа друго него алуминијум калијум алум, од чега је компонента алуминијум сулфат. Једињења алуминијума имају способност обавијања и стога се користе у производњи вишеслојних памучних тканина иу фармакологији.