Комплексна једињења и њихово значење
Комплексна једињења (ЦС) играју важну улогу у активности живих организама. Они се такође широко користе у индустрији. Данас разматрамо њихову различитост врста, примену и историју студије.
Увод у комплексна једињења
Комплексна једињења су супстанце формиране комбинацијом лиганда и агенса за комплексирање. Играјте улогу честица које могу да делују у атомима и јонима. А. Вернер је 1893. увео теорију комплексних једињења у свијет, названу теорија координације.
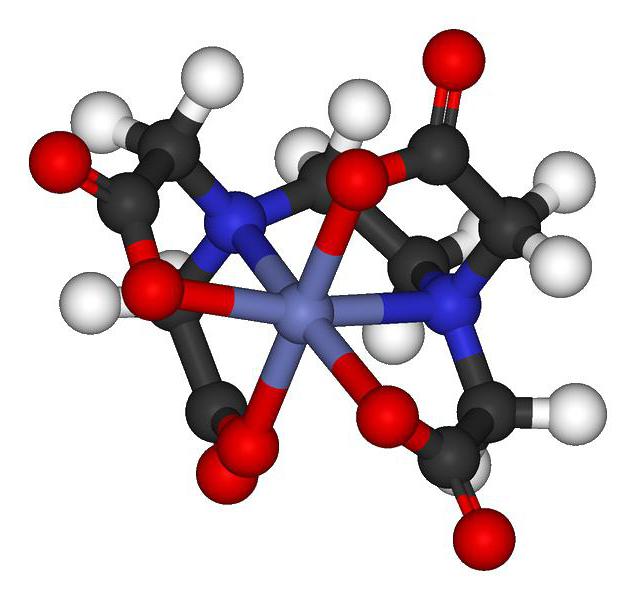
Присуство спољашње сфере и потпуна дисоцијација у раствору воде на ниске дисоцирајуће катионе и анионе карактеристичне су за ЦС. Међутим, постоје неке врсте које немају спољашњу сферу, која им не дозвољава да се растворе у води. Постоји огромна количина ЦОП-а
Ad
Врсте једињења
Сложена једињења су подељена у три главна типа:
- Први тип, који се разликује по комплексном набоју, укључује катионске комплексе, у којима су, око позитивног иона, координирани неутрални молекули. Други тип се назива анионски комплекс, у коме позитивно оксидовани атом делује као комплексни агенс, а аниони једноставног или комплексног типа су лиганди. Трећи тип се назива неутрални комплекс, формиран је због координације молекула око атома који има неутралан набој.
- У зависности од природе лиганда, подељени су на амонијаке (амонијак - лиганд), аквакомплекси (лиганд - вода), хидроксомплекси (лиганди - хидроксидни јони), кисели комплекси (лиганди - киселински остаци), карбонили (лиганди - молекули угљеника друге валенције).
- У складу са положајем лиганда су монодентат, бидентат и полидентат КС.
Хисторицал информатион
1893. године направљен је први покушај да се исцрпно опише структура ЦС користећи координациону теорију Алфреда Вернера. Рад је урађен пре него што се појавила теорија валентности електрона и уобичајено хемијске реакције природе.
Ad

У својој теорији, Вернер је тврдио да једињења неорганске природе имају језгре састављене од атома који формирају комплекс. Атоми који окружују комплексирање називају се координацијом. Они су распоређени у складу са обликом једноставног полиедра. А. Вернер је претпоставио присуство везе типа координације у заједничком електронском пару, који би атоми или молекули дали другом пару. Међутим, одсуство постојања таквих једињења изазвало је неповерење међу хемичком заједницом. Као резултат, наредне две деценије, научник је покушао да створи неопходне супстанце које би потврдиле његову теорију.
Вернер је 1911. синтетисао више од четрдесет молекула оптичког типа, који нису садржавали атоме угљеника, што је на крају променило мишљење научника хемије о његовој теорији.
Алфреду Вернеру је додељена Нобелова награда 1913. године за достигнућа у области хемије.
Номенклатура
Комплексни спојеви имају систем за креирање сопствених имена, који се састоји од пет тачака:
- Први је изражен анион, затим катион.
- Комплексни део почиње лигандом - анионом који се налази у унутрашњој сфери, а до краја се додаје са “о”.
- Монодентатни лиганди су означени помоћу грчког: моно, ди, три, тетра, пента, хекс (1, 2, 3, 4, 5, 6). При раду са полидентатним лигандима користе се трис, бис, тетракис и други.
- Означавајући унутрашњу сферу својим компонентама, идите на спољашњу.
- Средство за комплексирање честица са неутралним комплексом је назначено у номинативном случају.
Информације о структури
Комплексна једињења имају унутрашњу сферу која се састоји од низа јона или молекула неутралне природе, чврсто везаних за комплексни агенс. Зову се лиганди. Унутрашња сфера може носити три типа пуњења: "+", "-" или "0".
Ad
Спољна координациона сфера су јони који се не налазе у простору унутрашње сфере.
Веза између лиганда и централног јона може бити узрокована или електростатичким привлачењем или механизмом донор-акцептор.
Изомерија у координационим једињењима је главни статистички аспект. Када говоримо о изомеризму, они означавају различите међусобне положаје у простору атома или састојака једињења, што ће довести до промене физичких и хемијских својстава одговарајућег једињења - изомера. ЦС изомерија је структурна, оптичка и просторна.
Стереоцхемистри
Комплексна једињења, заједно са органска материја Високомолекулска једињења синтетичког или природног порекла су главни објекти стереохемијских студија. А. Вернер се сматра једним од оних научника који су дали развој читавом пољу истраживања и обновили неке области хемијске активности. Стереокемија до данас остаје референтна тачка за координациона хемијска истраживања.
Ad
Нека својства и методе добијања
Добијање комплексних једињења има прилично широк спектар избора, међутим, такви се чешће користе:
- Растварање хидроксида у воденом раствору амонијака који се не растварају у води.
- Интеракција амонијака са металним солима са својствима комплексирања; чешће су то метали у секундарној подгрупи.
- Интеракција цијанида или роданида са металима или солима.
- Простор је нерастворљив у Х 2 О металима амфотерног типа, односно њиховим оксидима или хидроксидима у алкалном раствору.
- Комплексне киселине се могу добити, на пример, реакцијом злата и водене киселине или Ау хидроксида са ХЦл.
Многе квалитативне карактеристике једињења зависе од њихових електронских својстава, тако да се боја ЦС може одредити агенсом комплексирања и лигандима. Расподела енергије на д-орбитали дозвољава електронима да се крећу од њених д кз , д ки , д зи под-нивоа на под-нивое са вишим енергетским индексом д з 2 или д з 2 - и 2 . Овај феномен је праћен апсорпцијом кванта светлости. Величина разлике између подељених нивоа изазива апсорпцију кванта светлости са опсегом таласних дужина различитих дужина, што даје одређену боју.
Ad
Комплексна једињења такође имају два важна магнетна својства, према којима су класификована као парамагнетски и диамагнетски. Парамагнетски комплекси имају своје µ-моменте, и због тога, улазећи у спољашња електромагнетска поља, у процесу интеракције, улазе у њих. Дијамагнетски комплекс нема магнетни моменат и зато се магнетно поље жури да га избаци. Својства парамагнетске природе одређена су присуством електрона који немају свој пар.
Усе оф

Једињења комплексног типа играју једну од најважнијих улога у било ком организму, на пример, кисеоник упарен са хемоглобином у крви се доводи преко тела О2 кроз ткива и ћелије; Хлорофил у биљкама се такође сматра комплексним.
Употреба комплексних једињења се широко користи у индустрији. Уз помоћ хемијских метода које укључују формирање КС, метали се екстрахују из руде. Примери укључују чисто гвожђе, никл и кобалт, који се добијају термичком разградњом металних карбонила. Ове комплексне супстанце, које се разлажу, емитују потребне метале.

Аналитичка хемија може користити ЦОП као индикаторе. Због њих се органска и неорганска синтеза може убрзати, јер су својства катализатора својствена њима због њихове високе активности. Електроформирање такође не може без комплексних једињења, што је узроковано немогућношћу добијања таквих поузданих премаза од једноставне соли, за разлику од цијанидних једињења.