Шта је кртица у хемији?
Концепт кртице се користи за мерење хемикалија. Да откријемо особитости ове количине, дајемо примере рачунских задатака са њеним учешћем, дефинишемо значај овог термина.
Дефиниција
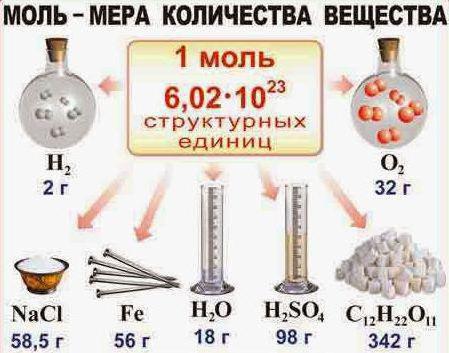
Кртица у хемији је јединица израчуна. Он представља количину одређене супстанце у којој има толико структуралних јединица (атома, молекула) колико их има у 12 грама атома угљеника.

Авогадро број
Количина супстанце је повезана са Авогадров број што је 6 к 10 ^ 23 / мол. За супстанце молекуларне структуре, сматра се да један мол укључује Авогадро број. Ако треба да бројимо број молекула садржаних у 2 мола воде, онда треба да помножимо 6 * 10 ^ 23 са 2, добијамо 12 * 10 ^ 23 комада. Погледајмо улогу коју кртица игра у хемији.
Количина супстанце
Супстанца која се састоји од атома садржи Авогадро број. На пример, за натријумов атом је 6 к 10 к 23 1 / мол. Која је његова ознака? Кртице у хемији су означене грчким словом “акт” или латиницом “н”. За математичке прорачуне везане за количину супстанце, користите математичку формулу:
н = Н / Н (А), где је н количина неке супстанце, Н (А) је Авогадро број, Н број структурних честица неке супстанце.
Ако је потребно, можете израчунати број атома (молекула):
Н = Н (А) * н
Стварна моларна маса се зове моларни. Ако је количина супстанце одређена у моловима, онда је вредност моларна маса Има јединице г / мол. У нумеричким терминима, она одговара вредности релативне молекуларне тежине, која се може одредити сумирањем релативних атомских маса појединачних елемената.

На пример, да би се одредила моларна маса молекула угљен диоксид потребно је извршити следеће израчуне:
М (ЦО2) = Ар (Ц) + 2Ар (О) = 12 + 2 * 16 = 44
При израчунавању моларне масе натријум оксида добијамо:
М (На2О) = 2 * Ар (На) + Ар (О) = 2 * 23 + 16 = 62
При одређивању моларне масе сумпорне киселине сумирамо две релативне атомске масе водоник са једном атомском масом сумпора и четири релативне атомске масе кисеоника. Њихове вредности се увек могу наћи у периодном систему. Као резултат тога, добијамо 98.
Кртица у хемији омогућава разне калкулације везане за хемијске једначине. Сви типични задаци рачунања у неорганској и органској хемији, који претпостављају проналажење масе и запремине супстанци, решавају се тачно кроз мољце.
Примјери задатака намире
Молекулска формула било које супстанце указује на број молова сваког елемента укљученог у његов састав. На пример, један мол фосфорна киселина садржи три молова атома водоника, један мол фосфорних атома и четири молова атома кисеоника. Све је врло једноставно. Кртица у хемији је прелазак са микрокосмоса молекула и атома у макросистем са килограмима и грамима.
Задатак 1. Одредити број молекула воде који се налазе у 16,5 мола.
За решење, користимо однос између Авогадровог броја (количине супстанце). Добијамо:
16.5 * 6.022 * 1023 = 9.9 * 1024 молекула.

Задатак 2. Израчунајте број молекула садржаних у 5 г угљен диоксида.
Прво, потребно је израчунати моларну масу дате супстанце, користећи предност његове релативне релативне молекуларне тежине. Добијамо:
М (ЦО2) = Ар (Ц) + 2Ар (О) = 12 + 2 * 16 = 44.
Затим израчунамо број молекула користећи горе наведену формулу:
Н = 5/44 * 6.023 * 1023 = 6.8 * 1023 молекула.
Алгоритам проблема на хемијској једначини
Приликом рачунања масе или продуката реакције употребом једначине, користи се алгоритам специфичне акције. Прво, одређује се који од почетних материјала је недовољан. Да бисте то урадили, пронађите њихов број у кртицама. Затим, направите једначину процеса, обавезно поставите стереохемијске коефицијенте. Почетни подаци се евидентирају над супстанцама, а испод њих се наводи количина супстанце која се узима у моловима (по коефицијенту). Ако је потребно, извршите конверзију јединица мере, користећи формуле. Затим саставите пропорцију и решите је на математички начин.
Ако се предлаже тежак задатак, онда се маса чисте супстанце прелиминарно израчунава, уклања нечистоће, а затим почиње да одређује њену количину (у моловима). Ни један проблем у хемији који се односи на једначину реакције није решен без такве величине као кртица. Поред тога, коришћењем овог термина, лако се може одредити број молекула или атома који користе Авогадро константни број за такве прорачуне. Налози за насеља су укључени у тест питања из хемије за матуранте основних и средњих школа.