Механизам донатор-акцептор - шта је то?
Донаторско-акцепторски механизам формирања хемијске везе подразумева пренос пуњења између акцептора и донора без стварања заједничке хемијске везе између њих. Такође је могуће пренети усамљени пар електрона на акцептор од донора, што резултира везом.
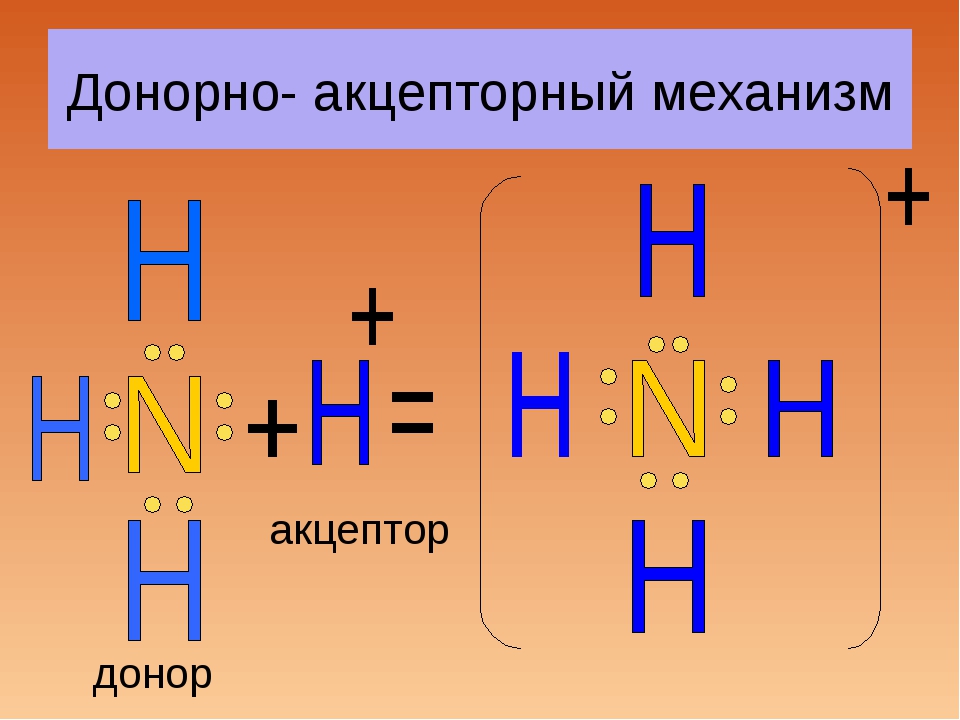
Формирање амонијумових соли
Размотримо механизам донор-акцептор на примеру амонијумових соли. Почињемо са интеракцијом амонијака (НХ3) и боровог трифлуорида (БФ3). Током реакције ослобађа се 171,4 кЈ / мол енергије. Интеракција се одвија према једнаџби:
НХ3 + БФ3 = НХ3БФ3
Од четири орбитале присутне у атому бора, три су испуњене електронима, тако да постоји једна празна орбита. У молекули амонијака, четири орбитале азота су опремљене електронима, а три од њих су допуњене водониковим електронима кроз механизам размене. Једна орбита има електронски пар који припада само атому азота. Зове се усамљени електронски пар. Захваљујући њој, механизам донор-акцептор је могућ.
Веза између амонијака и бор трифлуорида је могућа због чињенице да је празан електронски пар амонијака смештен на слободне орбитале бор флуорида.
Ово је механизам донор-акцептор за формирање ковалентних веза. Атом азота повећава валенцију употребом усамљеног пара електрона за додатно везивање. Бор повећава валенцију постављањем додатних електрона у орбиталу.
Према томе, валенца ових хемијских елемената карактеришу и неспарени електрони и усамљени електронски парови и слободне орбитале на спољашњем енергетском нивоу.
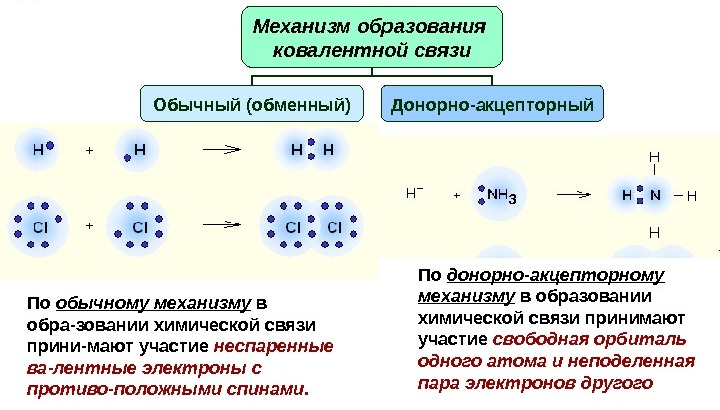
Дефинитионс
Донатор у овом примеру је атом азота, који даје свој електронски пар да формира хемијску везу. Акцептор је бор, има празну орбиту, прихвата електронски пар.
Процес је праћен смањењем потенцијалне енергије овог система, ослобађањем еквивалентне количине енергије. Питања која се тичу механизма формирања ове врсте ковалентне везе укључена су у ток школског програма из хемије, а предложена су у завршним испитима за матуранте средњих школа.
Формирање амонијум катиона
Ковалентна веза формирана донор-акцептор механизмом, карактеристичним за амонијумове соли. Осврнимо се на његове карактеристике. Дакле, донор-акцепторски механизам ствара везу између атома азота и водоника у реакцији:
НХ3 + Х + = НХ4 +
Акцептор је празна орбита катиона водоника. Азот у амонијевом катјону показује валенцију 4. Формирање везе настаје и због пара електрона који припадају азоту прије почетка интеракције.
Ово је ковалентна веза донор-акцептор механизмом. Као резултат интеракције, формира се амонијум катион, који се путем јонског механизма комбинира са анионима садржаним у киселинама.

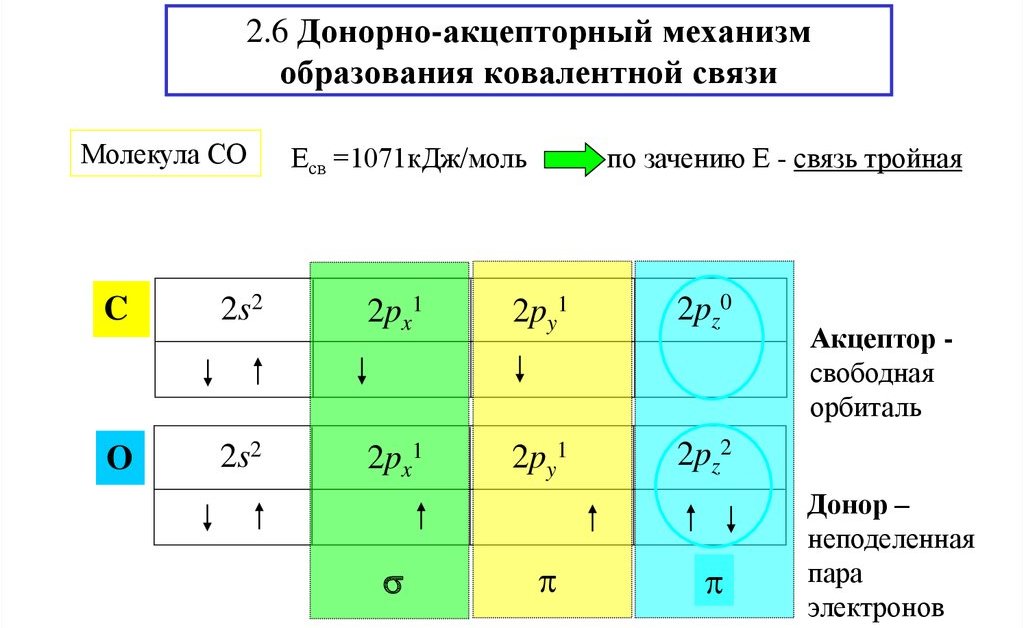
Формирање угљен моноксида
Механизам донор-акцептор се може узети као молекула ЦО као пример. На атому угљеника на спољашњем енергетском нивоу постоје два неспарена електрона. Исти број неспарених електрона је на атому кисеоника. Као резултат, формира се двострука веза између атома.
Због пара електрона кисеоника и празне орбите угљеника, користи се механизам донор-акцептор да се добије веза.
Молекула азотне киселине
Због присуства три неспарена електрона, атом азота у овом једињењу формира три варијанте везе: са двоструким кисеоником, са једним кисеоником са хидроксилном групом. Према механизму донор-акцептор, веза се формира између другог атома кисеоника и азота.
Непарени електрони се постављају на једну орбиталу, док се један ослобађа.
Такође можете претпоставити да је атом азота дат кисеонику електроном. Претворен у амонијумски катјон који има 4 неспарена електрона, задржава анион због сила електростатске интеракције.
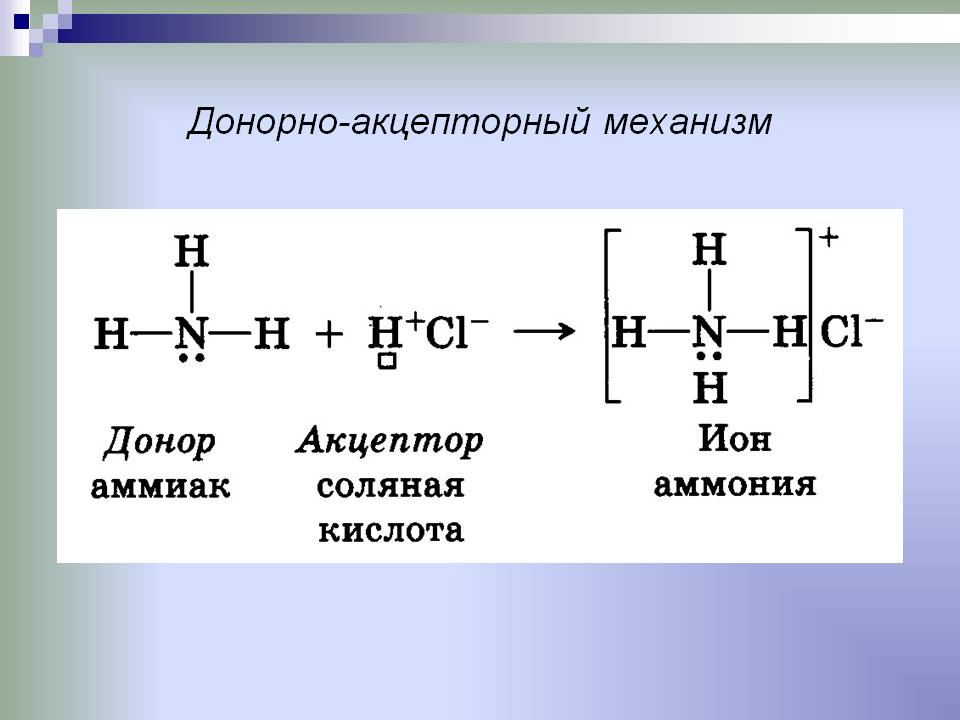
Својства комуникације
Као донор, постоје молекули у којима постоје атоми Н, О, Ф, Цл, повезани са атомима других хемијских елемената. Акцептор је честица са празним електронским нивоима. На пример, ово могу бити представници д-породица које имају непопуњене д-орбитале.
У молекули амонијака, користе се три неупарена електрона атома азота за формирање везе, а 1с-електрон на три атома водоника су укључени. Везе су дуж три осе п-орбитала. Молекул има варијанту регуларне пирамиде, у чијим угловима се налазе атоми водоника, а на врху - азотни азот. Угао између веза је 107 степени. Сличне облике молекула формирају следеће елементе са водоником: антимон, арсен, фосфор.
Својства ковалентне везе, која се формира од механизма донор-акцептор, не разликују се од карактеристика везе коју формира механизам размене. Донатори могу бити атоми азота, сумпора, фосфора, кисеоника, који поседују усамљене електронске парове на малим валентним орбиталима.
Функција акцептора се изводи помоћу водоник катиона, који су део п-метала, на пример, алуминијума, који формирају АлХ 4 - јон.
Такође, акцептори су д-елементи, који имају празну енергетску ћелију у спољном електронском слоју.
Треба напоменути да се све главне карактеристике, као што су засићеност, дужина, мноштво, примењују на овај механизам формирања комуникације.
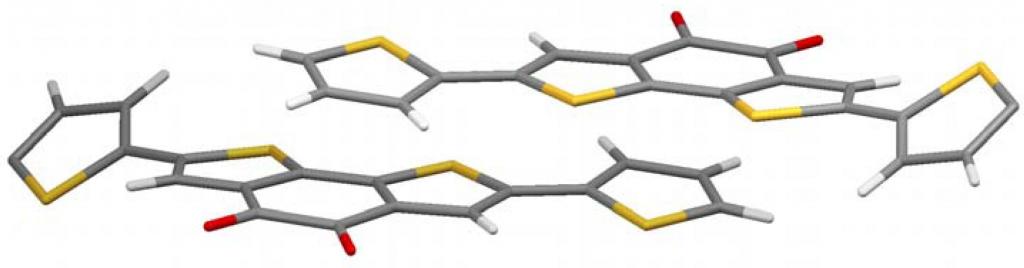
Карактеристике органских једињења
Интеракција механизама размјене је могућа за органске донаторе. Конкретно, међу њима су π-донори, типичан пример којих су тетракис (диметиламино) етилен (ТДАЕ), органски акцептори (фулерени), кинодиметани са акцепторским супституентима.
Хемијска интеракција таквих једињења ствара комплекс са преносом наелектрисања. У њему позитивно наелектрисани донор ступа у интеракцију с негативно набијеним акцептором због сила електростатичке природе. Значајни су системи у којима се трансфер наелектрисања у земаљском електронском стању дешава делимично, ау случају фото ексцитације, посматра се његов комплетан пренос.
Такви системи, донор-акцепторске дијаде, триаде у којима постоји група мостова између акцептора и донора, што омогућава да се повећа трајање стања са преносом електричног набоја, користе се за производњу уређаја који претварају соларну енергију. Сличан феномен повезан са преносом набоја у било ком од његових облика користи се у многим биолошким процесима.
Због тога се детаљно испитују карактеристике интеракције кроз механизам донор-акцептор у органским једињењима, анализирају се могућности убрзавања (успоравања) сличних процеса, могућности увођења додатних супстанци (катализатори).
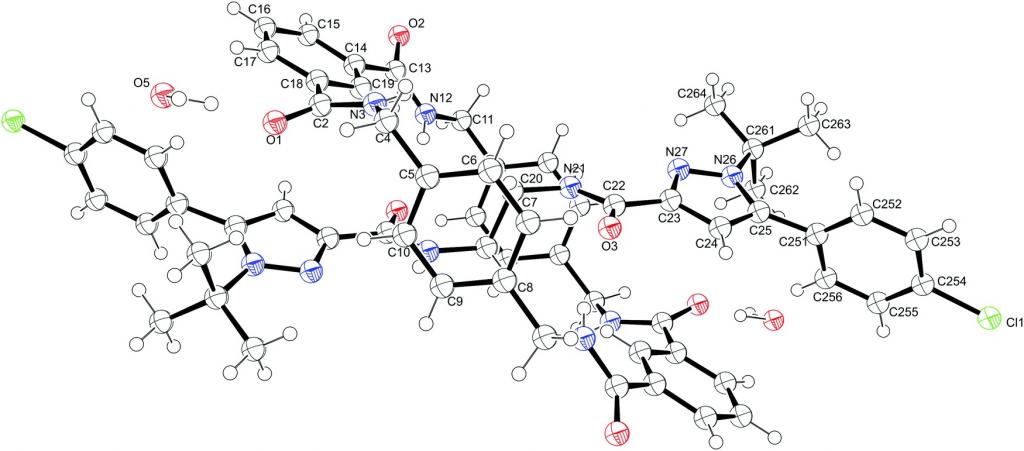
Да резимирамо неке
Интеракција донор-акцептор је једна од најважнијих манифестација ковалентне поларне хемијске везе. Велику пажњу посвећује неорганској, аналитичкој, органској хемији.
На пример, управо је са становишта механизма донор-акцептор објашњено формирање ковалентно локализованих веза у молекуларним јонима координационих (комплексних) једињења. Веза у њима настаје услед усамљеног електронског пара лиганда и слободних орбитала агенса за комплексирање. Механизам донор-акцептор такође објашњава формирање интермедијарних производа. Нарочито је реч о стварању комплекса са преносом наплате.
Постоји модел донор-акцепторског механизма само у оквиру концепта валенције као могућности локализације електронске густине у процесу формирања ковалентних веза. Овај механизам је основа за формирање различитих комплексних једињења. Таква интеракција је неопходна за киселинско-базне трансформације везане за трансфер водоничног јона (акцептор), формирање наноструктура.