Електронска конфигурација атома — кола и модели
Електронска конфигурација хемијских елемената је праћење локације електрона у његовим атомима. Електрони могу бити смјештени у шкољкама, подслојевима и на орбитали. Валенција елемента, његова хемијска активност и способност интеракције са другим супстанцама зависи од расподеле електрона. 
Правила уласка
Према утврђеној традицији, квантни број атома се пише одређеним латиничним словом. Стање нултог квантног броја је записано као с, праћено словима п, д, ф, г, б, и тако даље, према редослиједу слова у латиница.
Како написати електронску конфигурацију
Распоред атома се обично бележи за оне честице хемијских елемената који су у основном стању. Ако је атом узбуђен, улаз ће се звати узбуђена конфигурација. Дефиниција електронске конфигурације која се примењује у одређеном случају зависи од три правила која се примењују на атоме свих хемијских елемената.
Принцип пуњења
Електронска конфигурација атома мора бити у складу са принципом пуњења, према којем електрони атома испуњавају орбитале у растућем реду - од најнижег енергетског нивоа до највишег. Најниже орбитале било ког атома су увек прво попуњене. Затим електрони попуњавају постојеће орбитале другог енергетског нивоа, затим орбиту с, и само на крају - орбиталу п-под-нивоа. 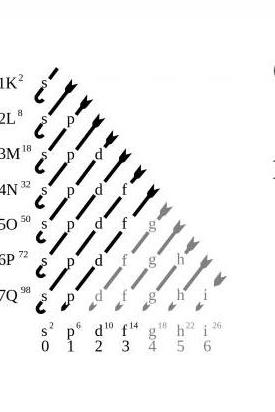
На писму се електронска конфигурација хемијских елемената преноси формулом у којој се поред имена елемента означава комбинација бројева и слова која одговарају положају електрона. Горњи индекс показује број електрона у овим орбиталима. 
На пример, атом водоника има један електрон. Према принципу пуњења, овај електрон се налази на с-орбитали. Дакле, електронска конфигурација водоника ће бити једнака 1с1.
Принцип забране Паула
Друго правило за попуњавање орбитала је посебан случај општег закона који је открио швајцарски физичар Ф. Паули. Према овом правилу, у сваком хемијском елементу нема пара електрона који имају исти скуп квантних бројева. Дакле, на било којој орбитали у исто време могу бити више од два електрона, а онда само ако имају различите спинове.
Принцип забране Паулија може се разматрати на специфичном примјеру. Електронска конфигурација атома берилијума може се записати као 1с 2 2с 2 . Када уђе у атом кванта енергије, атом прелази у побуђено стање. Ово се може писати овако:
1с 2 2с 2 (нормално стање) + хν → 1с 2 2с 1 2п 1 ( ексцитовано стање).
Ако упоредимо електронске конфигурације берилијума у нормалном и побуђеном стању, можемо видети да број неспарених електрона за њих није исти. Електронска конфигурација берилијума показује одсуство неспарених електрона у нормалном стању. Након ударца атома кванта енергије, појављују се два неспарена електрона. 
У принципу, у било ком хемијском елементу, електрони могу прећи у орбитале са вишим енергијама, али за хемију су од интереса само они прелази који се појављују између поднива са сличним енергијама.
Овај образац се може објаснити на следећи начин. Формирање хемијске везе увек је праћено ослобађањем енергије, јер атоми прелазе у енергетски повољно стање. Парни електрони на једном енергетски ниво у себи носи такве трошкове енергије који су потпуно компензовани након формирања хемијске везе. Трошкови енергије парних електрона различитих хемијских нивоа су тако високи хемијска веза не могу да их надокнаде. Ако не постоји хемијски партнер, побуђени атом ослобађа квантну енергију и враћа се у своје нормално стање - знанственици тај процес називају релаксацијом.
Правило гунда
Електронска конфигурација атома покорава се Гундовом закону, према којем пуњење орбитала једне подгрупе почиње са електронима који имају исти спин. Тек када сви појединачни електрони заузму успостављене орбитале, напуњени су набијеним честицама са супротним спином.
Правило Гунда је јасно потврђено електронском конфигурацијом азота. Атом азота има 7 електрона. Електронска конфигурација овог хемијског елемента је следећа: лс22с22п3. Сва три електрона, који се налазе на 2п-подгрупи, морају бити сами, заузимајући сваку од три 2-п орбитале, и сви спинови морају бити паралелни њима.
Ова правила помажу не само да разумију разлоге електронске конфигурације елемената периодичног система, већ и да разумију процесе који се одвијају унутар атома.