Глицерин: структурна формула, својства и примјена
Ово је најједноставнији триатомски алкохол. Хемијска формула глицерола је Ц3Х5 (ОХ) 3 . То је чиста вискозна течност. Без мириса, слатког укуса. Није отрован, стога се широко користи у свакодневном животу, прехрамбеној индустрији, козметици и медицини. Структурна формула глицерола је приказана на слици. Али како је минирано?
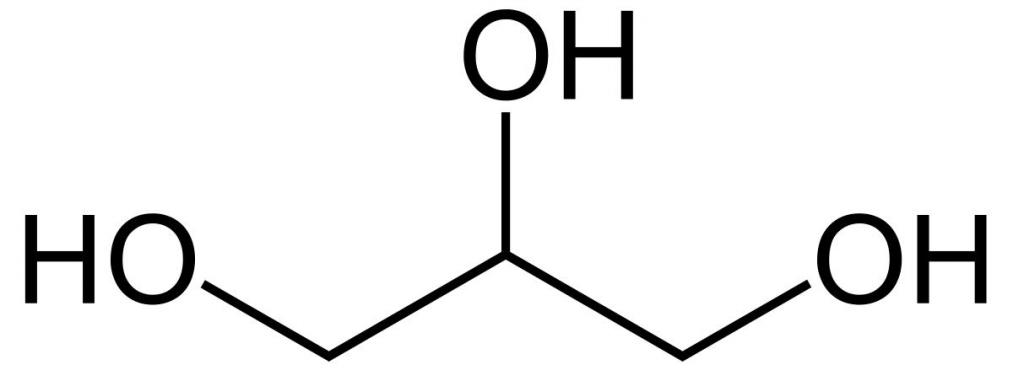
Начини добијања глицерина
Готово сав индустријски глицерол се добија из масти. Са хемијске тачке гледишта, они су естери глицерола. Током сапонификације ових масти (сапун), глицерин се формира као нуспродукт. Тада је веома лако издвојити се из реакционе смеше.
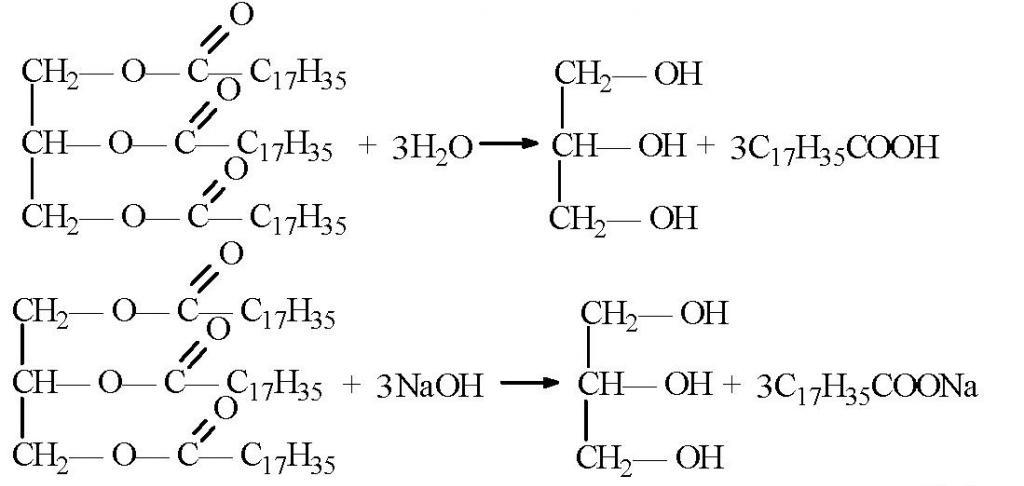
Глицерин је могуће синтетизовати на друге начине. На пример, из ацетона. У овом случају, редукује се водоником да би се добио изопропил алкохол. У следећој фази, молекул воде се одваја дехидрацијом да би се произвео пропилен, који је затим хлорисан. Добијени дихлоропропан се хлорише још једном да се добије триклоропропан. Последња фаза производње глицерола је хидратација када се загрева. У овој фази, сва три молекула хлора су замењена хидроксилним групама. На сличан начин сада у индустрији добија се синтетичка супстанца. Само као сировина се користи пропилен, који се ослобађа из бочних гасова током дестилације уља.
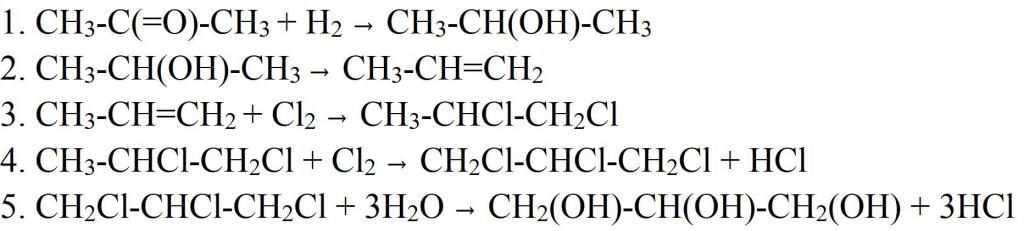
Али од пропилена да би се добио глицерин може бити други начин. Због тога се пропилен оксидује до акролеина. Оксидација се изводи са ваздушним кисеоником у присуству катализатора (бакар) и повишене температуре. Затим се додаје водоник пероксид, дајући дихидрични алдехид алкохол. Осмијум оксид (ВИИИ) се користи као катализатор за ову реакцију. Алдехидна група у добијеном једињењу је хидрогенована, претварајући је у трећу хидроксилну групу. Тако испада глицерин.
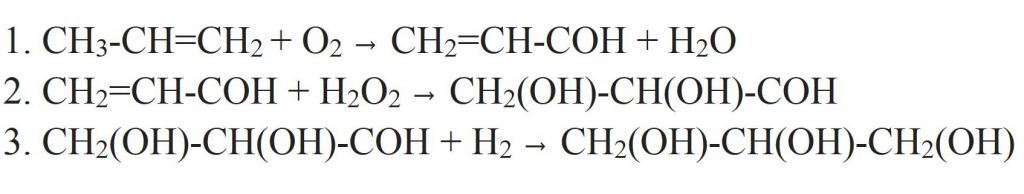
Друга верзија синтезе у једном тренутку предложила је ЕЕ Вагнер. Оксидацијом алил алкохола са калијум перманганатом у алкалном средству, глицерол се може добити у једној фази.
Пхисицал пропертиес
Глицерин је безбојна течност без мириса слаткастог укуса. То је хигроскопно, односно, тежи да апсорбује воду. На температури од 20 ° Ц топи се, а на температури од 290 ° Ц долази до кљуцања са делимицним распадом. Меша се са водом и алкохолима у било ком односу. То је због хемијске формуле. Хидроксилне групе омогућавају глицеролу да формира многе водоничне везе са молекулима воде. Ово омогућава растварање.
Ad
Растворимо глицерин иу ацетону и неким другим органским супстанцама. Нерастворљив у бензену и етрима. Он може бити такав за многа органска и неорганска једињења. Његова густина у течном стању је 1,26 г / цм3. Такође је важно напоменути да је глицерин веома вискозна течност. Имовина је 1474 пута већа од воде.
Хемијска својства
Цоминг фром структурна формула глицерин садржи три хидроксилне групе. Стога ће за њега бити карактеристичне хемијске реакције монохидричних алкохола. Штавише, кисела својства глицерола су много јача од оних других монохидричних алкохола. Дакле, може да ступи у интеракцију са металима, њиховим оксидима или алкалијама. Једначине хемијских реакција глицерола су приказане у наставку.
Ad
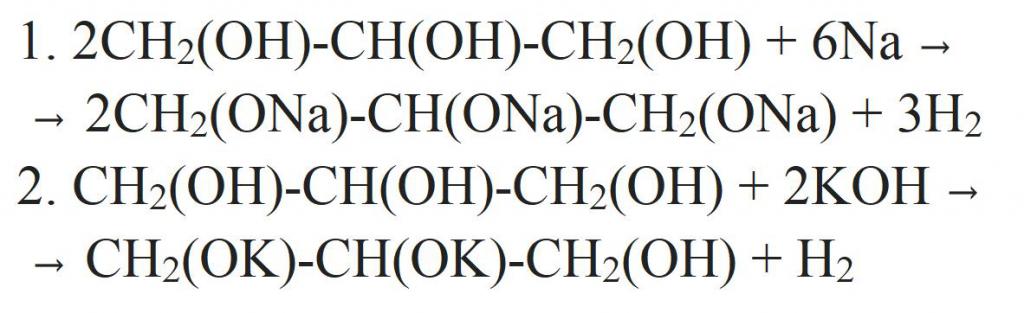
Такође може да уђе у реакције дехидрације, формирајући различите производе. Тако да добијете акролеин.
Одвојено, треба рећи за супституцију хидроксилне групе за халоген. Ово се може десити када глицерин ступа у интеракцију са халогенидом водоника. Као што се може видети из структурне формуле глицерола, као резултат реакције, могу се формирати моно-, ди- и три-деривати. Потпунија замена се може постићи ако се интеракција врши са фосфорним халидима.
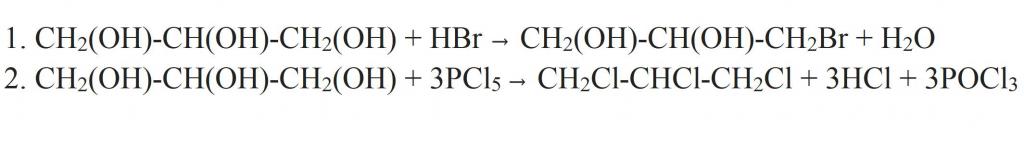
Али глицерин има специфична својства која су јединствена за полихидричне алкохоле. На пример, она ступа у интеракцију са бакарним (ИИ) хидроксидом и формира комплексно једињење плаве боје - бакар глицерат. Ова реакција је квалитативна за све полихидричне алкохоле.
Карактери за њега и реакција естерификације. То је реакција интеракције са киселинама, што резултира естером. Штавише, глицерин се естерификује и органским и минералним киселинама. На пример, нитрична. Ова реакција се назива и нитрација. Као резултат тога, испада веома користан, али изузетно експлозиван производ - нитроглицерин. Опет, из структурне формуле глицерола, може се видети да се не могу све ерилификовати све хидроксилне групе. Све зависи од услова реакције.
Ad
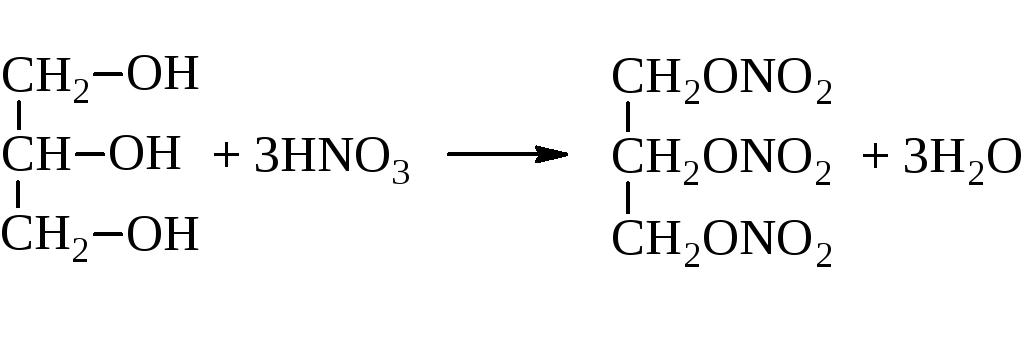
Код интеракције са водоником под високим притиском и у присуству катализатора, редукује се једна од хидроксилних група. Као резултат реакције добија се дихидрични алкохол - пропилен гликол.
Глицерин такође може ући у реакције поликондензације, формирајући мешавину полиглицерола. За то се дуго дуго загрева на скоро 300 ° Ц у слабо алкалном окружењу. Прегледана је хемијска формула глицерина.
Оксидација
Глицерин има много опција за оксидацију. Финални производ зависи од природе оксидационог средства, катализатора и других реакционих услова. Према томе, глицерин се може оксидовати јаким оксидационим средствима, на пример, калијум дихроматом у киселој средини. Као резултат ове реакције, сав глицерин се разлаже на угљен диоксид и воду.
Ad
Оксидација се може јавити блаже. На пример, реакцијом са водоник пероксидом добија се алдехид или кетон. Соли гвожђа (ИИ) се користе као катализатор.
Оксидација се може извести да се добије глицеринска киселина. У овом случају, интеракција се изводи са концентрованим нитратна киселина. Једна од хидроксилних група се једноставно оксидује у карбоксилну групу. Више егзотичних киселина се такође добијају из глицерина. У интеракцији са раствором калијум перманганата настају тартронске и мезоксалне киселине. А када се оксидује са ваздушним кисеоником уз загревање у присуству баријум хидроксида, добија се смеша оксалне и мравље киселине. Глицерин јодне киселине може бити оксидисан до мрављег и формалдехида.
Индустриал апплицатионс
Због свог састава и својстава, глицерин се користи у индустрији.
- У текстилној индустрији користи се за израду меких и еластичних тканина, као и за синтезу боја и синтетичких влакана.
- Користи се у производњи одређених врста папира.
- У кожарској индустрији, његова решења се користе за штављење и тов коже.
- У пољопривреди, семе се третира глицерином како би се осигурала стабилнија клијавост.
- У индустрији боја, глицерин се користи за синтезу полирања и лакова.
- У производњи материјала за паковање, као што је целофан, користи се као пластификатор.
- Полимери на бази глицерина користе се за паковање. Папир импрегниран глицерином има ватроотпорне особине.
Примена у прехрамбеној индустрији
Глицерин је додатак исхрани Е422. Користи се као стабилизатор за очување и повећање вискозности производа. Користи се у производњи пекарских и кондиторских производа (посебно чоколаде) као средство за згушњавање и одржавање влаге. Помаже да се дода обим готових производа. Захваљујући овом додатку, хлеб може дуже остати свеж.
Ad
Екстракти на бази глицерина често се додају у напитке. Они вам омогућавају да учините њихов укус мање оштрим. Такође се користи у производњи алкохола. Додајте и дуван да регулишете влагу, елиминишете иритантан укус.
Медицинске апликације
Глицерин је део неких лекова који се користе у лечењу кожних болести. Има антисептичка својства, спречава инфекцију рана. Такође помаже у смањењу интракранијалног и интраокуларног притиска, тако да се користи у лечењу церебралног едема.
Због чињенице да је глицерин добар растварач, он се активно користи у фармаколошкој индустрији. Са овом супстанцом, може се постићи врло висока концентрација активног састојка. Он такође може дати жељену конзистенцију лекова. Често се додаје мастима и кремама, јер спречава испаравање влаге и сушење.
Примена у козметологији
Глицерин је део многих козметичких препарата: сапуни, шампони, креме, хидратантне маске. Када дође у контакт са кожом у малим количинама, задржава влагу у горњим слојевима коже. Међутим, неки тврде да честа употреба производа са базом глицерина лишава кожу природне влаге и само погоршава сувоћу. Такође, глицерин се често користи као додатак у сапуну. Тако се његова способност прања повећава.
Утицај на људско тело
Глицерин се добро апсорбује у организму, јер га дигестивни систем лако претвара у маст. Из тог разлога, не сматра се токсичним. Дневна потрошња ове супстанце није ограничена. Али не заборавите да је глицерин хигроскопан, тако да доводи до великог ослобађања волова у организму, то јест, постоји ризик од дехидрације. Из тог разлога, његова употреба у прехрамбеним производима је строго регулисана. Када дође у контакт са кожом, има и ефекат сушења. Још увијек постоје дебате о потреби употребе супстанци у козметици.
Тако је у чланку испитан састав и својства глицерина, његова примјена.