Водонична електрода: дефиниција, уређај, формула и карактеристике
У тексту који следи, дефинишемо значење термина "водонична електрода". Не знају сви шта је то. Овде ће се открити његово опште значење. Такође ћемо обратити пажњу на реакције оксидације и редукције, које су повезане са типом рада сличног објекта, а посебно ћемо говорити о деловима који га формирају.
Увод
Стандардна водонична електрода која се зове референтна електрода. Користе се током мерења електрокемијске природе. Њихова употреба се налази иу саставу галванских ћелија. Водонична електрода (ЕИ) је метална плоча или жица која апсорбује водоник у гасовитом облику. Сама плоча је уроњена у водене растворе засићене кисеоником и садржи његове јоне.

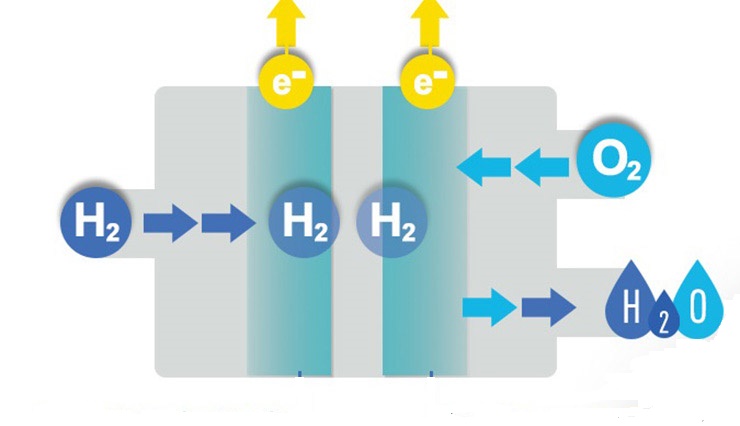
Овај елемент има потенцијал услед концентрације Х + јона у дебљини раствора. Електрода се користи као референца према којој се одређује потенцијал испитиваних хемијских реакција. Ако је притисак водоника једнак једној јединици атм., А концентрација протона одговара омјеру 1 мол / л, тада се сматра да је потенцијал ВЕ једнак нули. Ако користите платину као површину за специфичну реакцију, као и ВЕ и дефинисану електроду, онда можете посматрати занимљиву реакцију, током које се формира стабилан атом водоника:
2Х + + 2е - = Х2.
Другим речима, Х атоми су редуковани или оксидовани, тип реакције је одређен потенцијалом водоничне електроде на којој се одвија реакција.
Приликом мерења ЕМФ уређаја за галванизацију у стандардним условима (решење о којем смо горе говорили), они увек користе концепт стандардног електродног потенцијала. То је одређено врста хемијске реакције.
Оксидација и редукција
Када говоримо о електродама са водоником, поменули смо појам оксидационе и редукционе реакције, који се може јавити код атома водоника при коришћењу одговарајућих електрода.
Опоравак у хемији је феномен у којем:
- Атомска, ионска честица или молекул прихвата (сваки) један или више електрона.
- Уочава се смањење степена оксидације одређених атома у одређеној честици.
- Органске супстанце губе атоме кисеоника и / или добијају водоник.
Раније је само трећа дефиниција сматрана рестаурацијом (од средине деветнаестог века), док је прва и друга почела да се примењује тек у двадесетим годинама прошлог века. Данас се сматра да се друга дефиниција може сматрати заједничком за све процесе редукције у хемији. Уз помоћ трећег типа описа, редокс реакције су често изоловане и препознате.

Размислите више. Под оксидацијом се подразумева процес који је праћен постепеним повећањем атомске енергије оксидациона стања одређену супстанцу. То се дешава кроз "транспорт" електрона из атома донора, који је одговоран за повратак е - , на акцептор атом, који ће примити е - .
Увођење термина у научну и свакодневну циркулацију језичких јединица обавезно је академику В. М. Севергину. Ова иновација настала је на пријелазу између КСВИИ и КСИКС вијека. Научник је користио овај термин да означи процесе интеракције кисеоника (који се налази у ваздуху) са другим супстанцама. Понекад оксидационе реакције могу довести до стварања нестабилних честица и њиховог каснијег распадања на мање саставне компоненте реакције.
Апплицатион
За мерење стандардног електрокемијског потенцијала најчешће се користе водоничне електроде. Такође се користи за одређивање нивоа концентрације јона водоника и других врста јона. Чак и уз употребу ВЕ проводити истраживања која помажу да се зна производ растворљивости у односу на наведену константу брзине у току неких електрокемијских реакција.
Најважнији захтеви за референтну електроду су:
- Способност рада у температурном опсегу.
- Стабилност рада.
- Способност репродукције резултата реакције и истраживања.
- Компатибилност са испитиваном талином.
- Недостатак стационарног потенцијала.
Механизам уређаја
Уређај стандардних водикових електрода укључује:
- Платинска електрода је елемент система који има способност да искључи контаминацију раствора спољашњим низом јона током електролизе. Такви делови немају чисте површине (искључујући релативно уске потенцијалне области). Поље реакције супстанци се назива двослојни. Одликује се чињеницом да су овде у додиру само метал, јони и растварачи. А ово друго је у посебном стању. Зависно од вредности потенцијала, метал може бити обложен водоником у апсорбованом облику (ниска вредност) или са оксидима (висока вредност).
- Електролитички мост је средство за комуникацију две половине галванске структуре механизма.
- Хидроводни гас.
- Киселински раствори (обично ХЦл) са концентрацијом катиона водоника: Х + = 1 мол / л.
- Опструкција продора молекула кисеоника (из ваздуха) затварача.

Потенцијал
За израчунавање потенцијала водоничне електроде на апликацији на једну електроду је немогуће. Међутим, ова тврдња важи само за експерименталне начине.
Потенциометријска средства, која играју важну улогу у питању потенцијала електрода, заснивају се на дефиницији електромоторне силе (ЕМФ):
Е = Е 1 –Е 2 ;
Тамо где је Е дефинисана ЕМФ, и Е 1 и Е 2 делују као потенцијал електрода кола које се истражују.
Како израчунати? Потенцијал водоничне електроде једнак је броју који се може одредити помоћу Нернстове једначине:
Е = Е 0 + РТ / Нф у волу / црвеној = Е 0 + РТ / нФ у [вол] и вол / [црвеном] и црвеном
Где?
- Е 0 - стандардна вредност потенцијала редокс система;
- Р је гасна константа једнака 8,312 Ј / (К мол);
- Т је апсолутна вредност температуре;
- Ф је Фарадаи-ова константа (96485Цл / мол);
- н је број електрона који су учесници у реакцији;
- вол и црвено су индикатори активности различитих облика редокс система (оксидација и редукција);
- [ок] и [ред] - моларна концентрација супстанци одговорних за феномен оксидације или редукције;
- Гамма [ок] и [ред] - величина коефицијента активности.

Хисторицал дата
ЦЕ се одликује сложеношћу процеса рада. Међутим, постало је познато и почело се дуго користити.
ВЕ је био власнички дизајн П. П. Л. Серенсена. Користио их је као централно средство за своја истраживања, што је омогућило појаву модерне теорије пХ-материје.
ЈФ МцЦлендон је користио ХЕ у неколико првих експеримената на проучавању пХ-метрије унутар желуца. Како се то догодило? Научник је користио референтну електроду у којој је постављена водонична електрода. Ово последње је уведено заједно са пХ сондом унутар људског стомака.