Ионска веза: примери једињења
Као резултат међусобне електростатичке привлачности између молекула и атома хемијских елемената, може доћи до ионске везе. Примери таквих једињења могу се посматрати у различитим реакцијама галванских батерија, чак и једноставне сол има једињење овог типа. О томе шта је ионска веза Како се разликује од ковалентног, описано у овом чланку.
Једноставни и комплексни јони
Оба појединачна атома и њихова различита једињења су укључена у јонску везу. Сви учесници такве везе имају електрични набој и држе се заједно због електростатских сила. Постоје једноставни јони, као што су На + , К + , који су катиони; Ф - , Цл - - везано за анионе. Такође, постоје комплексни јони који се састоје од два или више атома. Примери јонске хемијске везе засноване на комплексним јонима су ОХ-, аниони, НО3-, катион НХ 4 + . Једноставни јони са позитивним набојем формирају се од атома са ниским јонизационим потенцијалом - обично су то метали главних подгрупа група И - ИИ. Једноставни јони са негативним набојем су у већини случајева типични неметали. 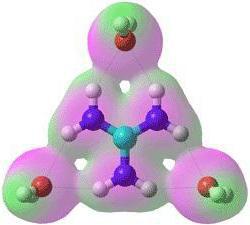
Ковалентна и јонска веза
Примери система креираних из две честице са супротним електричним набојем показују да се у таквом случају увек јавља електрично поље. То значи да електрично активни јони могу привући и друге ионе у различитим правцима. Због силе електричне привлачности и постоји јонска веза. Примери таквих једињења показују две фундаменталне разлике између јонских и ковалентних веза.
Ad
- Електрично поље јона опада са растојањем у било ком правцу. Дакле, степен интеракције између јона не зависи од тога како се ти јони налазе у простору. Из ових опсервација можемо закључити да је јонска веза скаларна, то јест, она нема правац.
- Два иона са различитим набојем не привлаче једни друге, већ и сусједне набијене ионе - различит број набијених честица супротног знака може се придружити одређеном иону. Ово је још једна разлика између ковалентних и ионских веза: потоња нема засићеност. Број везаних јона одређен је линеарним димензијама набијених честица, као и принципом да атрактивне силе иона супротних набоја треба да превладају над одбојним силама које дјелују између једнако набијених честица.
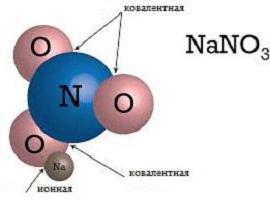
Удружења
Будући да је одсутност засићења и смера јона, они се теже комбиновати једни са другима у различитим комбинацијама. Ова имовина научници су назвали удружењем. На високим температурама, удружење је мало: кинетичка енергија молекули и јони су прилично високи, ау гасовитом стању, супстанце са ионским типом везе су у облику појединачних молекула. Међутим, средње и ниске температуре омогућавају формирање различитих структурних једињења, чије је формирање одговорно за ионски тип везе. Примери структуре супстанци у течном и чврстом стању приказани су на сликама. 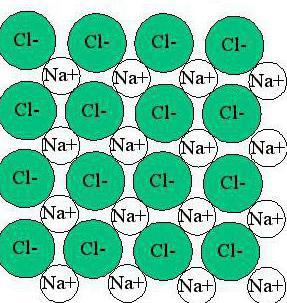
Као што видите, ствара се ионска веза цристал латтице у којој је сваки елемент окружен јонима са супротним знаком набоја. Штавише, таква супстанца има исте карактеристике у различитим правцима.
Ad
Поларизација
Као што знате, када је електрон везан за не-метални атом, ослобађа се одређена количина енергије. Међутим, приањање другог електрона већ захтева енергију, тако да формирање једноставних вишеструко наелектрисаних аниона постаје енергетски непрофитабилно. Међутим, елементи као што је СО 4 2- , ЦО 2 2- показују да комплексни, вишеструко набијени негативни јони могу бити енергетски стабилни, будући да су електрони у споју распоређени на такав начин да набој сваког атома није већи од набоја самог електрона. Таква правила диктирају стандардне ионске везе.
Примери типичних елемената који се јављају на сваком кораку (НаЦл, ЦсФ) не показују потпуно одвајање позитивних и негативних набоја. На пример, у кристалима соли, ефективни негативни набој ће бити само око 93% укупног набоја електрона. Овај ефекат је примећен код других једињења. Ово непотпуно раздвајање набоја назива се поларизација. 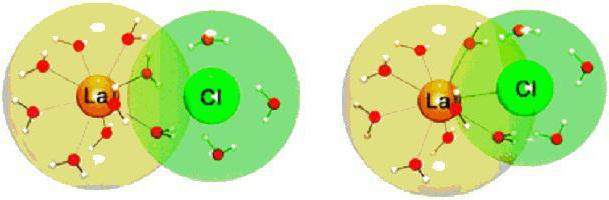
Узроци поларизације
Узрок поларизације је увек електрично поље. Спољни слој електрона доживљава највеће померање током поларизације. Међутим, треба напоменути да различити јони имају различиту поларизабилност: што је слабије повезивање спољног електрона са нуклеусом, то је лакше поларизује целокупни јон и више је деформисан електронски облак.
Поларизација јона има познато дејство на једињења која формирају јонску везу. Примјери кемијских реакција показују да водонични ион Х + има највећи поларизирајући ефект, будући да има најмању величину и потпуно одсуство електронског облака.