Ле Цхателиеров принцип у хемији
У неким случајевима, супстанце које су резултат реакције или интерагују једна са другом или се разлажу, а онда се у систему јављају истовремено две реакције: директне (формирају се реакциони производи) и обрнуте (почетне супстанце се ново синтетишу). У случају коинциденције стопа директних и инверзних процеса у систему који се разматра, јавља се равнотежа, која се назива хемијска. Ово је динамичка равнотежа, јер сама реакција не престаје, али се истом количином супстанце формира и разлаже истовремено. Са сталном температуром и притиском, ова ситуација може потрајати доста дуго. У графичком облику, приказан је у наставку. Под еквивалентном брзином подразумева се одређена константа, која је истовремено једнака брзини директне и реверзне реакције.
Ad
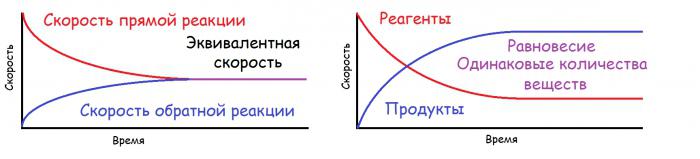
Принцип пристрасности хемијске равнотеже
Принцип помака (помака) равнотеже открио је Ле Цхателиер 1884. године. Касније га је резимирао Карл Фердинанд Браун (1887). Према томе, тренутно има име близанца - принцип Ле Цхателиер-Бровн. Овај закон се користи иу хемији иу термодинамици, електродинамици, екологији и биохемији. Постоје многе формулације, али суштина сваког од њих се своди на следеће: „Када се утицај врши на систем у равнотежи, хемијска равнотежа се помера тако да компензује ову промену (тј. Систем ће покушати да успостави равнотежу) ". Описани принцип се може јасно показати користећи следећи систем. На фиксном носачу налази се опруга. У мировању, овај систем је у равнотежи. Ако се опруга растегне, равнотежа ће се помакнути према вањском утјецају. Међутим, систем такође повећава противљење. И у једном тренутку силе опозиције и спољног утицаја постају једнаке једна другој, због чега настаје ново стање равнотеже.
Ad
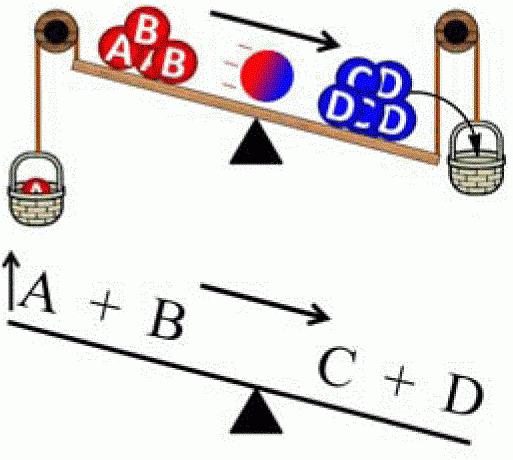
Принцип Ле Цхателиер се може користити само за системе у равнотежи, иначе ће резултати анализе бити нетачни. Постоје три главна параметра чија промена изазива промену у хемијској равнотежи: притисак, температура и концентрација хемикалија.
Температуре
Промена температуре је најчешћи узрок промене хемијске равнотеже, што је разумљиво, јер је тај фактор много лакше утицати него, на пример, притисак. Овде треба напоменути да су реакције подељене на два типа топлотним ефектом. Међу њима су: егзотермна (са топлотом) и ендотермна (са њеном апсорпцијом). Како ће се променити хемијска равнотежа у овом случају? Принцип Ле Цхателиера се у овом случају своди на следеће: са повећањем температуре, равнотежа се помера ка реакцији, која се одвија апсорпцијом топлоте, и када се она смањује, односно у супротном смеру. Дакле, ако за реакцију приказану испод да подигнете температуру, равнотежа ће се помакнути на десну страну.
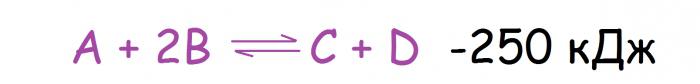
Већина директних реакција су егзотермне и реверзне реакције су ендотермне (ово није правило, већ опсервација из које се могу наћи многи изузеци).
Притисак
Како се притисак мења, следећи параметар система се трансформише - његов волумен (повећава се или смањује), тако да ефекат коришћења овог параметра има посебно јак утицај на системе у којима су присутни гасови. У овом случају, принцип хемијска равнотежа је као што следи. Ако се притисак у систему повећа, онда се равнотежа помера ка редукцији броја молекула гаса, а како се притисак смањује, равнотежа се креће у супротном смеру. Ако се број молекула гаса не промени током реакције, онда се равнотежа не мења како се притисак мења, као, на пример, у следећој реакцији.
Ad
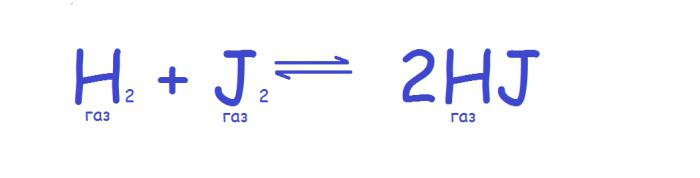
Међутим, у пракси овај принцип важи само за идеалне гасове, јер сви стварни имају различиту компресибилност. Тако, чак и ако број молекула гаса остане непромењен, равнотежа може да зависи од притиска. У пракси, то ће бити видљиво када висок притисак. У случају течних и чврстих супстанци, промена притиска заправо не утиче на равнотежу због малих запремина које заузимају такве супстанце. Када се разматрају мешовити системи, узимају се у обзир само молекули гаса.
Равнотежни помак у систему као резултат промјене концентрације било које твари укључене у реакцију
У току промене концентрације супстанце, принцип Ле Цхателиер функционише на следећи начин. Са порастом концентрације продуката реакције, равнотежа се помера ка реверзној реакцији, а са смањењем броја насталих супстанци, равнотежа се креће у супротном смеру.
Ad
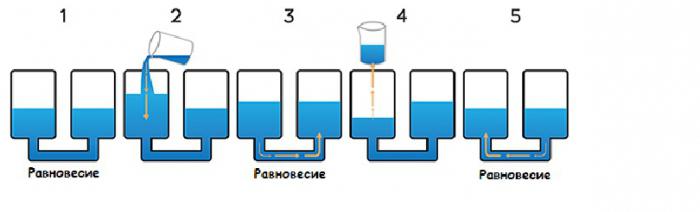
Шта се дешава ако додате инертни гас
Запремину система можете променити не само компресовањем или слабљењем притиска, већ и додавањем инертног гаса, који неће реаговати. Шта ће се десити са системом када му се дода хелиј? У ствари, највероватније се ништа неће десити, јер се однос супстанци укључених у реакцију неће променити, а процес није битан за укупни притисак система, већ делимичан за сваку компоненту.
Ефект катализатора
Количина катализатора и његово присуство уопште не утичу на померање хемијске равнотеже. Ово се дешава с обзиром на чињеницу да овај елемент једнако убрзава и директну и обрнуту реакцију, одржавајући равнотежу у систему непромијењеном.
Начин проучавања хемијске равнотеже
Детаљно разматрање хемијске равнотеже је веома важно за потпуно разумевање процеса. Једна од најчешће коришћених техника је тзв. Равнотежна метода замрзавања. Дакле, постоји брзина систем хлађења у уравнотеженом стању. Равнотежа једноставно нема времена за промјену, а на ниским температурама брзина већине процеса успорава се готово до нуле. Због тога је могуће у потпуности анализирати састав смеше на било којој температури (концентрација супстанци укључених у реакцију, при нултом степену, ће одговарати броју компоненти на температури на којој је почело смањење). Ово искуство се проводи неколико пута, а реакције се одвијају у оба смјера.
Ad
Да ли постоји потпуна неповратност?
Немогуће је потпуно променити хемијску равнотежу у једном правцу. Чак и са привидним апсолутним помаком, увек ће бити мали број молекула који ће реаговати.

У пракси, готово све реакције су реверзибилне, и колико ће овај ефекат бити видљив, често зависи од температуре (често је равнотежа једноставно снажно помакнута у једном смјеру, тако да постаје видљива само када се увјети промијене). То је због ове преваленције реверзибилности хемијске реакције проучавање равнотеже је посебно важно.
Примери синтеза у којима се хемијска равнотежа помера током производње
У производњи, хемијска равнотежа се обично помера у правцу директне реакције да би се добили, односно, реакциони производи. Постоје многи примери таквих синтеза: геттинг аммониа оксид сумпора (ВИ), азотни оксид (ИИ), итд.