Први закон термодинамике за просечну особу.
Сва људска активност се заснива на потрошњи енергије. Без енергије је тешко замислити активност организма, функционисање свих добара за људе. Важно је како унутар особе тако и за његову вањску егзистенцију. Различите индустрије не могу самостално радити, јер захтијевају енергију. Транспорт робе, грејање простора, синтеза нових супстанци у ћелијама тела - све је то због способности да се произведе рад.
Место енергије у термодинамици
Да би се одредило место енергије у овој грани науке, треба сазнати шта тачно подразумева термин "термодинамика". Ово је област физике у којој се дубински проучавају процеси конверзије енергије. Свако зна да је енергија представљена у неколико облика: она може бити хемијска, електрична, термална, механичка и светлосна. Ова грана науке има чак и своје законе и принципе, на пример, први закон термодинамике, као и неке друге. На основу тога, може се рећи да ова област знања не би постојала да својства горе описане физичке величине нису позната.
Ad
Како је трансформација енергије?

Многи људи не разумеју чињеницу преноса енергије из једне државе у другу. Али у свакодневном животу тако често користимо пролазну енергију да више не говоримо о томе одакле долази. На пример, када свакодневно улазимо у аутомобил, не мислимо да у тренутку вожње хемијска енергија улази у електричну енергију. У електричном мотору, почетна електрична енергија се претвара у механичку енергију, ау парној турбини топлота се претвара у механичку физичку величину. Уз све то постоје одређени квантитативни односи различитих облика енергије. Али током процеса трансформације јављају се неки квантитативни губици: потрошња корисне енергије је увијек већа од њене производње. Овај феномен се лако објашњава: трансформација не може без трења, током које нека енергија постаје топлота и расипа се у простору. Испоставља се да се овај дио више не може користити као корисна количина. Према томе, свака конверзија није без губитака.
Ad
Први закон термодинамике
Проучавајући процес конверзије енергије, научници су открили два основна закона. Овај чланак ће бити посвећен првом од њих. Овај закон термодинамике каже: за сваку промену - хемијску или физичку - количина енергије остаје константна. На други начин, такође се зове закон о очувању енергије. Из ове дефиниције следи да се енергија не појављује изненада и једноставно не нестаје. Ако у процесу било које активности прелази у различите облике, од једног до другог, онда се његов укупан број не мијења. Другим ријечима, енергија се не ствара или уништава, што одражава први закон термодинамике. Дефиниција у различитим изворима може варирати, али суштина остаје иста.

Историја открића овог закона
Почетак свог закона од средине КСИКС века. Немачки лекар Маиер, посматрајући како се мијења боја људске крви у тропима, размишљао је о односу између таквих физичких појмова као што су топлина и енергија. С друге стране, познати научник Џоул је скренуо пажњу на развој Мејера, нешто што му је додато. Све податке о овом закону ујединио је још један њемачки лијечник, Хелмхолтз, када је проучавао физичке основе органа перцепције - људског слуха и вида. Он је формулисао закон на такав начин да га цео свет данас познаје.
Ad
Врсте размјене енергије
Топлота која се јавља када се једна врста енергије преноси на другу утиче на промену унутрашње енергије неког објекта. Када се промени, појављује се противљење раду спољашњих сила које утичу на овај објекат. Унутрашња енергија може бити кинетичка (то је кретање атома објекта), потенцијал (он се чува у хемијским везама између атома), гравитациона енергија читавог система (тј. Ефекат на објект) гравитационе силе који се манифестују унутра). На основу ових врста, научници су идентификовали одређене врсте размене енергије.
- Први се обично схвата као предизоловани системи - нема размене енергије и других елемената одређеног система.
- Други тип су затворени системи, који се одликују недостатком размене елемената система, али се у незнатној мери мења енергија.
- Отворени системи (трећи тип размене) карактеришу размена и енергија и њихови елементи.
Цонцепт унутрашња енергија у термодинамици
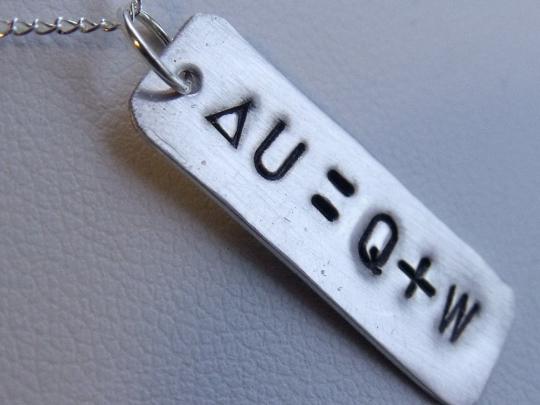
Унутрашња енергија објекта или система у термодинамици игра готово кључну улогу. У ствари, ово је комплексна комбинација неколико токова активности молекула и атома. Састоји се од врста као што је енергија ротационог и кретање напред молекула, енергија кретања атома и група атома, која се налази унутар молекула и емитује се када те честице осцилирају. Нуклеарна енергија атома и енергија интеракције молекула између њих такође су повезани са унутрашњом енергијом неког објекта. У НР зависи од почетног стања објекта и коначних показатеља његовог стања. Ова енергија је континуирана, као њен први закон термодинамике. Може се лако израчунати користећи следећу формулу: топлота која се додаје систему, умањена за рад који обавља овај систем. Овде не говоримо о природи процеса промене унутрашње енергије, чак ни о коначном стању равнотеже, јер то већ одређује други закон термодинамике.
Ad
Однос топлоте и унутрашње енергије
Ови концепти су веома блиско повезани. Претпоставља се да је топлота део унутрашње енергије система. Разумећемо шта је то врућина. Сам субјекат нема такав у уобичајеном смислу те речи. Може се рећи да је топлота енергија која пролази од објекта који има високу температуру до објекта са температуром нижом од оне прве.

Другим ријечима, то је дио унутарње енергије објекта, који се из њега преноси, јер има више температурне показатеље. Такав трансфер у физици и хемији назива се грејање.
Први закон термодинамике, хемија
Овај закон је од фундаменталне важности не само за физичке експерименте, проучавање феномена и откривање нових процеса, већ и за другу науку - хемију - и сродне индустрије. Када се проучава постојање и пренос енергије у различите форме из перспективе хемијских реакција тела или објекта, отвара се хоризонт интересантних истраживања и образаца у биоенергетској равни.
Ad

Многи сматрају да је први закон термодинамике удаљен од живота обичног човека, да су молекули и атоми подложни само разумевању од стране малог броја посвећених људи. Али ово је далеко од случаја. Основа живота сваког живог организма је метаболизам, који се не може догодити без трансформације енергије. Дакле, хемијски процеси конверзије енергије у људском телу су од посебног интереса не само за физичаре, већ и за дијететичаре и спортске инструкторе. Уосталом, знајући све карактеристике овог процеса, можете успешно помоћи људима да се ослободе вишка килограма, као и да се брину о себи уз помоћ правилно састављеног менија који се састоји од здраве хране.