Како изгледа формула аминокиселине?
Општа формула аминокиселина потврђује присуство у молекулу угљеника, водоника, кисеоника, као и садржаја две функционалне групе: карбоксилне и амино групе. Управо они објашњавају јачи карактер ових једињења, дуалност њихове структуре.
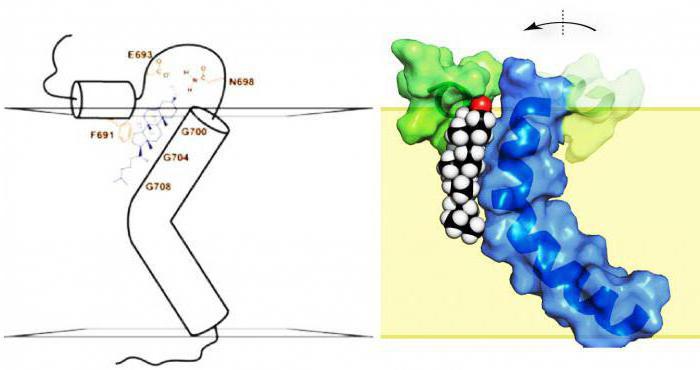
Значај спојева
Сви процеси повезани са виталном активношћу организама јављају се на молекуларном нивоу. Зато је толико важно имати потпуно разумевање карактеристика свих органска материја њихове физичке и хемијске особине.
Размотримо неке аминокиселине чије формуле и имена су познати чак и савременим ученицима.
Већ неколико деценија, дошло је до брзог развоја биохемије. Захваљујући иновативним истраживачким методама, било је могуће објаснити комплексне трансформације повезане са синтезом протеинских молекула. Информације добијене у специјализованим научним лабораторијама користе се у медицинској, фармацеутској индустрији.

Биоцхемистри феатурес
Ова наука проучава хемијски састав живих организама, њихову структуру, трансформације. Захваљујући биохемији изведена је општа формула аминокиселина, угљених хидрата и масти. Настала у деветом веку, само данас је биохемија постала савезник у лечењу комплексних наследних болести.
Својства и структура амино киселина
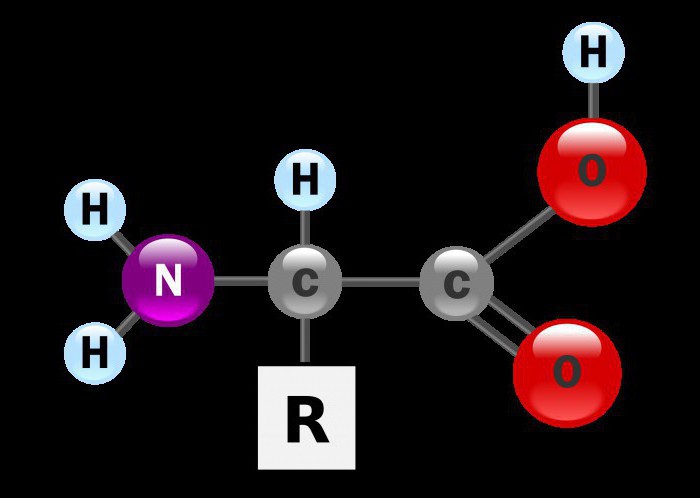
Свака формула аминокиселина је дериват амонијака и карбоксилне киселине. Тренутно има око три стотине представника ове класе, који се налазе у дивљини. Било која формула аминокиселина, без обзира на карактеристике угљеничног ланца, састоји се од две функционалне групе одједном. Свака од њих оставља траг на општим хемијским својствима ових једињења. Општа формула амино киселина је НХ2-ЦХ (Р) -ЦООХ
Радикал, који је део молекула, је дериват ограничавајућег угљоводоника.
Постоје заменљиве и есенцијалне аминокиселине, њихове формуле се разматрају у току органске хемије.
Двадесет чланова ове класе су део протеинских молекула, сматрају се њиховом основном структурном компонентом.
Међу онима које би матуранти требали да знају су: аланин, пролин, леуцин, глицин, глутамин, валин, аспарагинска киселина.
Амино Цлассифицатион
У зависности од типа аминокиселинске формуле, могу постојати неке разлике у називу. У нашем времену изолујемо једињења са неполарним радикалима. Међу њима, изаберите аланин, пролин, валин, изолеуцин, триптофан, фенилаланин. Поред тога, постоје аминокиселине које имају поларне ненапуњене радикале: серин, цистеин, глутамин, аспарагин.
Стандардна једињења су интегралне компоненте полипептидних протеинских ланаца, који делују као Л-просторни изомери. Готово сви од њих садрже асиметрични атом угљеника у структури, што објашњава слободну просторну ротацију аминокиселина.
Ова једињења су укључена у микробне ћелије, пронађене у саставу антибиотика.
Процес међусобне трансформације стереоизомера назива се рацемизација. Поред стандардних представника ове класе, нестандардне аминокиселине су такође укључене у протеинске молекуле.
У зависности од специфичности молекула протеина, у њеном формирању учествују само одређене аминокиселине. На пример, хидроксипролин је присутан у колагенском саставу.
Све аминокиселине су слаби електролити, тако да у воденом раствору пролазе само делимичну дисоцијацију. Способност једињења да буду у облику поларних јона користи се при анализи биолошких објеката како би се идентификовао аминокиселински састав. За то су погодни поступци као што је електрофореза, хроматографија са изменом јона.
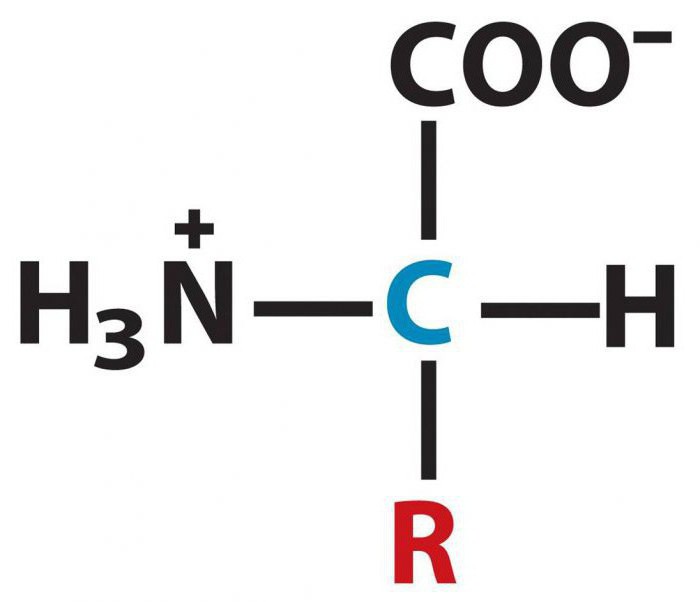
Аминокиселинска секвенца одређује карактеристике примарне структуре молекула протеина. Међу главним областима примене ове класе органских супстанци може се приметити употреба у органској синтези, фармацеутска индустрија. Аминокиселине се такође користе као храна за стоку.