Која је расподела електрона у нивоима енергије различитих хемијских елемената?
Дистрибуција електрона у енергетским нивоима објашњава металне, као и неметалне особине елемената.
Електронска формула
Постоји одређено правило према којем су слободне и упарене негативне честице смјештене на нивоима и нивоима. Размотримо детаљније расподелу електрона по нивоима енергије.
На првом енергетском нивоу постоје само два електрона. Орбитале се попуњавају када се повећа снабдевање енергијом. Дистрибуција електрона у атому хемијског елемента одговара броју секвенце. На енергетским нивоима са минималним бројем најизраженијих гравитација валентни електрони до језгра.
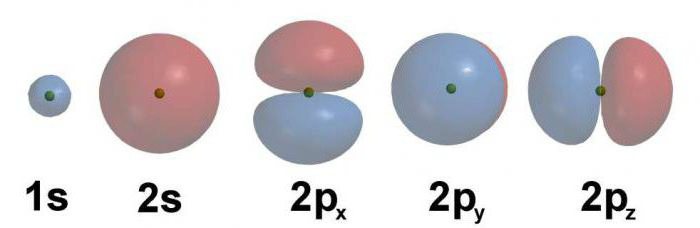
Пример електронске формуле
Размотримо расподелу електрона енергетским нивоима на примеру атома угљеника. Његов редни број је 6, дакле, шест протона са позитивним набојем налазе се унутар језгра. С обзиром да је угљеник репрезентативан за други период, карактерише га присуство два енергетска нивоа. На првом се налазе два електрона, на другом - четири.
Правило Хунда објашњава распоред у истој ћелији само два електрона који имају различите спинове. На другом енергетском нивоу постоје четири електрона. Као резултат тога, расподела електрона у атому хемијског елемента има следећи облик: 1с22с22п2.
Постоје одређена правила према којима је расподела електрона по поднивоима и нивоима.
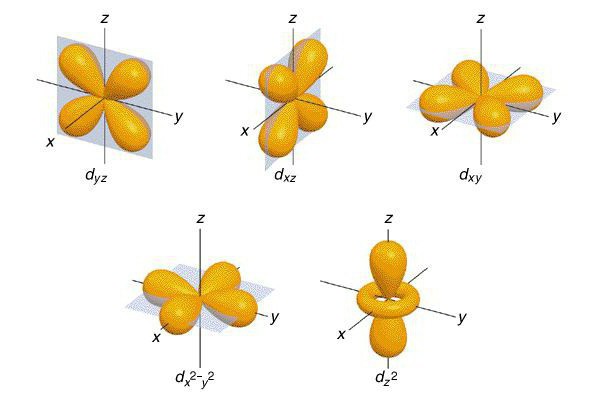
Паули принцип
Овај принцип формулисао је Паули 1925. године. Научник се сложио о могућности постављања у атом само два електрона који имају исте квантне бројеве: н, л, м, с. Имајте на уму да се расподела електрона у нивоима енергије јавља како се сток слободне енергије повећава.
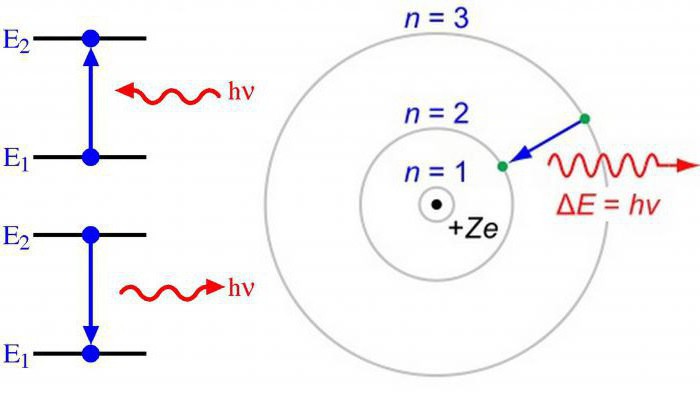
Руле Клецхковски
Пуњење енергетских орбитала врши се према повећању квантних бројева н + л и карактерише повећање енергетске резерве.
Размотримо расподелу електрона у атому калцијума.
У нормалном стању, његова електронска формула има следећи облик:
Ца 1с2 2с2 2п6 3с2 3п6 3д0 4с2.
Елементи сличних подгрупа који се односе на д- и ф-елементе, постоји "неуспех" електрона из спољашње под-нивоа, који има мању енергетску резерву, на претходни д- или ф-подниво. Сличан феномен је карактеристичан за бакар, сребро, платину, злато.
Дистрибуција електрона у атому подразумева попуњавање под-нивоа са неспареним електронима који имају исте спинове.
Тек након што су све слободне орбитале потпуно испуњене појединачним електронима, квантне ћелије су допуњене другим негативним честицама обдареним супротним спиновима.
На пример, у неоткривеном стању азота:
1с2 2с2 2п3.
Својства супстанци имају ефекат електронска конфигурација валентни електрони. По њиховом броју, можете одредити вишу и нижу валенцију, хемијску активност. Ако је елемент у главној подгрупи периодне табеле, могуће је помоћу броја групе да направи спољашњи ниво енергије, одредите га оксидациона стања. На пример, фосфор, који је у петој групи (главна подгрупа), садржи пет валентних електрона, па је способан да прихвати три електрона или да да пет честица другом атому.
Изузеци од овог правила су сви представници подгрупа периодне табеле.
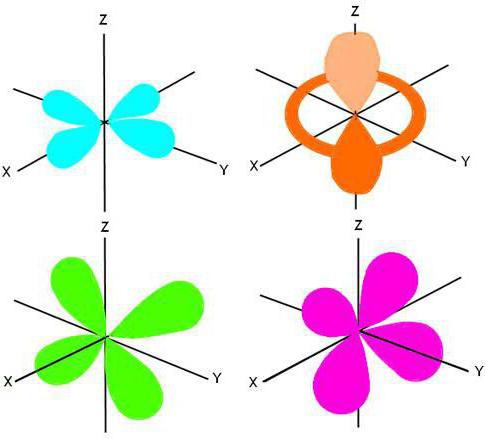
Фамили Феатурес
У зависности од структуре спољашњег енергетског нивоа, постоји подела свих неутралних атома у периодном систему на четири породице:
- с-елементи су у првој и другој групи (главне подгрупе);
- п-породица се налази у ИИИ-ВИИИ групама (А подгрупе);
- д-елементи се могу наћи у сличним подгрупама од И до ВИИИ групе;
- Ф-фамилија се састоји од актинида и лантанида.
Сви с-елементи у нормалном стању имају валентне електроне на с-подниво. Присуство слободних електрона на с- и п-нивоима је карактеристично за п-елементе.
Д-елементи у неоткривеном стању имају валентне електроне и на последњем с- и на последњем д-под-нивоу.
Закључак
Стање електрона у атому може се описати помоћу скупа основних бројева. У зависности од карактеристика његове структуре, можемо говорити о одређеној количини енергије. Користећи Хунд, Клецхковски, Паули правило за било који елемент укључен у периодном систему, можете креирати конфигурацију неутралног атома.
Електрони који се налазе на првим нивоима имају најмању количину енергије у неизраженом стању. Када се загрева неутрални атом, примећује се прелаз електрона, који је увек праћен променом броја слободних електрона, што доводи до значајне промене у брзини оксидације елемента и промени његове хемијске активности.