Ацетилен: хемијска својства, припрема, употреба, мјере опреза
Ацетилен (или, према међународној номенклатури, етин) је незасићен угљоводоник који припада класи алкина. Хемијска формула ацетилена је Ц2Х2. Атоми угљеника у молекулу повезани су троструком везом. Он је први у својој хомологној серији. То је безбојни гас. Врло запаљиво.
Геттинг
Све методе индустријске производње ацетилена конвергирају се у двије врсте: хидролиза калцијевог карбида и пиролиза разних угљиководика. Ово последње захтева мање енергије, али чистоћа производа је прилично ниска. Метода карбида је супротна.
Суштина пиролизе је да се метан, етан или други лаки угљоводоник претварају у ацетилен када се загревају на високе температуре (од 1000 ° Ц). Загревање се може вршити помоћу електричног пражњења, плазме или горећег дела сировине. Али проблем је у томе што се као резултат реакције пиролизе може формирати не само ацетилен, већ и много других производа који се касније морају збринути.
Ad
2ЦХ4 → Ц2Х2 + 3Х2
Карбидна метода се заснива на реакцији интеракције калцијум карбида са водом. Калцијум карбид се добија из његовог оксида спајањем са коксом у електричним пећима. Дакле, тако висока потрошња енергије. Али чистоћа ацетилена добијеног на овај начин је изузетно висока (99,9%).
ЦаЦ2 + Х20 → Ц2Х2 + Ца (ОХ) 2
У лабораторији, ацетилен се такође може добити дехидрохалогенацијом дихалогенских деривата алкана употребом алкохолног алкалног раствора.
ЦХ2Ц1-ЦХ2Цл + 2КОХ → Ц2Х2 + 2КЦл + 2Х2О
Физичка својства ацетилена
Ацетилен је плин без боје и мириса. Иако му нечистоће могу дати мирис чешњака. Практично нерастворљив у води, слабо растворљив у ацетону. На температури од -83.8 ° Ц је укапљен.
Ad
Хемијска својства ацетилена
На основу троструке везе ацетилена, она ће бити карактерисана реакцијама додавања и реакције полимеризације. Атоми водоника у молекулу ацетилена могу бити замењени другим атомима или групама. Према томе, може се рећи да ацетилен показује киселинска својства. Испитајмо хемијске особине ацетилена на специфичне реакције.
Реакције прилога:
- Хидрогенација. Изводи се на високој температури и у присуству катализатора (Ни, Пт, Пд). На паладијском катализатору може бити непотпуна хидрогенација.
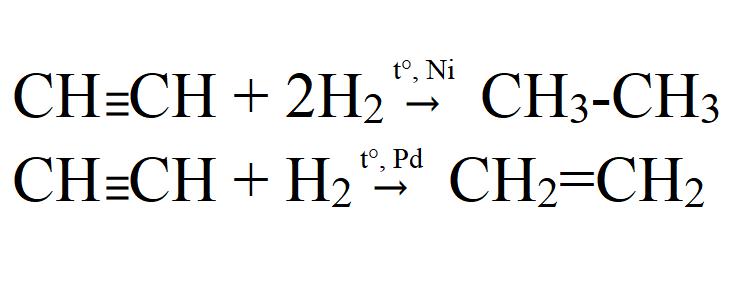
- Халогенација Може бити и делимична и потпуна. Лако иде чак и без катализатора или грејања. У светлу хлорисања долази до експлозије. У исто време, ацетилен се потпуно разлаже на угљеник.
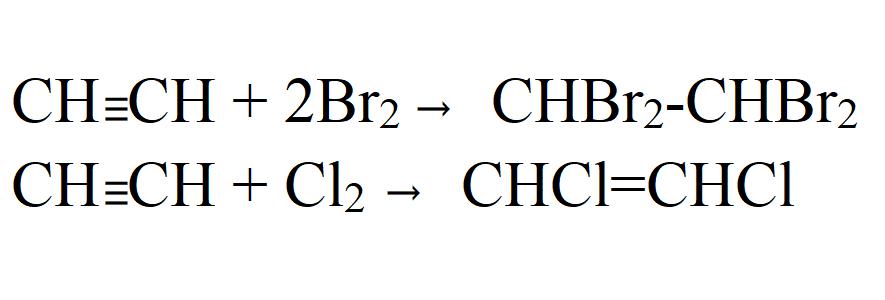
- Приступање сирћетној киселини и етил алкохолу. Реакције иду само у присуству катализатора.
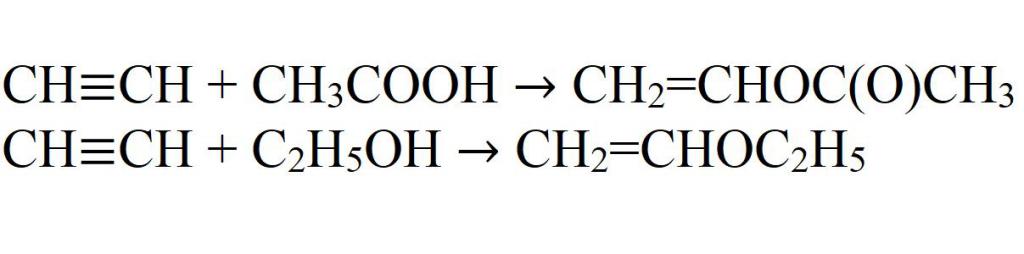
- Додавање цијановодоничне киселине.
ЦХ2ЦХ + ХЦН → ЦХ2 = ЦХ-ЦН
Реакције замене:
- Интеракција ацетилена са метал-органским једињењима.
ЦХ = ЦХ + 2Ц2Х5МгБр → 2Ц2Х6 + БрМгЦ2ЦМгБр
- Интеракција са металним натријумом. Потребна је температура од 150 ° Ц или претходно растварање натријума у амонијаку.
2ЦХ≡ЦХ + 2На → 2ЦХ2ЦНа + Х2
- Интеракција са комплексним солима бакра и сребра.
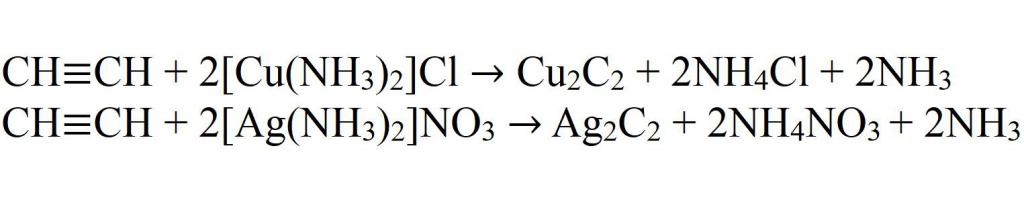
- Интеракција са натријум амидом.
ЦХ≡ЦХ + 2НаНХ2НаЦ2ЦНа + 2НХ3
Реакције полимеризације:
- Димеризатион. У овој реакцији, два молекула ацетилена су спојена у један. Потребан је катализатор - моновалентна сол бакра.
- Тримеризација. У овој реакцији, три молекуле ацетилена формирају бензен. Потребно је загревање на 70 ° Ц, притисак и катализатор.
- Тетрамеризатион. Као резултат реакције добија се осмерочлани циклус - циклоктатетрен. Ова реакција такође захтева мало топлоте, притиска и погодног катализатора. То су обично комплексна једињења двовалентног никла.
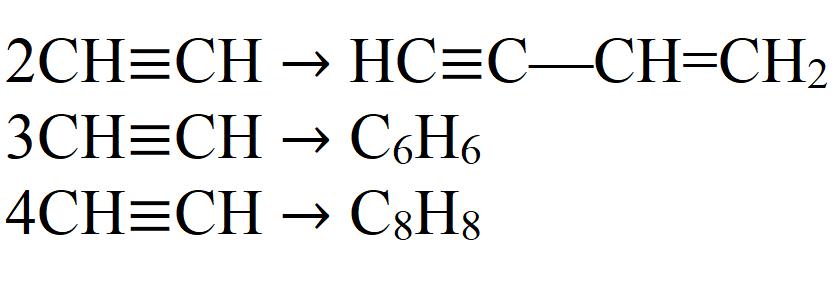
То нису све хемијске особине ацетилена.
Апплицатион
Структурна формула ацетилена показује нам прилично јаку везу између атома угљеника. Када се разбије, на пример током сагоревања, ослобађа се много енергије. Из тог разлога, ацетиленски пламен има рекордно високу температуру од око 4000 ° Ц. Користи се у бакљама за заваривање и сечење метала, као иу ракетним моторима.
Ad
Пламен сагоревања ацетилена такође има веома велику осветљеност, тако да се често користи у уређајима за осветљење. Користи се у експлозивној технологији. Истина, не примењује се сам ацетилен, већ његове соли.
Као што се може видети из различитих хемијских својстава, ацетилен се може користити као сировина за синтезу других важних супстанци: растварача, лакова, полимера, синтетичких влакана, пластике, органског стакла, експлозива и сирћетне киселине.
Сигурност
Као што је већ поменуто, ацетилен је запаљива супстанца. Са кисеоником или ваздухом, он је у стању да формира изузетно запаљиве смеше. Да би се изазвала експлозија, довољна је једна искра од статичког електрицитета, загревање до 500 ° Ц или мали притисак. На температури од 335 ° Ц чисти ацетилен се спонтано запали.
Ad
Због тога се ацетилен чува у цилиндрима под притиском, који се пуне порозном супстанцом (плавац, активни угаљ, азбест). Тако се ацетилен дистрибуира кроз поре, смањујући ризик од експлозије. Често се ове поре импрегнирају ацетоном, због чега настаје ацетиленски раствор. Понекад се ацетилен разблажује са другим, више инертним гасовима (азот, метан, пропан).
Овај гас такође има токсични ефекат. Када се удахне, почиње тровање тела. Знаци тровања су мучнина, повраћање, тинитус и вртоглавица. Велике концентрације могу чак довести до губитка свијести.