Основни закони хемије. Основни појмови и закони хемије
Неће бити сувишно прво дефинисати појам “ хемија ” - то је најважнија наука која проучава структуру супстанци, њихове трансформације. Обухвата следеће основне појмове и законе (хемија):
1. Хемијске особине било које супстанце се успостављају на основу стања електронских љуски (спољашњих) молекула, а атоми који га формирају. Језгра и унутрашњи електрони остају готово непромијењени током кемијских процеса.
2. Предмет хемије - хемијски елементи, њихове комбинације (атоми, једноставни, комплексни: иони, карбени, слободни радикали, молекули, радикални јони, као и материјали, хемијска једињења, њихове асоцијације: кластери, клатрати, асоцијати, солвати, итд.) ). Има их огроман број, и константно расте због чињенице да ова наука сама формира свој објект (већ је познато око 10 милиона хемијских једињења).
Ad
3. Супстанца је врста материје са одређеном масом одмора која се састоји од елементарних честица као што су електрони, неутрони, протони, мезони итд. Ова знаност проучава супстанце које се претварају у атоме, јоне, молекуле и радикале. То су: сложена, једноставна (хемијска једињења).
4. Најмања компонента хемијског елемента која се не може хемијски раздвојити и која задржава сва оригинална својства дефинисана електричном љуском и нуклеарно наелектрисање се назива атом . Део супстанце (једињења) која садржи идентичне атоме назива се хемијски елемент , од којих сваки одговара комплексу одређених атома.
5. Молекул је микрочестица која има 2 или више атома и способна је за аутономно постојање. Има константан квантитативни, квалитативни састав атомских језгара, као и константан број електрона; опремљена јединственим својствима. 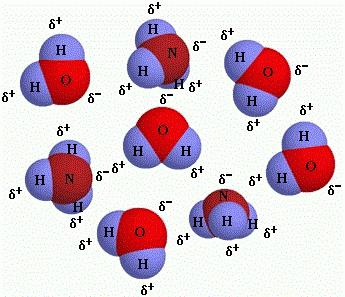
6. Једноставне супстанце формирају атоми само првог хемијског елемента, због чега су посебан облик његовог постојања у слободном стању (О₂, Х₂, Хе, О₃, С₈), а сложене супстанце формирају различити хемијски елементи и могу имати константан састав ( далтониди или стехиометријска једињења) или варијабилни (бертхоллидес или нестехиометријска једињења).
Ad
7. Јони су моноатомске или полиатомске честице са електричним набојем. Позитивно набијени иони су катиони, а негативно аниони. У облику гаса, они су у свом слободном стању.
8. Валенција је способност атома да замени или везује друге атоме (атомске групе) и формира хемијске везе. Валенцна мера је број атома водоника (кисеоника) који су везани за хемијски елемент. Водоник је моновалентан и кисеоник је бивалентан.
9. Хемијске реакције су трансформација неких супстанци (почетних једињења) у супстанце различите врсте (продукти реакције), које не мењају језгре атома.
10. Реагенси - полазни материјали или једно од најактивнијих почетних једињења, које одређују смер реакције. 
Порекло поменутог термина
Постоје два стајалишта у погледу његовог поријекла:
- Од древног имена Египта - "Хем", који се дословно преводи као "црни", "тамни". Вероватно због боје земље у долини р. Неил
- Од старогрчког израза "цхемеиа" - уметнички облик топљења метала.
Модерно име долази од латинске речи "цхимиа". Она је интернационална (на пример, у немачкој хемији, у француској химији, у енглеској хемији). Познато је да је предак термина "хемија" грчки алкемичар Зосима (В цент.).
Ad
Органска хемија: дефиниција, органска једињења
То је наука која проучава једињења угљеника која се производе од стране живих организама. До данас је познато више од 2 милиона органских једињења, подељених у групе као што су алкени, алкохоли, алкани, итд. Већина њих је укључена у састав уља и заузима водеће позиције у производњи: боја, лекова, пластике, козметике. .
Састав органских једињења: атоми угљеника и други елементи (кисеоник, водоник), који су повезани јаким ковалентним везама. Једињења која се формирају од атома угљеника са водоником се називају угљоводоници .
Главна компонента природног гаса је једноставан угљоводоник (метан - ЦХ₄). Органска хемија тачно истражује органска једињења разликују се по породицама, а које се називају хомологне серије .
Горе наведене групе (алкени, алкани) припадају различитим хомологним серијама, од којих свака укључује хиљаде једињења. Њихова локација у овој серији одређена је бројем угљеникових атома у молекулима (на пример, молекули првог споја из низа алкана: метан - 1 атом угљеника, етан - 2, пропан - 3).
Ad
Имена једињења која садрже 1 атом угљеника почињу префиксом "мет", 2 атома - "ет", 3 атома - "проп." Таква једињења, која припадају првој хомологној серији, имају слична хемијска својства, али различита физичка. А она једињења која имају мало угљеникових атома су гасови, довољно велики број атома су течности, а чврсте материје су прекомерно презасићене атомима.
Број органских једињења је прилично велик због способности атома да формирају дуге ланце или прстенове. Ове структурне јединице су спојене заједно због ковалентних веза (њихови електрони спољашњих љуски су "опште доступни"). Облици угљеника су једноставни (сваки атомски пар дели између њих 1 пар електрона), 2. или чак 3. ковалентне везе (два и, појединачно, три пара електрона).
Након реакције довољно засићеног једињења (органског) са другим једињењем, постојеће везе су прекинуте, а неки атоми замењени другим.
Основни стехиометријски закони хемије
Они су укључени у овај део хемије, као стехиометрија. Познато је да садржи следеће основне законе хемије:
- Гаи-Луссац;
- Авогадро;
- еквиваленти и очување масе;
- вишеструке везе;
- конзистентност састава.
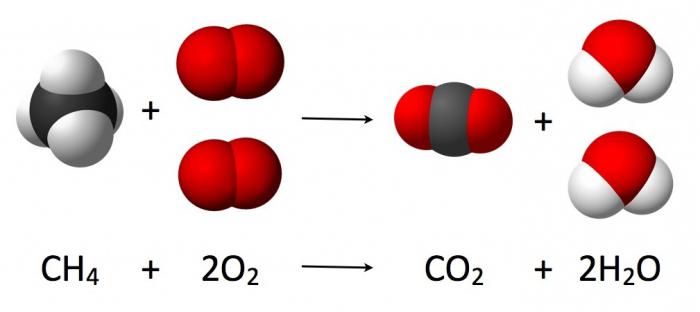
Суштина закона очувања масе и енергије
Основу формирања хемијских једначина чини метода материјалне биланце, чија је основа закон очувања масе (хемије). Према његовим речима, маса реагенса је идентична маси коначних производа реакције.
Први пут га је открио МВ Ломоносов 1748. године. Тада је француски хемичар А. Лавоисиер (1789) дошао до истих резултата.
У току хемијске реакције, број интеракционих атома је непромјењив (уочава се само њихово преграђивање, праћено уништењем почетних супстанци). Проточна интеракција кисеоника са водоником, која доводи до формирања воде, може се записати једнаџбом одговарајуће хемијске реакције (као на слици испод). 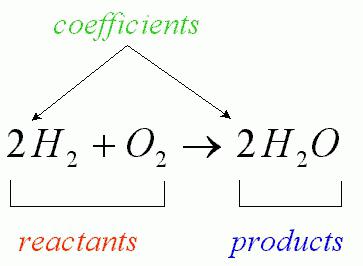
Формуле ових хемијских једињења су коефицијенти који се називају "стехиометријски". Модерна формула се дешифрује на следећи начин: збир маса и енергија унутар изолованог система је константан.
Ad
Има облик: Е = м · ц², где
ц је брзина светлости (3 · 10⁸ м / с);
Почетком 20. века, Алберт Ајнштајн је био у стању да докаже исправност ове једначине за било који облик материје.
Суштина закона константности
Формулирали су је 1808. године француски кемичари Ј. Проуст и Ц. Л. Бертхоллет. У њему се наводи да свака појединачна супстанца добијена било којом познатом методом увијек има сталан квантитативни и квалитативни састав.
Закон константности материје (хемија) омогућио је да се састав супстанци изрази хемијским знаковима, одговарајућим индексима (на пример, Х20, Ц2Х20Х, ЦХ3). Почетком 20. века (1912–1913), еминентни руски професор Н. С. Курнаков је открио постојање једињења променљивог састава, које је назвао бертхоллидес .
Ако се сећате наредне лекције из хемије, закон константности састава се сматра правичним за супстанце које имају молекуларну структуру. Као што је већ раније споменуто, поред супстанци са константним саставом, постоје и супстанце са варијаблама: измјењивање монолитних структурних јединица (иона, атома) одвија се у супротности с утврђеном периодичношћу.
Због присуства једињења варијабилног састава, закон константности састава (хемија) садржи појашњења о томе да постоји директна веза између структуре састава једињења и метода за њихово добијање: ако постоји молекуларна структура, састав се не мења у зависности од било ког поступка припреме, већ у ситуацији када је структура не-молекуларна (ионска, атомска и метална решетка) - састав зависи од специфичних услова производње. 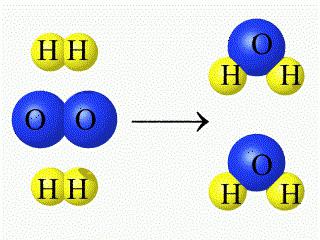
Закон о еквивалентима формулације
Открио га је њемачки кемичар Н. Рицхтер и састоји се од сљедећег: масе супстанци које међусобно дјелују (кемијски) једнаке су или су вишеструке масе њихових кемијских еквивалената (ступањ кемије 11).
Еквивалент је условна или стварна честица супстанци које могу заменити, ослободити, прикачити, итд., Што је једнако првом водониковом јону јоноизмењивих или киселинско-базних реакција; Редокс реакције 1. електрона.
На други начин, може се рећи да мол еквивалената (одређена количина супстанце која садржи онолико структурних елемената колико има угљеникових атома у 12 г изотопа ¹2Ц) реагује са истим истим молом еквивалената, али различите супстанце .
Математички, овај закон је:
мₐ: Мₔ (А) = мᵦ: Мₔ (Б), где
мₐ је маса неке супстанце А,
мᵦ је маса супстанце Б,
Мₔ (А) је масени (моларни) еквивалент одговарајуће супстанце А,
Мₔ (Б) - маса (моларна) еквивалент супстанце Б.
Догађа се да се једна реагујућа супстанца у почетку налази у чврстом стању, а друга у гасовитом стању. Онда се закон који се разматра изражава следећом формулом:
мₐ: Мₔ (А) = Вб: Вₔ (Б).
Суштина закона вишеструких односа
Формулисао га је енглески хемичар Д. Далтон 1803. године. Његова суштина је да у ситуацији када два хемијска елемента стварају неколико једињења (молекуларних), масени удјели било ког од њих су повезани као цели бројеви (хемија степен 11).
У процесу интеракције кисеоника и азота добија се 5 оксида. У настајућим молекулима на 1 г азота рачунају се следеће количине кисеоника у грамима: 0,57, 1,14, 1,71, 2,28, 2,85. Корелирају се у пропорцијама: 2: 1, 1: 1, 2: 3, 1: 2, 2: 5 (композиције: НО, НО, Н = 0, НО2, Н20).
Авогадрови закони и односи волумена
Суштина потоњег: у идентичним условима, запремине гасовитих реагенса су међусобно повезане и обима насталих гасовитих продуката као целих бројева (Ј. Гаи-Луссац).
У случају интеракције гасовитих супстанци, њихове запремине су повезане као коефицијенти (стехиометријске) једначине реакције: 2Х₂ + О₂ = 2Х2О (г).
Што се тиче Авогадров закон, затим је његова формулација следећа: идентични запремини гаса у истим условима садрже исти број молова.
Математички, може се представити на следећи начин:
н (к) = м: М (к), где
н (к) је потребан број молова неке супстанце,
м је маса одговарајуће супстанце
М (к) је моларна маса реактанта.
Последице овог закона:
- 1 моларна гасна супстанца замењује запремину од 22,4 литара (под нормалним условима).
- 1 мол гасовита супстанца садржи идентичан број молекула, који је једнак 6.023 1023 - Авогадров број.
- Код познатих маса гасовитих супстанци или њихових моларних маса, могуће је одредити релативну густину: мᵦ: мᵦ = пₐ: пᵦ, где
пₐ, пᵦ - густина супстанци А и Б, г / цм³.
Тако су горе наведени основни закони хемије (стехиометријски). Следеће ће се сматрати гас и термодинамика.
Гасни закони хемије
Само четири закона:
1. Боиле - Мариотта: ако је температура константна вриједност (Т = цонст) унутар изотермалног процеса, тада тлак произведен масом плина обрнуто је пропорционалан његовом волумену: пВ = цонст.
2 Гаи-Луссац: ако је притисак гаса константан (п = цонст) унутар исобариц процесс тада је његова запремина директно пропорционална апсолутној температури: В: Т = цонст. 
3. Чарли: ако је запремина гаса константна вредност у оквиру изохорног процеса, онда је њен притисак директно пропорционалан апсолутној температури: П: Т = цонст.
4. Комбиновани гас: пВ: Т = цонст.
Ово су основни закони гасне хемије.
Закони хемијске термодинамике
Три су:
1. Закон о очувању енергије (хемија): ако у току било ког процеса нестане енергија прве врсте, онда различит облик енергије "долази" да га замени иу различитој количини која је строго еквивалентна првом. Према томе, може се рећи да у оквиру сваког изолованог система, укупна резерва енергије остаје непромењена.
2. Унутар граница изолованог система, процеси који се јављају спонтано повећавају ентропију (трансформацију) система.
3. Ако температура тежи нули, ентропија система остаје непромењена (независно од њених параметара).
То су основни закони термодинамике (хемије).
Суштина закона маса
Ово је основни закон физичке хемије. Закон дејства маса (у хемији): брзина којом се одвија хемијска реакција је пропорционална производу концентрација реагенса.
У случају хомогене реакције са првим ступњем (А + Б - продукти реакције), овај закон се може представити као једнаџба:
в = к · цₐ · цᵦ, где
в је брзина реакције
цₐ, цᵦ - концентрације реагенса, респективно, А и Б, мол / л,
к је константа брзине реакције.
Закон дејства маса (у хемији) омогућава да се идентификује физичко значење ове константе: она је једнака брзини реакције при концентрацијама реактаната на 1 мол / л или је вредност њиховог производа једнака једној. Константа зависи од температуре, природе реагенса, али не и од њихове концентрације.
Периодни закон: формулација, улога
Препознато је да је овај закон најважније достигнуће у хемији, може се рећи, основа модерне хемије. Након његовог открића, престала је бити искључиво дескриптивна наука, такозвана научна предвиђања постала је могућа.
Периодични закон (хемија) је 1869. године открио познати руски научник Дмитри Ивановић Мендељејев. Званични текст: “Својства једноставних тијела, као и облици и својства спојева елемената су у периодичкој зависности од величине атомских тежина елемената”.
То су основни закони хемије (физички).
Хемија као систем знања о супстанцама и њиховим трансформацијама
Знање се изводи из поузданих опширних информација о једињењима и елементима (хемијским), њиховим реакцијама, понашању у оквиру природне и вештачке средине. Постојећи критеријуми за поузданост проучених чињеница, као и начини њиховог организовања, континуирано се развијају. Главне генерализације се преносе на научне законе, чија формулација омогућава отварање нових фаза хемије (на пример, основни закони хемије: Далтонов закон, Мендељејев периодични закон, итд.). Теоријски аспекти, у којима се примјењују специфични појмови, омогућавају објашњење и предвиђање чињеница ужег домена предмета. Дакле, може се рећи да знање, подржано искуством, постаје чињеница тек након теоријске интерпретације.
Дакле, прва хемијска теорија је теорија “флогистона” (она је препозната као нетачна), она је промовисала формирање модерне хемије, с обзиром на чињеницу да је она распршене чињенице спојила у један систем, допуштајући да формулише низ нових питања. Али структурна теорија (Ф. Кекуле, А. М. Бутлеров) је помогла да се поједностави и објасни опсежни материјал органске хемије и одреди убрзани развој хемијске синтезе, као и проучавање структуре органских једињења.
Наука у питању као знање је веома динамичан систем. Еволутивна природа процеса акумулације знања периодично се прекида револуцијама - радикалним преструктурирањем система теорија, метода и чињеница са појавом новог скупа концепата или чак фундаментално новог стила свјетоназора и мишљења. Тако су радови Антоине Лаурент Лавоисиер (увођење квантитативних метода експеримента, материјалистичка теорија оксидације, развој хемијске номенклатуре), периодични закон Мендељејев, развој нових аналитичких метода (кроматографија, микроанализа), настанак нових подручја која формирају нови предмет хемије и утичу на сва његова поља (на пример, физичка хемија, заснована на хемијској кинетици и термодинамици).
Такође треба напоменути да је хемијско знање опремљено развијеном структуром, чији је хемијски оквир главне хемијске дисциплине формиране у 19. веку (органска, аналитичка, неорганска и физичка хемија). Касније, у процесу њене еволуције, појавиле су се многе нове дисциплине (био- и кристална хемија, итд.) И инжењерска индустрија - хемијска технологија.
Дакле, у чланку се разматрају основни појмови и закони хемије.