Хемијска својства алкадиена - незасићених угљоводоника
Карактеристика свих незасићених угљоводоника је присуство пи-веза у њиховим молекулима, које се називају и двоструке везе. Алкадиени су отворени неразгранати или разгранати угљенични ланци и имају две двоструке везе. У чланку ћемо проучити структуру молекула, као и главну хемијске особине алкана, алкенес, алкадиенов.
Структура молекула и општа формула
Молекуларне формуле диенских угљоводоника поштују општу формулу: Ц н Х 2 н -2 . Ацетиленски угљоводоници имају исту формулу, тако да су изомери незасићених угљоводоника са две пи везе. У структури молекула алкадиена разликују се супстанце у којима су двоструке везе раздвојене једноставним сигма везама. Овај тип једињења се назива коњугат. Најпознатији од њих је бутадиен. Такође су позната једињења у којима две двоструке везе припадају истом атому угљеника.
Ad

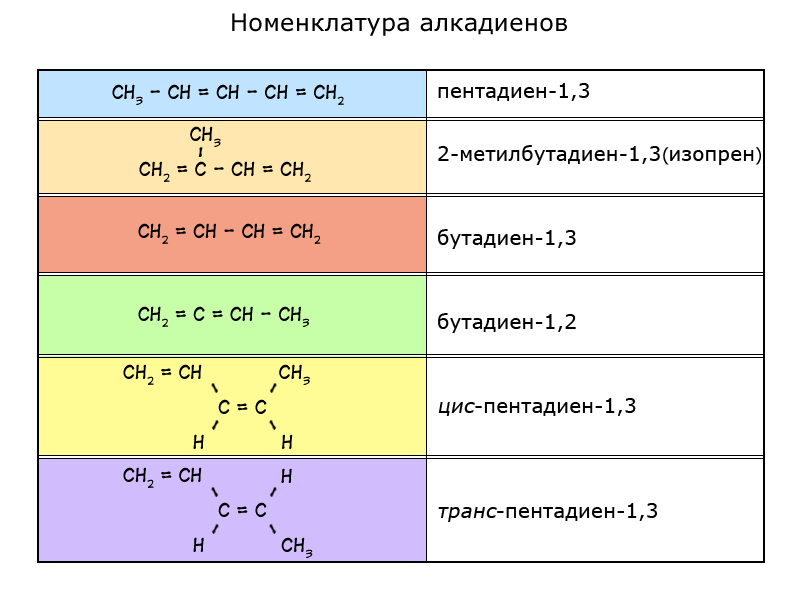
Номенклатура
На хемијска својства алкадиена утиче структура њихових молекула, односно просторни распоред атома у односу један на други. Номенклатура ове класе угљоводоника формирана је од имена алкана, суфикса -а у којем се мијења у –диен, на примјер пентан - пентадиен, бутан - бутадиен. Изомерија једињења зависи од два фактора: локације незасићених веза и броја атома угљеника који формирају скелет молекула.
Хемијска својства коњугованих алкадиена
Присуство две пи-везе, одвојене једноставном везом, обезбеђује незасићене угљоводонике са способношћу да веже атоме других хемијских елемената, као што су халогени или водоник. У већини реакција, додавање се дешава код екстремних атома угљеника. Броминација бутадиена може бити представљена са два узастопна процеса. Прво, на алкадиен је везана једна честица брома и формирана је супстанца - дериват алкена, назван дибромобутен. Други молекул брома се додаје преосталој пи вези у тачки њене руптуре, подложан прекомерној количини мола халогена, и као резултат тога, формира се дериват 1,2,3,4-тетрабромобутана. Хемијске особине се могу разликовати по способности реакција адиције. алкани, алкени, алкадиенс, алкин.
Ad
Засићени угљоводоници услед одсуства двоструких веза у њиховим молекулима, они нису у стању да додају атоме других елемената. Карактерише их супституција атома водоника са честицама, на пример, хлор, бром или јод. Највећи практични значај међу свим представницима диенских једињења је бутадиен, који се у хемији органске синтезе користи као сировина за производњу гума.
Производња бутадиена
Најпознатији поступак екстракције супстанце је метода С. В. Лебедев, у којој се преко катализатора пропушта парни етанол. Једначина реакције ће бити следећа:
2Ц3Х5ОХ → Х2Ц = ЦХ-ХЦ = ЦХ2 + 2Х2О + Х2
Међутим, тренутно у индустрији, највећи део бутадиена се добија реакцијом дехидрације бутана, који је део придружених гасова и отпадних гасова из индустрије за прераду нафте у хемијској производњи. Други важан диенски угљоводоник, изопрен, може бити миниран 2-метилбутан (изопентан) дехидрогенацијом. Изопренска гума се разликује од дивинила вишим степеном отпорности на хабање и отпорности на кисело окружење. Хемијска својства алкадиена, посебно, реакције полимеризације омогућавају вам да их користите за производњу синтетичких каучука са различитим својствима.
Ad
Полимеризација и кополимеризација
И изопрен и бутадиен могу се претворити у полимере - органска једињења високе молекуларне тежине. Такође су способни за кополимеризацију, тј. Формирање полимера заједно са другим угљоводоницима са двоструким везама у молекулима. Услови за појаву таквих реакција су веома сложени и различити: високи притисак, катализатори, загревање реакционе смеше. Међутим, одлучујући фактор полимеризације је просторна структура молекула мономера.
Хемијске особине алкадиена, алкена и алкина су међусобно сличне не само у њиховој способности додавања реакција, већ и у процесе полимеризације. Производи добијени таквим реакцијама - полиетилен, полипропилен, стирен, изопрен и бутадиен гуме - нашла широку примјену у индустрији, животу, грађевинарству и пољопривреди.

Својства гуме
Производи синтетске полимеризације 2-метилбутадиена и бутадиена - гума, као и материјал добијен њиховом вулканизацијом (гума) - имају низ јединствених карактеристика. Изузетно су отпорни на хабање и хабање, не растварају се у агресивним хемијским срединама, отпорни су на промјене температуре околине и прекомјерне влажности. Пронашли су примјену у аутомобилској и грађевинској опреми, у производњи зракоплова, у производњи производа лаке индустрије. Први каучук синтетизирао је 1932. совјетски кемичар С. Лебедев, али је био мање издржљив од природног материјала добивеног из сока тропске биљке, хевеа. Хемијске особине алкадиена, посебно изопентана, омогућиле су синтезу изопренске гуме користећи полимеризациону реакцију, у којој су мономерне јединице биле стриктно оријентисане у простору. Добио је име полимерне стереорегуларне структуре. У будућности, у производњи полимера из дивинила и стирена, синтетисана је још једна гума помоћу слободно радикалног механизма са просторном уређеношћу молекула - стирен-бутадиена, који има повећану отпорност и отпорност на трошење.

У нашем чланку смо разматрали припрему и хемијска својства алкадиена, а такође смо открили поља примене ових једињења у индустрији и свакодневном животу.