Да ли је метода титриметријске анализе шта је то?
Титриметријска метода анализе (титрација) омогућава спровођење волуметријске квантитативне анализе и широко се користи у хемији. Његова главна предност је разноврсност метода и метода, због чега се може користити за рјешавање различитих аналитичких задатака.
Принцип анализе
Титриметријска метода анализе заснива се на мерењу запремине раствора познате концентрације (титранта) који реагује са испитиваном супстанцом.
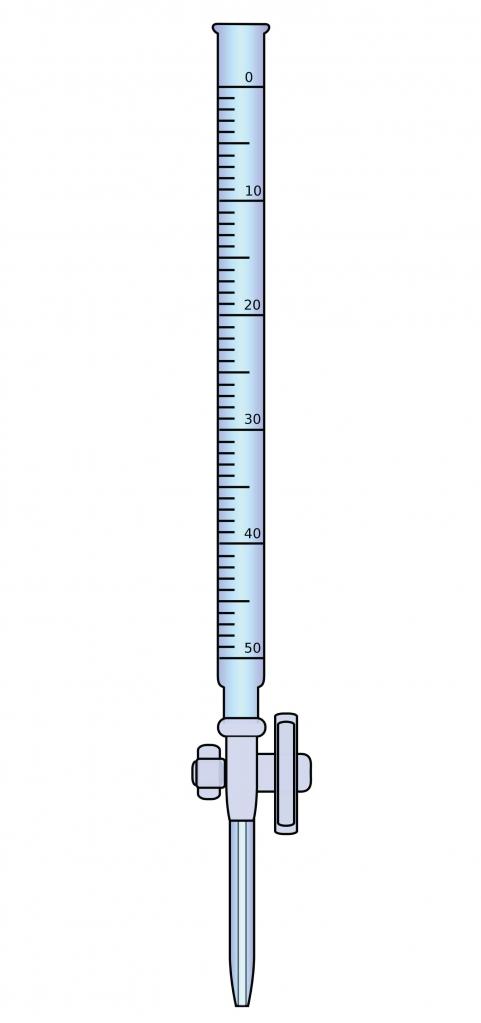
За анализу ће вам бити потребна посебна опрема, наиме бирета - танка стаклена цев са примењеном градацијом. Горњи крај ове цеви је отворен, а на доњем се налази зауставни вентил. Калибрирана бирета помоћу левка испуњава титрант на нулу. Анализа се врши до крајње тачке титрације (ЦТТ), додавањем мале количине раствора из бирете у испитивану супстанцу. Крајња тачка титрације је идентификована променом боје индикатора или неке физичко-хемијске особине.
Ad
Коначни резултат се израчунава према утрошку запремине титранта и изражава се у титру (Т) - маса супстанце на 1 мл раствора (г / мл).
Процес образложења
Титриметријска метода квантитативне анализе даје точне резултате, јер супстанце међусобно реагују у еквивалентним количинама. То значи да је производ њиховог волумена и количине идентичан један са другим: Ц 1 В 1 = Ц 2 В 2 . Из ове једначине лако је пронаћи непознату вредност Ц 2 , ако су преостали параметри подешени независно (Ц 1 , В 2 ) и утврђени су током анализе (В 1 ).
Откривање крајње тачке титрације
Будући да је правовремено снимање завршетка титрације најважнији дио анализе, потребно је одабрати праве методе. Употреба индикатора боје или флуоресцентних индикатора сматра се најпогоднијим, али се могу користити и инструменталне методе као што су потенциометрија, амперометрија и фотометрија.
Ad

Коначан избор методе за детекцију ЦТТ зависи од потребне тачности и селективности одређивања, као и од брзине и могућности аутоматизације. Ово посебно важи за мутна и обојена решења, као и за агресивне медије.
Захтеви реакције титрације
Да би титриметријска метода анализе дала исправан резултат, потребно је да одаберете праву реакцију која ће бити у основи. Услови за то су следећи:
- стехиометрија;
- високи проток;
- висока константа равнотеже;
- доступност поуздане методе фиксирања експерименталног краја титрације.
Погодне реакције могу бити било ког типа.
Врсте анализе
Класификација метода титриметријске анализе заснива се на типу реакције. На основу тога се разликују следеће методе титрације:
- киселина-база;
- редок;
- комплексометријски;
- седатив.
Сваки тип се заснива на сопственом типу реакције, одабрани су специфични титранти, у зависности од тога које подгрупе метода су идентификоване у анализи.
Киселинска база
Титриметријска метода анализе која користи реакцију интеракције хидроксонијума са хидроксидним јоном (Х3О + + ОХ - = Х 2 О) назива се кисела база. Ако позната супстанца формира протон у раствору, што је типично за киселине, метода припада ацидиметријској подгрупи. Овде се обично користи стабилна хлороводонична киселина ХЦл као титрант.
Ad
Ако титрант формира хидроксидни јон, метода се назива алкалиметрија. Употребљене супстанце су алкалне, на пример, НаОХ, или соли добијене реакцијом јаке базе са слабом киселином, као што је На2Ц03.
Индикатори који се користе у овој боји. То су слаба органска једињења - киселине и базе, у којима се структура и боја протонираних и непротонираних облика разликују. Најчешће, монокроматски индикатор фенолфталеин (бистар раствор у алкалном средству постаје малина) и двобојна метил-наранџа (црвена супстанца постаје жута у киселом медију) се користе у киселинско-базној титрацији.

Њихова раширена употреба је повезана са високом апсорпцијом светлости, због чега је њихова боја јасно видљива голим оком, и контрастом и уском прелазном зоном боје.
Редокс титрација
Редокс титриметријска анализа је метода квантитативне анализе која се заснива на промени односа концентрација оксидисаних и редукованих облика: аОк 1 + бРед 2 = аРед 1 + бОк 2 .
Метода је подељена на следеће подгрупе:
- перманганатометрија (титрант - КМнО 4 );
- јодометрија (И2);
- дикроматометрија (К2Цр207);
- броматометрија (КБр03);
- јодатометрија (КИО 3 );
- цериметрија (Це (СО4) 2 );
- ванадометрија (НХ4ВО3);
- титанометрија (ТиЦл3);
- хромометрија (ЦрЦл2);
- аскорбометрија (Ц6Х8ОХ).
У неким случајевима, улогу индикатора може одиграти реагенс који учествује у реакцији и мијења боју усвајањем оксидиране или редуковане форме. Али они такође користе специфичне индикаторе, на пример:
- Приликом одређивања јода, користи се скроб који формира тамно плаво једињење са И3-јонима;
- у титрацији фери-гвожђа користе се тиоционатни јони који формирају комплексе са металом, обојене у светло црвеној боји.

Поред тога, постоје посебни редокс индикатори - органска једињења која имају различите боје оксидисаних и редукованих облика.
Комплексометријска титрација
Укратко, титриметријска метода анализе, названа комплексометријска, заснива се на интеракцији две супстанце са формирањем комплекса: М + Л = МЛ. Ако се користе соли са живом, на пример, Хг (НО3) 2 , метода се зове мерцуриметрија, ако је етилендиаминтетраацетатна киселина (ЕДТА) комплексонометрија. Посебно, употребом потоњег метода, користи се титриметријска метода за анализу воде, односно тврдоће.
Ad
У комплексонометрији се користе транспарентни метални индикатори који добијају боју у формирању комплекса са металним јонима. На пример, када се титрирају соли фери-гвожђа са ЕДТА, као индикатор се користи транспарентна сулфосалицилна киселина. Раствара црвену боју када је комплексирана са гвожђем.

Међутим, метални индикатори често имају своју боју, која варира у зависности од концентрације металног јона. Као такви индикатори користе се полибазичне киселине, које формирају прилично стабилне комплексе са металима, који се у исто време брзо погоршавају када су изложени ЕДТА са контрастном дисколорацијом.
Титрација падавина
Титриметријска метода анализе, која се заснива на реакцији интеракције две супстанце са формирањем чврстог једињења које преципитира (М + Кс = МКС ↓), је преципитација. Има ограничену вредност, јер се процеси таложења обично одвијају неквантизовани и нестехиометријски. Али понекад се још увек користи и има две подгрупе. Ако се у методи користе соли сребра, на пример, АгНО 3 , то се назива аргентометрија, ако се ради о живиним солима, Хг 2 (НО 3 ) 2 , затим меркурометрију.
Ad
Да би се одредила крајња тачка титрације коришћењем следећих метода:
- Мохров метод, у коме је индикатор хроматски јон који формира седимент црвене цигле са сребром;
- Фолгардову методу базирану на титрацији раствора јона сребра са калијум тиоцијанатом у присуству фери-гвожђа, који формира црвени комплекс са титрантом у киселој средини;
- Фаиенце метода са титрацијом са показатељима адсорпције;
- Гаи-Луссац метода, у којој се ЦТТ одређује просветљењем или замагљивањем отопине.

Овај последњи метод се у последње време практично не користи.
Методе титрације
Титрација је класификована не само по основној реакцији, већ и методом имплементације. На основу тога се разликују:
- дирецт;
- супротно;
- титрацију супституента.
Први случај се користи само у условима идеалне реакције. Титрант се додаје директно у супстанцу која се детектује. Тако уз помоћ ЕДТА одредите магнезијум, калцијум, бакар, гвожђе и око 25 метала. Али у другим случајевима чешће се користе сложеније методе.
Бацк титратион
Идеална реакција није увек могућа. Најчешће се одвија полако, или је тешко изабрати метод за фиксирање крајње тачке титрације, или се између производа стварају испарљива једињења, због чега се супстанца коју треба одредити делимично губи. Да би се превазишли ови недостаци, можете користити метод обрнуте титрације. Да би се то урадило, велика количина титранта се сипа у супстанцу која се детектује, тако да је реакција завршена, и онда се одређује колико раствор остаје нереагован. За то се остаци титранта из прве реакције (Т1) титрирају другим раствором (Т2), а његова количина се одређује разликом продуката волумена и концентрација у две реакције: С Т1 В Т 1 -Ц Т 2 В Т 2 .
Употреба титриметријске методе анализе у обрнутом смјеру подупире одређивање мангановог диоксида. Његова интеракција са железовим сулфатом је веома спора, тако да се сол узима у сувишку и реакција се убрзава загревањем. Нереагована количина иона гвожђа се титрира са калијум дихроматом.

Титратион Вице
Титрација супституента се користи у случају нестехиометријских или спорих реакција. Његова суштина је да је за аналит изабрана стехиометријска реакција са помоћним једињењем, након чега је производ интеракције подвргнут титрацији.
То је оно што они раде приликом одређивања дикромата. У њу се додаје калијум јодид, што доводи до ослобађања еквивалента јода еквивалентног супстанци која се детектује, која се затим титрира са натријум тиосулфатом.
Према томе, титриметријска анализа омогућава одређивање квантитативног садржаја широког спектра супстанци. Познавајући њихове особине и карактеристике реакција, може се изабрати оптимална метода и метода титрације, која ће дати резултат са високим степеном тачности.