Магнезијум хидроксид: опис супстанце, својстава и употребе
Магнезијум хидроксид је неорганска супстанца, то је слабо растворљиво једињење, које узрокује стварање талога у воденим растворима. Формула магнезијум хидроксида је Мг (ОХ) 2 , то јест, то је дво-киселинска база. Боље растворљив у води него типичне нерастворне базе, али мање растворљив од калцијум хидроксида. Из тог разлога, то се назива слабо растворним једињењима.
Шири се у природи
Магнезијум хидроксид у природи налази се у облику минералног бруцита. Велике наслаге ове пасмине су веома ретке. У Русији се копа на налазишту Кулдур, гдје се његове резерве процјењују на 14 милиона тона. Производња на њој иде брзином од око 250 хиљада тона производа годишње, али се од ове године обим производње удвостручио. Разлог за то је добра потражња за овим минералом у иностранству. Највећи увозник је Јапан.

Изгледа као модри бијели, сиви или зеленкасто-бијели кристали са стакленом искрицом на паузи. Има прилично ниску тврдоћу, тако да је лако сећи ножем. Може да садржи нечистоће. У зависности од њиховог броја и типа, издваја се неколико подврста овог минерала. Тако, ферронемалит садржи, поред магнезијум хидроксида, 5% гвожђа у облику оксида, а ферробрусит - већ чак 36%. Оксид гвожђа има смеђу боју (боја рђе), тако да ови минерали добијају исту нијансу уместо уобичајеног светло зеленог. Ту је и мангобрусит. Нечистоћа је овде манган. Овај минерал има медно-жуту боју. Али, у контакту са кисеоником ваздуха, минерал брзо губи своју лепу боју и брзо поцрни.
Овај минерал се користи углавном као сировина. Производи оксидне и друге магнезијумове спојеве, флуксове и разне ватросталне материјале. Али бруцит се може применити без икакве обраде. Дакле, овај минерал се користи за пречишћавање гасова из хлора и за сорпциону филтрацију воде.
Геттинг
Главна реакција за добијање нерастворљивих хидроксида је реакција интеракције алкалија са магнезијумовим солима. На пример, у интеракцији магнезијум сулфата са натријум хидроксидом. Ово је добра илустрација. И још један пример - у интеракцији магнезијум хлорида и калијум хидроксида.
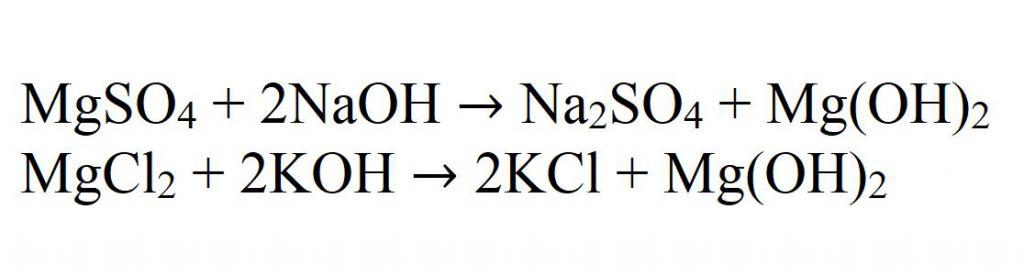
У јонском облику, све такве реакције су написане као:
Мг 2+ + ОХ - → Мг (ОХ) 2
Интеракција магнезијума или његовог оксида са водом такође може произвести хидроксид. Ова реакција је веома спора и само када се загрева.
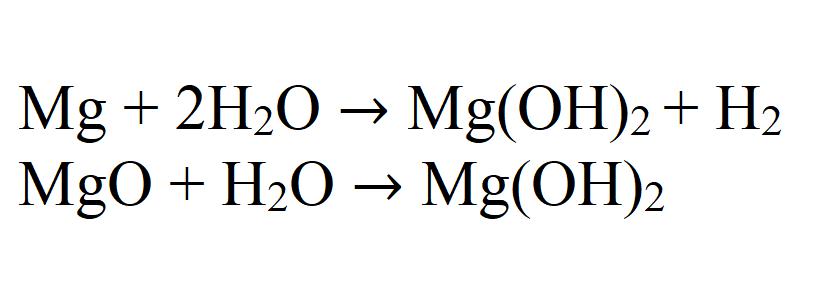
Такав је доста чест минерал - доломит. Са хемијске тачке гледишта, то је мешавина калцијум карбоната и магнезијума. При обради овог минерала са воденим раствором магнезијум хлорида, када се загрева, нерастворљиви хидроксид се таложи:
МгЦО3 · ЦаЦО3 + 2Х2О + МгЦл2 → Мг (ОХ) 2 + ЦаЦл2 + 2ЦО2
Пхисицал пропертиес
У сувом облику, магнезијум хидроксид је бела кристална супстанца. Не мирише, али има алкални укус. Слабо растворљив у води (само 0,6 мг на 100 мл воде). Али чак и упркос томе, његови водени раствори имају слабу алкалну средину и боје индикаторе у одговарајућим бојама. Али ово једињење се раствара у растворима амонијумових соли. Не топи се, јер се на температури од 480 о Ц разграђује на магнезијум оксиду и води, као и свака друга нерастворљива база. Густина под нормалним условима: 2.4 г / цм3.
Хемијска својства
Магнезијум хидроксид је типична нерастворна база. Ово одређује његове хемијске особине. На пример, магнезијум хидроксид реагује са киселинама, киселим оксидима и неметалима:
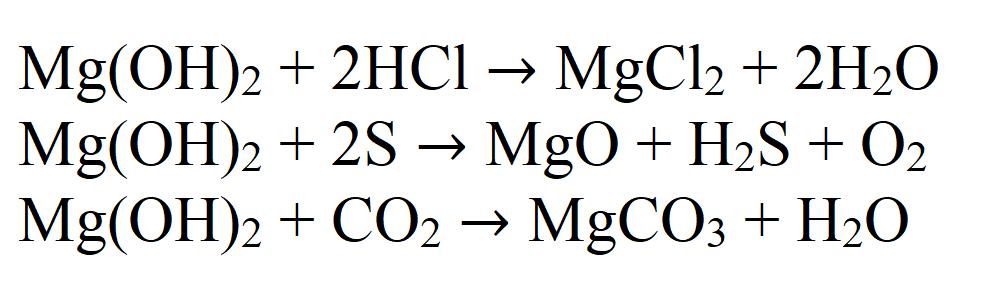
Због ове последње реакције, она тежи да апсорбује угљен диоксид директно из ваздуха да формира карбонат, стога се не препоручује да се ова супстанца држи отвореном дуже време.
Такође је у интеракцији са солима, ако реакција производи талог или гас:
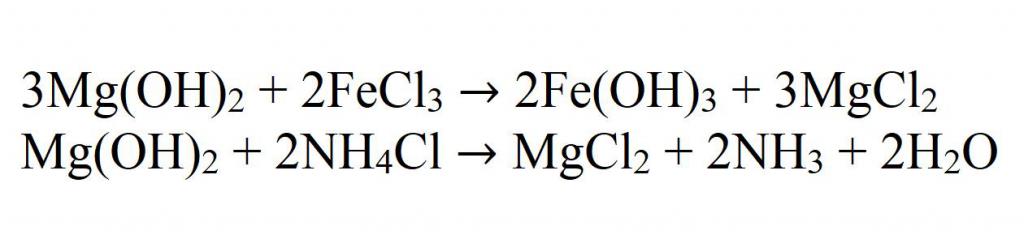
Као што је горе поменуто, када се загрева, магнезијум хидроксид се разлаже према једначини:
Мг (ОХ) 2 → Х 2 О + МгО
Што се тиче формирања комплексних једињења, где би магнезијумов катион деловао као лиганд, постоје супротне информације о овој тачки. Неки извори указују да магнезијум није склон њиховом формирању, а постоје само нестабилна једињења са магнезијум халидима. Други извори указују на то да магнезијум хидроксид може реаговати са врућим алкалијама у облику хидромагнезата:
Мг (ОХ) 2 + 2НаОХ → На2 [Мг (ОХ) 4 ]
Медицинске апликације
У медицини се суспензије на бази магнезијум хидроксида користе као антацид. Ово је олакшано основним својствима. Једном у стомаку, магнезијум хидроксид смањује своју киселост неутрализацијом хлороводоничне киселине. Користи се за гастритис, чир на желуцу и чир на дванаеснику. Лекови на бази не смањују киселинско-базну равнотежу и не нарушавају излучивање хлороводоничне киселине. Али и поред тога, лек има бројна ограничења и контраиндикован је за особе са преосетљивошћу на магнезијум хидроксид.
Продукт интеракције магнезијум хидроксида и хлороводоничне киселине желучаног сока је магнезијум хлорид. То је јак лаксатив (акција се одвија након 2-6 сати). Због тога је магнезијум хидроксид активна компонента неких лекова у овој области. Вишак магнезијума у организму се лако излучује путем бубрега, али ако особа пати од било каквих болести ових органа, онда може добити вишак магнезијума у тијелу када узима лијекове (хипер-магнезија).
Још једна особина овог једињења је опуштање мишића. Понекад се препарати који садрже магнезијум хидроксид преписују женама са претњом побачаја.
Примена у другим индустријама
Магнезијум хидроксид се користи у прехрамбеној индустрији као адитив Е528. У производима регулише киселост и стабилизује боју. Магнезијум хидроксид се такође користи за везивање сумпор-диоксида, чија је појава непожељна у прехрамбеним производима. Користи се у производњи конзервираног поврћа, умака, краставаца и сира. Овај додатак се сматра безопасним, али је забрањен у Аустралији, Великој Британији и Новом Зеланду.
Такође, магнезијум хидроксид се користи као адитив за успоравање пламена у полимерима (ПВЦ, полиолефини), као адитив у детерџентима и зубним пастама, за пречишћавање шећера и третман отпадних вода.
Оксид добијен из магнезијум хидроксида је веома корисно једињење. Може да издржи температуре од око 3000 степени, тако да се користи као ватростални материјал. Дакле, додаје се опекама, од којих се затим праве високе пећи. Користити магнезијум оксид и као сорбент за пречишћавање нафтних производа. Абразивна способност овог једињења је такође висока. Чисти и полира површине делова у електронској индустрији.