Периодични закон хемијских елемената Дмитрија Ивановића Мендељева
Овде ће читалац пронаћи информације о једном од најважнијих закона које је човек икада открио у научној области - периодичном закону Мендељева Дмитрија Ивановића. Упознаћете се са његовом вредношћу и утицајем на хемију, разматрат ће се опште одредбе, карактеристике и детаљи периодичног закона, историја открића и основне одредбе.
Шта је периодични закон?
Периодни закон је природни закон фундаменталне природе, који је први открио ДИ Менделеев 1869. године, а откриће је било резултат поређења својстава одређених хемијских елемената и вредности атомске масе које су биле познате у то време.

Менделејев је тврдио да, према његовом закону, једноставна и комплексна тела и различита једињења елемената зависе од њихове зависности периодичног типа и од тежине њиховог атома.
Периодни закон је јединствен на свој начин и то због чињенице да се он не изражава математичким једнаџбама, за разлику од других основних закона природе и универзума. Графички, свој израз проналази у периодном систему хемијских елемената.
Историја открића
Откриће периодичног закона догодило се 1869. године, али су покушаји систематизације свих познатих елемената Кс почели много прије тога.
Први покушај да се створи такав систем предузела је И. В. Дебереинер 1829. године. Он је све хемијске елементе који су му познати класификовао у трију једни других повезаних близином половине суме атомских маса које припадају овој групи од три компоненте. Након Дебереинер-а, направљен је покушај да се створи јединствена табела класификације елемената А. де Цханцоуртоиса, његов систем је назвао "земљаном спиралом", а након што је компоновао октаву Невландса од стране Јохна Невландса. Године 1864, скоро истовремено, Виллиам Алдинг и Лотхар Меиер објавили су табеле креиране независно једна од друге.

Периодични закон је представљен научној заједници 8. марта 1869. године, а то се десило током састанка руског друштва. Менделејев Дмитриј Ивановић, за све, најавио је своје откриће, а исте године Мендељејев уџбеник “Основи хемије” је објављен, гдје је први пут приказан периодни систем који је он креирао. Годину дана касније, 1870. године, написао је чланак и ставио га на изложбу у РЦВ, гдје је први пут кориштен концепт периодичног закона. Године 1871. Мендељев је дао исцрпан опис свог з-ина у чувеном чланку о периодичном легитимитету хемијских елемената.

Непроцјењив допринос развоју хемије
Значај периодичног закона је невероватно велик за научну заједницу у целом свету. То је због чињенице да је његово откриће дало снажан потицај развоју и хемије и других природне науке, на пример, физика и биологија. Повезаност елемената са њиховим квалитативним хемијским и физичким карактеристикама је била отворена, она је такође омогућила разумевање суштине конструкције свих елемената по једном принципу и довела до модерне формулације појмова о хемијским елементима, конкретизацији знања о концепту супстанци сложене и једноставне структуре.
Употреба периодичног закона омогућила је решавање проблема хемијског предвиђања, како би се утврдио узрок понашања познатих хемијских елемената. Атомска физика, укључујући и нуклеарну енергију, постала је могућа због истог закона. Заузврат, подаци науке омогућили су да се прошире хоризонти суштине овог закона и да се дубље упознају са његовим разумевањем.
Хемијска својства елемената периодног система
У суштини, хемијски елементи су међусобно повезани карактеристикама својственим њима у слободном стању и атома и јона, солватираних или хидрираних, у једноставној супстанци и форми коју могу формирати њихова бројна једињења. Међутим, својства к-цуе обично се састоје од двије појаве: својстава карактеристичних за атом у слободном стању и једноставне супстанце. Многе врсте својстава припадају овој врсти својстава, али најважније су:
- Атомска јонизација и њена енергија, у зависности од позиције елемента у табели, његов редни број.
- Енергетски однос између атома и електрона, који, као и атомска јонизација, зависи од локације елемента у периодном систему.
- Електронегативност атома, не носи константну вредност, али се може мењати у зависности од различитих фактора.
- Радијуси атома и јона - овде се, по правилу, користе емпиријски подаци, који су повезани са таласном природом електрона у стању кретања.
- Атомизација једноставних супстанци - опис реактивности елемента.
- Степен оксидације је формална карактеристика, али се појављује као једна од најважнијих карактеристика елемента.
- Оксидациони потенцијал за једноставне супстанце је мерење и индикација потенцијала неке супстанце за њено деловање у воденим растворима, као и ниво испољавања својстава редокс природе.
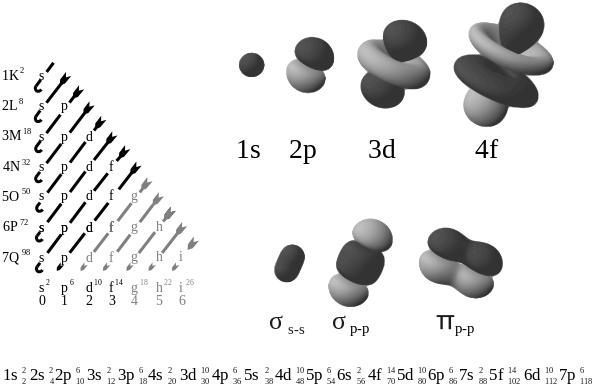
Учесталост елемената интерног и секундарног типа
Периодни закон даје разумевање друге важне композитне честице природе - унутрашње и секундарне периодичности. Горе наведене области проучавања атомских својстава су, у ствари, много теже него што мислите. Разлог за то је што елементи ел. На пример, унутрашњи процес преласка елемента с из прве групе на осми на п-елемент праћен је тачкама минимума и максимума на кривој енергије јонизованог атома. Овај феномен показује унутрашњу несталност периодичности промена својстава атома у складу са њеним положајем у периоду.
Резултати
Читач сада јасно разуме и дефинише шта је Мендељејев периодични закон, схвата његову важност за човека и развој различитих наука, и има идеју о својим тренутним позицијама и историји открића.