Квантно-механички модел атома и његове структуре
Планетарни квантно-механички модел Боровог атома често се памти по својој уредној и познатој слици електрона. Окрећу се око централног језгра, као планете око Сунца. Због тога је тешко заменити слику оне која тачније представља квантно-механички модел атома који користе савремени физичари.
Како се атом креће и креће?
Атом има мали језгро и таласе оштрих орбита. Локација и кретање електрона описани су таласима њихове материје. Ове структуре предвиђају могућност проналажења електрона у датом подручју атома. Али одакле је дошао квантно-механички модел Боровог атома?
Планетарни модел иницирао је процес увођења квантне теорије у структуру атома. Бохр је увео идеју о стационарним стањима у којима је атом био стабилан. Транзиције између ових стања објашњавају постојање спектралних линија. У случају водоника, он је био у стању да добије нивое енергије:
Ad
- Прелази између нивоа енергије одговарају линијама у спектру водоника.
- Његов модел није могао да предвиди нивое енергије за било које друге атоме (иако би се нивои алкалних метала попут водоника могли приближити истини).
Одвојено, рад Хајзенберга и Шредингера је изведен како би се изнашли начини да се потпуније опишу квантизовани нивои енергије атома.
Аналогије Хеисенберга и Шредингера: како су водиле једнаџбу у доказ валова
Квантно-механички модел структуре атома има јединствен скуп својстава. Хајзенберг је користио матрице, а Шредингер је развио таласну једначину да би доказао апсолутност разлике у понашању кванта. Дуалност честица је детаљније приказана у видеу.
Ad

Шредингерове једначине дају приказ густине вероватноће електрона око нуклеуса атома. Већина дефиниција квантне теорије и квантне механике нуди исти опис за оба. Они суштински описују квантну теорију, у којој и енергија и материја имају карактеристике таласа у неким условима и карактеристике честица у другима.
Да би идеја била јаснија, људи су почели да воде експерименте у смислу менталног обећања.

- Квантна теорија сугерише да енергија долази у дискретним пакетима који се називају кванти (или, у случају електромагнетног зрачења, фотони).
- Квантна теорија има неки математички развој, често назван квантна механика, који нуди објашњења за понашање електрона у електронским облацима атома.
Главне одредбе квантно-механичког модела структуре атома је дуалност електронских таласа у електронском облаку, што ограничава нашу способност да истовремено меримо енергију и положај електрона.
Скривене особине електрона
Што прецизније измеримо енергију или положај електрона, мање знамо о другом. Не можемо тачно да означимо положај и момент електрона у исто време. Због тога је немогуће предвидети путању честице. Сходно томе, понашање електрона описано је другачије него понашање честица нормалне величине. Треба да знате:
- Најчешћи начин за описивање електрона у атомима у складу са квантном механиком је решавање Сцхродингер-ове једначине за енергетска стања електрона у овом облаку.
- Када је електрон у тим стањима, његова енергија је јасно дефинисана, а позиција није.
- Положај је описан мапом дистрибуције вјероватноће, названом орбитална.
Трајекторију коју обично повезујемо са макроскопским објектима замењују електрони у облацима електрона, а статистички описи не указују на путању, већ на област у којој се налази. Пошто електрон у атомском електронском облаку одређује његово хемијско понашање, да би разумио хемију, неопходно је описати конфигурацију електрона у кључу квантно-механичког модела атома.
Хеисенбергов принцип неизвесности: подручје унутар атома
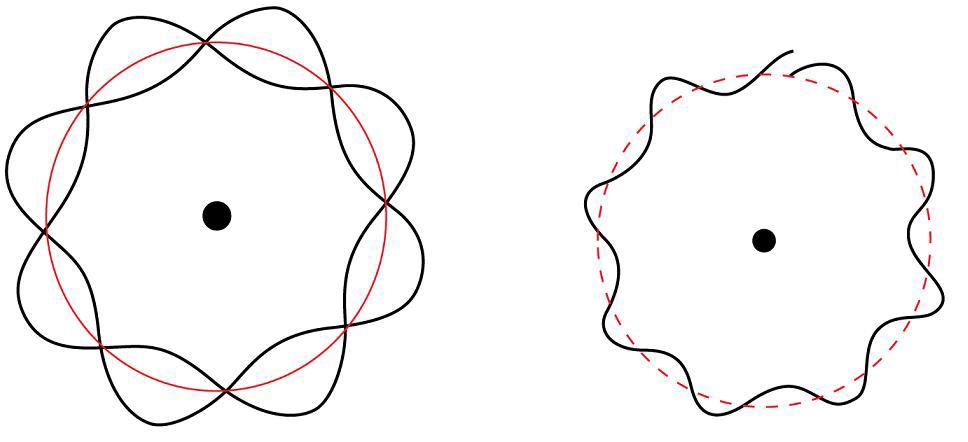
Лоуис де Броглие је предложио да се све честице могу сматрати материјалним валовима са таласном дужином - ламбда, дефинисане следећом једначином:
Ламбда = стварно време (сат) + миливолт сат
Ервин Сцхродингер је предложио квантно-механички модел атома. Укратко: електроне третира као таласе материје.
Квадрат функције вала представља вероватноћу проналажења електрона у датом региону унутар атома. Атомска орбита је дефинисана као регион унутар атома, где је електрон.
Хеисенбергов принцип несигурности каже да не можемо знати ни енергију ни положај електрона. Стога, када сазнамо више о положају електрона, мање знамо о његовој енергији, и обрнуто. Електрони имају својствено својство звану спин. Свака два електрона који заузимају исту орбиту морају имати супротне спинове.
Ad
Луминифероус етер у квантном свету
Природа светлости је предмет истраживања од антике. У седамнаестом веку, Исак Њутн је водио експерименте са сочивима и призмама. Он је био у стању да покаже да се бела светлост састоји од појединачних боја дуге, комбинованих заједно. Њутн је објаснио резултате своје оптике са "корпускуларним" приказом светлости, у којој се светлост састојала од токова екстремно малих честица које се крећу великом брзином у складу са Њутновим законима кретања. Вриједи напоменути:
Цхристиан Хуигенс је показао да оптички феномени као што су рефлексија и рефракција могу бити једнако добро објашњени са тачке гледишта светлости као таласи који се крећу великом брзином кроз медиј назван "светлећи етар". Прожима цео простор.
Ad
На почетку деветнаестог века, Тхомас Иоунг је показао да светлост која пролази кроз уске, блиско размакнуте прорезе ствара интерференцијске обрасце који се не могу објаснити са становишта Невтонових честица, али се могу лако интерпретирати са становишта таласа.
- Касније, у деветнаестом веку, након што је Џејмс Кларк Максвел развио своју теорију електромагнетног зрачења и показао да је светлост видљив део огромног спектра електромагнетних таласа, поглед на честицу светлости постао је потпуно дискредитован.
Данас се ове области називају класична механика и класична електродинамика (или класични електромагнетизам).
Како је напредовала идеја увођења нових концепата у физици

До краја деветнаестог века, научници су видели да је физички универзум приближно састављен од две одвојене области:
- материја формирана од честица које се крећу према Невтоновим законима кретања;
- електромагнетно зрачење које се састоји од таласа који се контролишу Маквелловом једначином.
Парадокси су довели до модерне структуре квантно-механичког модела Сцхродингер-овог атома, који блиско повезује честице и таласе на фундаменталном нивоу, назван двојност таласне честице, која је заменила класични поглед.
Дискретни Боров вал: како се понашају емисиони спектри водоника
Према Бохровом моделу, емисиони спектри различитих елемената садрже дискретне линије. Видљива област емисионог спектра водоника може бити представљена коришћењем табеле.
Ad
| Основни квантни број | Број поднивоа | Број електрона |
| 1 | 1 | 2 |
| 2 | 2 | 8 |
| 3 | 3 | 18 |
| 4 | 4 | 32 |
Ово је схематски приказ кванта, где је познат број електрона и нивоа. У животу у вакуумским условима немогуће је са сигурношћу рећи да постоји ограничење на под-нивоима, али не може бити више од 7. Квантизовани емисиони спектри указују да Борови могу постојати унутар атома само на одређеним атомским радијусима и енергијама.

Конструишући модел, Бохр је извео једнаџбу која је исправно предвидела различите нивое енергије у атому водоника. Квантно-механички модел је био погодан само за представљање овог конкретног случаја. Нивои су одговарали емисијским линијама у спектру супстанце.
Бохров модел, који је доказао једноелектронски водиков систем
Брзина електрона на енергетском нивоу основног стања водоника је 2,2 × 10 6 с ÷ м, при чему је с дужина, м је маса. Можемо заменити константу, као и масу и брзину електрона у де Броглијеву једначину. Али у исто време, није могао да објасни електронску структуру у атомима који садрже више од једног електрона.
Ако се окренемо хемији, квантно-механички модел атома водоника треба да се састоји само од протона. Када се састају са електронима или неутронима, честица почиње да се понаша као талас. У другим случајевима, атоми друге супстанце могу се, без обзира на структуру, понашати као таласи или честице. Укратко, квантно-механички модел атома водоника је материјални дуализам вала, али не и честица.
Преклапање таласа један на други: како се путање пресека атома не мијеша
Радио таласи са мобилног телефона, рендгенске снимке које користе стоматолози, енергија која се користи за кување у вашој микроталасној пећници, топлотно зрачење из врелих објеката и светло са ТВ екрана су сви облици електромагнетног зрачења који показују таласасто понашање. Потребно је запамтити:
- Талас је осцилација или периодично кретање које може преносити енергију из једне тачке простора у другу.
- Дрмање краја ужета преноси енергију из ваше руке на други крај ужета; шљунак који пада у рибњак доводи до ширења таласа дуж површине воде; експанзија ваздуха која прати муњу генерише звучне таласе (громове) који могу да путују неколико миља.
- У сваком од ових случајева, кинетичка енергија се преноси кроз супстанцу (конопац, воду или ваздух), док супстанца остаје на месту.
Валови не би требали бити ограничени на путовање кроз материју. Као што је Маквелл показао, електромагнетни таласи се састоје од електричног поља, осцилујућег у времену са окомитим магнетним пољем. Они су окомити на правац кретања. Ови таласи могу да прођу кроз вакуум при константној брзини од 2.998 × 108 м / с, где је ц брзина светлости.