Сумпор диоксид - физичка својства, припрема и употреба
Сумпор диоксид има молекуларну структуру сличну озону. Атом сумпора који се налази у центру молекула везан је за два атома кисеоника. Овај гасовити производ оксидације сумпора нема боју, производи јак мирис, а када се услови промене лако се кондензује у бистру течност. Супстанца је добро растворљива у води, има антисептичка својства. СО2 се производи у великим количинама у хемијској индустрији, односно у циклусу производње сумпорне киселине. Гас се широко користи за прераду пољопривредних и прехрамбених производа, бељење тканина у текстилној индустрији.
Систематска и тривијална имена супстанци
Потребно је разумети разноврсност термина који се односе на исто једињење. Званично име једињења, чији хемијски састав одражава формулу СО 2 , је сумпор диоксид. ИУПАЦ препоручује употребу овог термина и његовог енглеског еквивалента - Сумпор диоксид. Уџбеници за школе и факултете чешће спомињу такав назив - сумпор оксид (ИВ). Римски број у заградама означава валенцију атома С. Кисик у овом оксиду је бивалентан, а оксидативни број сумпора је +4. Техничка литература користи тако застареле термине као сумпор диоксид, анхидрид сумпорне киселине (производ његове дехидрације).
Ad
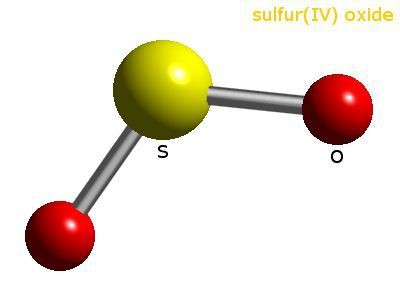
Састав и молекуларна структура СО2
Молекул СО2 је формиран од једног атома сумпора и два атома кисеоника. Између ковалентних веза постоји угао од 120 °. Сп2 хибридизација се јавља у атому сумпора - они су поравнати у форми и енергији облака од једног с и два п-електрона. Они су укључени у образовање. ковалентна веза између сумпора и кисеоника. У О - С пару, удаљеност између атома је 0.143 нм. Кисеоник је електронегативнији елемент од сумпора, што значи да се везни парови електрона померају од центра ка спољашњим угловима. Читав молекул је такође поларизован, негативни пол је О атом, позитиван је С атом.
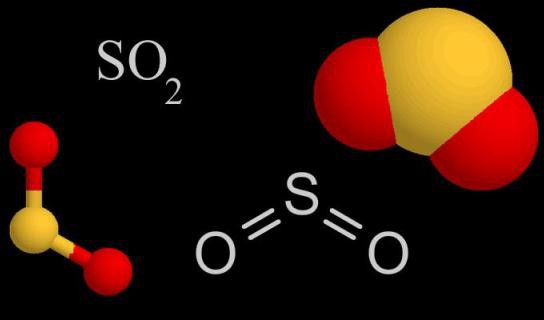
Неки физички параметри сумпор диоксида
Оксид тетравалентног сумпора у нормалним условима околине чува гасовито агрегатно стање. Формула сумпор-диоксида омогућава одређивање њене релативне молекуларне и моларне масе: Мр (СО2) = 64.066, М = 64.066 г / мол (може се заокружити на 64 г / мол). Овај гас је скоро 2,3 пута тежи од ваздуха (М (ваздух) = 29 г / мол). Диоксид има оштар, специфичан мирис горућег сумпора, који је тешко збунити са било којим другим. Неугодно је, иритира слузокожу очију, изазива кашаљ. Међутим, оксид сумпора (ИВ) није толико токсичан као што је сумпороводик.
Ad
Под притиском на собној температури, гасовити сумпор диоксид се раствара. На ниским температурама, супстанца је у чврстом стању, топи се на -72 ... –75,5 ° Ц. Са даљим повећањем температуре, појављује се течност, и на -10.1 ° Ц, гас се поново формира. Молекули СО2 су термички стабилни, распад у атомски сумпор и молекуларни кисеоник се јављају на веома високим температурама (око 2800 ºС).

Растворљивост и интеракција са водом
Сумпор диоксид, када се раствори у води, делимично реагује са њом да би формирао веома слабу сумпорну киселину. У тренутку његовог добијања, одмах се разлаже на анхидрид и воду: СО2 + Х20О2Х2С03. У ствари, решење није присутно сумпорна киселина и хидрирани молекули СО2. Гасовити диоксид боље реагује са хладном водом, а његова растворљивост опада са повећањем температуре. Под нормалним условима, може се растворити у 1 запремини воде до 40 запремина гаса.
Ad
Сумпор диоксид у природи
Значајне количине сумпор диоксида се ослобађају вулканским гасовима и лавом током ерупција. Многе врсте антропогених активности такође доводе до повећања концентрације СО 2 у атмосфери.

Сумпорни анхидрид се доводи у ваздух металуршким постројењима, где испушни гасови нису заробљени током печења руде. Многе врсте фосилних горива садрже сумпор, због чега се значајне количине сумпор диоксида испуштају у атмосферски ваздух када се сагоревају угаљ, нафта и гас. Сумпор диоксид постаје токсичан за људе при концентрацијама у ваздуху које прелазе 0,03%. Код особе почиње кратак дах, могу се појавити симптоми као што су бронхитис и упала плућа. Веома високе концентрације сумпор диоксида у атмосфери могу довести до озбиљног тровања или смрти.
Сумпор диоксид - производња у лабораторији иу индустрији
Лабораторијске методе:
- Када се сумпор сагорева у посуди са кисеоником или ваздухом, добија се диоксид по формули: С + О2 = СО2.
- Могуће је дјеловати на соли сумпорне киселине с јачим неорганским киселинама, боље је узети солну киселину, али је могуће разриједити сумпорну киселину:
- На2С03 + 2ХЦл = 2НаЦл + Х2С03;
- На2С03 + Х2С04 (д) = На2С04 + Х2С03;
- Х2С03 = Х20 + СО2.
3 Када бакар реагује са концентрованом сумпорном киселином, не ослобађа се водоник, већ сумпор диоксид:
2Х2С04 (конц.) + Цу = ЦуС04 + 2Х2О + СО2.
Савремене методе индустријске производње сумпор диоксида:
- Оксидација природног сумпора при сагоревању у посебним пећима: С + О 2 = СО 2 .
- Паљење гвожђа пирит (пирит).
Основна хемијска својства сумпор диоксида
Сумпор диоксид је активна супстанца хемијски. У редокс процесима, ова супстанца често делује као редукциони агенс. На пример, у интеракцији молекулског брома са сумпор диоксидом, реакциони производи су сумпорна киселина и бромоводоник. Оксидативна својства СО2 се појављују када се овај гас пропушта кроз водоник сулфидну воду. Као резултат, ослобађа се сумпор, јавља се само-оксидација-само-редукција: СО2 + 2Х2С = 3С + 2Х2О.
Сумпор диоксид показује киселинска својства. Одговара једној од најслабијих и најнестабилнијих киселина - сумпорној. Ово једињење не постоји у свом чистом облику, могуће је детектовати киселинске особине раствора сумпор-диоксида помоћу индикатора (лакмус је ружичаст). Сумпорна киселина даје просечне соли - сулфите и киселине - хидросулфите. Међу њима су стабилна једињења.
Ad
Процес оксидације сумпора у диоксиду до хексавалентног анхидрида сумпорне киселине је каталитички. Добијена супстанца је снажно растворена у води, реагује са молекулима Х 2 О. Реакција је егзотермна, формира се сумпорна киселина, односно хидратизована форма.
Практична употреба сумпор диоксида
Главни метод индустријске производње сумпорне киселине, који захтева елемент диоксид, има четири фазе:
- Добијање сумпор диоксида сагоревањем сумпора у посебним пећима.
- Пречишћавање добијеног сумпор диоксида из свих врста нечистоћа.
- Даља оксидација до шествалентног сумпора у присуству катализатора.
- Апсорпција сумпор триоксида водом.
Раније је скоро сав сумпорни диоксид потребан за производњу сумпорне киселине у индустријским размерама добијен печењем пирита као нуспроизвода производње челика. Нове врсте прераде металуршких сировина мање користе сагоревање руде. Стога је последњих година природни сумпор постао главни извор за производњу сумпорне киселине. Значајне глобалне резерве ове сировине, њихова доступност нам омогућава да организујемо велике прераде.
Ad

Сумпор диоксид се широко користи не само у хемијској индустрији, већ иу другим индустрије. Текстилне млинице користе ову супстанцу и продукте њене хемијске интеракције за бељење свиле и вунене тканине. Ово је једна од врста избељивања без хлора, у којој влакна нису уништена.
Сумпор диоксид има одлична дезинфекциона својства, која се користе у борби против гљивица и бактерија. Сумпорни анхидрид се фумигује складиштењем пољопривредних производа, винских бачава и подрума. Користи се СО2 у прехрамбеној индустрији као конзерванс и антибактеријска супстанца. Додајте га сирупима, упијте свеже воће. Сулфитизатион
Сок од шећерне репе промени боју и дезинфикује сировине. Конзервирани пиреи од поврћа и сокови садрже и сумпор диоксид као антиоксидант и конзерванс.
