Ковалентна веза: концепт, знаци, хемијско значење
Важна врста везе између атома
Ковалентна веза заједно са ионским је главни тип хемијска веза. Она карактерише способност атома да међусобно комуницирају и стварају густе љуске на електронском нивоу које служе као основа за молекуле са потпуно новим својствима.
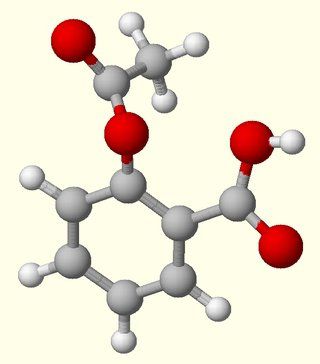
Појам и хемијско значење ове врсте хемијске везе
Према правилу, ковалентна веза је веома честа по природи. врста хемијске везе на којој се врши сједињавање електрона атома, што резултира формирањем заједничке молекуларне орбиталне Ова новоформирана љуска дозвољава атомима да доведу број својих електрона до броја који њихова вањска орбита може примити. Као резултат, молекул стиче стабилност и стабилност.
Ad

Кључне карактеристике и својства
Израз "ковалентна веза" означава жељу атома да ступају у интеракцију са другим атомима, њихову способност да формирају стабилно једињење. Таква веза се може јавити како између идентичних атома (на пример, водоника или хлора), тако и између различитих атома (на пример, у молекулима сумпороводика, хлороводонична киселина). У првом случају, формира се специфичан електронски облак, чије елементарне честице, смјештене на вањским орбиталима, почињу служити обје језгре, не обраћајући пажњу на то да ли су „своје“ или „ванземаљци“.
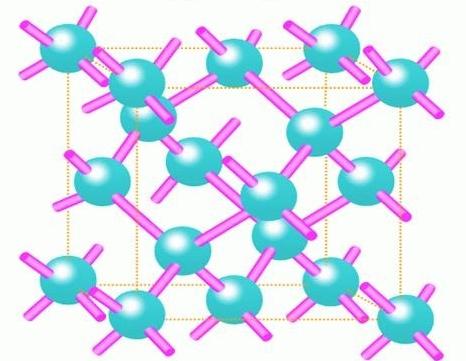
Тежња ка смањењу трошкова енергије
Главни разлог због којег атоми теже да добију нестали електрон у своју спољашњу љуску је њихова жеља да смање трошкове енергије. Уосталом, одавно је познато да је укупна енергија једног молекула истог водоника много нижа од суме енергија два атома истог елемента. Дакле, ковалентна веза је природна реакција материје на жељу да се значајно смањи трошак ресурса за његово постојање.
Ad
Још једна велика последица
У формирању и даљем постојању ових једињења постоји још једна важна регуларност. Чињеница је да је ковалентна веза заснована на одређеним удаљеностима између атома у молекулу. Оне не могу бити мање од одређене вриједности, јер ће у противном систем изгубити стабилност, а његова енергија ће се убрзано повећавати. Ова имовина се активно користи у разним секторима националне економије, на пример, у нуклеарној индустрији.
Славна владавина Левиса
Ковалентна веза, чија се својства тренутно проучавају, функционише на основу чувеног правила октет-дублет, које је у то време формулисао познати хемичар Лајс. Према његовом концепту, формирање ове врсте везе захтева такав број електрона да спољашње љуске атома постану комплетне, као што је структура инертних гасова. На пример, у молекули водоника његови саставни елементи личе на хелијум, ау молекулу хлора аргон.