Алдехиди и кетони. Формула, припрема, апликација
Међу органским једињењима који садрже кисеоник од изузетне су важности две класе супстанци, које се увек проучавају заједно због сличности у структури и манифестованих својстава. То су алдехиди и кетони. Управо ови молекули су основа многих хемијских синтеза, а њихова структура је довољно интересантна да се проучи. Размотримо детаљније шта су ове класе једињења.

Алдехиди и кетони: опште карактеристике
Са становишта хемије, класа алдехида треба да садржи органске молекуле који садрже кисеоник у функционалној групи -СОН, названој карбонил. Општа формула у овом случају ће изгледати овако: Р-ЦОХ. По својој природи, то могу бити ограничавајућа и незасићена једињења. Међу њима су и ароматични представници, заједно са алифатичним. Број атома угљеника у радикалном ланцу варира у прилично широким границама, од једног (формалдехид или метан) до неколико десетина.
Ad
Кетони такође садрже карбонилну групу -ЦО, али она није повезана са катионом водоника, већ са другим радикалом који је различит или идентичан ономе што улази у ланац. Општа формула је следећа: Р-ЦО-Р ,. Очигледно је да су алдехиди и кетони слични у присуству функционалне групе ове композиције.
Кетони такође могу бити ограничавајући и незасићени, а испољена својства су слична блиско сродној класи. Постоји неколико примера који илуструју састав молекула и одражавају прихваћене ознаке формула разматраних супстанци.
- Алдехиди: метанал-ХЦл, бутанал-ЦХ3-ЦХ2-ЦХ2-ЦОХ, фенилацетиц - Ц6Х5-ЦХ2-ЦОХ.
- Кетони: ацетон или диметил кетон - ЦХ3-ЦО-ЦХ3, метил етил кетон - ЦХ3-ЦО-Ц2Х5 и други.
Очигледно је да се име ових једињења формира на два начина:
Ad
- према рационалној номенклатури према радикалима и класи суфикса -ал (за алдехиде) и -он (за кетоне);
- тривијално, историјски.
Ако дате општу формулу за обе класе супстанци, постаће јасно да су они изомери једни од других: Ц н Х 2н О. За себе су карактеристични следећи типови изомерије:
- за кетоне, структуру угљоводоничног ланца радикала и положај -ЦО групе;
- за алдехиде - само распоред атома у ланцу.

Да би се разликовали представници оба разреда, користити квалитативне реакције већина нам омогућава да идентификујемо алдехид. Пошто је хемијска активност ових супстанци нешто већа, због присуства водоник катиона.
Молекуларна структура
Размотрите како алдехиди и кетони изгледају у свемиру. Структура њихових молекула може се одразити у неколико тачака.
- Атом угљеника директно укључен у функционалну групу има сп2 хибридизацију, која омогућава да део молекула има раван просторни облик.
- У овом случају, поларитет везе Ц = О је јак. Што је више електронегативан, кисеоник узима већину своје густине, концентришући делимично негативни набој на себе.
- У алдехидима, ОХ веза је такође високо поларизована, што чини атом водоника мобилним.
Као резултат, испоставило се да таква структура молекула омогућава да се предметна једињења оксидирају и редукују. Формула алдехида и кетона са редистрибуираном електронском густоћом омогућава предвиђање продуката реакције у којима ове супстанце учествују.
Ad
Историја открића и проучавања
Као многи органска једињења тек у 19. стољећу људи су успјели изолирати и проучавати алдехиде и кетоне, када су се виталистички погледи потпуно срушили и постало је јасно да се ова једињења могу формирати синтетичким, умјетним средствима, без судјеловања живих бића.
Међутим, 1661. Р. Боиле је успео да добије ацетон (диметил кетон), када је калцијум ацетат подвргнуо загревању. Али није могао детаљно проучити ову супстанцу и именовати је, одредити систематску позицију међу осталима. Тек 1852. године Виллиамсон је могао да приведе крају ову ствар, а онда је почела историја детаљног развоја и акумулације знања о карбонилним једињењима.

Пхисицал пропертиес
Размотрите физичке особине алдехида и кетона. Почнимо од првог.
- Према стању агрегације, први представник је метан, следећих једанаест су течности, више од 12 атома угљеника је део чврстих алдехида нормалне структуре.
- Тачка кључања: зависи од броја Ц-атома, што су више, то је већа. Штавише, што је ланац разгранати, то је нижа температура.
- За течне алдехиде, индекси вискозности, густине и рефракције такође зависе од броја атома. Што их је више, тако су и више.
- Гасовити и течни алдехиди се добро растварају у води, али то практично не може да учини.
- Мирис представника је веома пријатан, често су то мириси цвећа, парфема, воћа. Само они алдехиди у којима је број атома угљеника 1-5 су снажно и неугодно мирисне течности.
Ако одредите својства кетона, можете одабрати и оне главне.
Ad
- Агрегатна стања: нижи представници су течности, масовнији су чврста једињења.
- Мирис је оштар, неугодан за све представнике.
- Растворљивост у води је добра за ниже, одлична је за све у органским растварачима.
- Хлапљиве супстанце, овај индикатор превазилази концентрације киселина, алкохола.
- Тачка кључања и тачка топљења зависе од структуре молекула, веома варирају од броја угљеникових атома у ланцу.
То су главна својства разматраних једињења, која припадају групи физичких.
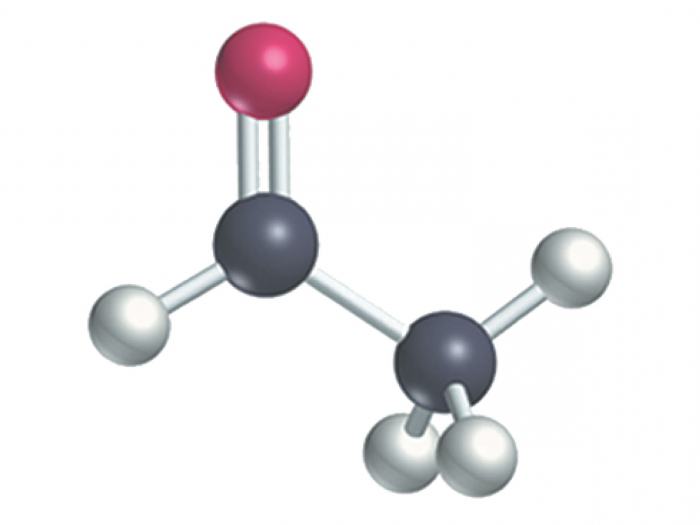
Хемијска својства
Најважније је шта алдехиди и кетони реагују са хемијским својствима ових једињења. Стога их сматрамо нужно. Прво, бавите се алдехидима.
- Оксидација у одговарајуће карбоксилне киселине. Општи преглед једначине реакције: Р-ЦОХ + [О] = Р-ЦООХ. Ароматични представници још лакше улазе у такве интеракције, а такође су у стању да формирају естере индустријске важности. Као оксиданти користе се: кисеоник, Толленс реагенс, бакар (ИИ) хидроксид и други.
- Алдехиди се манифестују као јаки редукциони агенси, док се претварају у ограничавајући монохидрични алкохоли.
- Интеракција са алкохолима у облику продуката ацетала и хемиацетала.
- Посебне реакције - поликондензација. Као резултат, формирају се фенолформалдехидне смоле које су важне за хемијску индустрију.
- Неколико специфичних реакција са следећим реагенсима:
- водено-алкохолни алкали;
- Григнард реагенс;
- хидросулфити и други.
Квалитативна реакција на ову класу супстанци је реакција "сребрног огледала". Као резултат, формира метално редуковано сребро и одговарајућу карбоксилну киселину. Захтева раствор амонијака од оксида сребра или реагенса Толлинс.
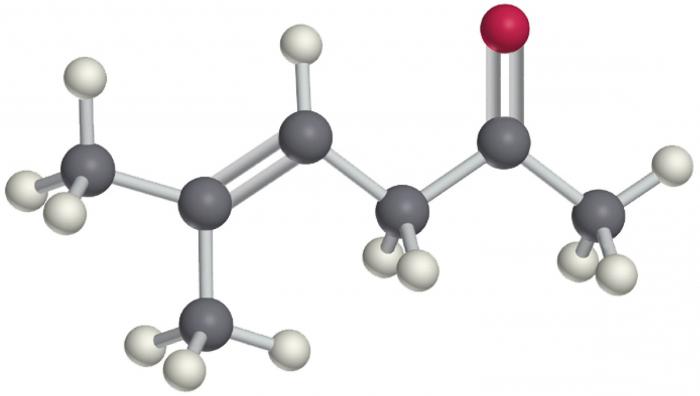
Хемијска својства кетона
Алкохоли, алдехиди, кетони су слични по својим својствима једињења, пошто сви они садрже кисеоник. Међутим, већ у фази оксидације постаје јасно да су алкохоли најактивнија и лако осетљива једињења. Кетони су најтеже оксидовати.
Ad
- Оксидирајућа својства. Као резултат, формирају се секундарни алкохоли.
- Хидрогенација такође доводи до горе наведених производа.
- Кето-енолни таутомеризам је специфично специфично својство кетона да узима бета облик.
- Реакције алдолне кондензације са формирањем бета-кетоспиртова.
- Такође, кетони могу да комуницирају са:
- амонијак;
- хидроцианична киселина ;
- хидросулфите;
- хидразин;
- ортосиликатна киселина.
Очигледно, реакције таквих интеракција су веома сложене, посебно оне које су специфичне. То су све главне карактеристике које алдехиди и кетони показују. Хемијске особине су основа многих синтеза важних једињења. Зато је познавање природе молекула и њиховог карактера током интеракција изузетно неопходно у индустријским процесима.
Реакције адхезије алдехида и кетона
Већ смо прегледали ове реакције, али им нисмо дали такво име. Све интеракције могу се приписати додавању, као резултат тога карбонилна група је показала активност. Или боље речено, покретни атом водоника. Због тога су овом питању приоритет алдехиди, због њихове боље реактивности.
Које супстанце су могуће реакције алдехида и кетона за нуклеофилну супституцију? Ово је:
- Хидроцианична киселина, цијанхидрин се формира - сировина у синтези аминокиселина.
- Амонијак, амини.
- Алкохоли.
- Вода
- Натријум хидросулфат.
- Григнард реагенс.
- Тиоли и други.
Ове реакције су од великог индустријског значаја, јер се производи користе у различитим областима људске активности.

Начини да дођете
Постоји неколико основних метода којима се синтетишу алдехиди и кетони. Добијање у лабораторији и индустрији може се изразити на следеће начине.
- Најчешћи метод, укључујући у лабораторијама, је оксидација одговарајућих алкохола: примарно у алдехиде, секундарне у односу на кетоне. Хромати, јони бакра, калијум перманганат могу да делују као оксидациони агенс. Општи преглед реакције: Р-ОХ + Цу (КМнО4) = Р-ЦОХ.
- У индустрији се често користи метода базирана на оксидацији алкена - оксосинтеза. Главни агенс је синтетски гас, смеша ЦО 2 + Х2. Резултат је алдехид са великим бројем атома по ланцу угљеника. Р = РР + ЦО2 + Х2 = РРР-ЦОХ.
- Оксидација алкена озоном - озонолиза. Резултат такође указује на алдехид, али осим тога, кетон је такође у смеши. Ако су производи ментално повезани, уклањају кисеоник, постаје јасно шта је оригинални алкен узет.
- Куцхеровска реакција - хидратација алкина. Обавезни агенс - живе соли. Једна од индустријских метода за синтезу алдехида и кетона. Р2РР + Хг2 + + Х20 = РР-ЦОХ.
- Хидролиза дихалогенских деривата угљоводоника.
- Редукција карбоксилних киселина, амида, нитрила, киселинских хлорида, естара. Као резултат, формирају се и алдехид и кетон.
- Пиролиза смеша карбоксилних киселина преко катализатора металних оксида. Мешавину треба испарити. Доња линија је елиминација између молекула угљен диоксида и воде. Резултат је алдехид или кетон.
Ароматски алдехиди и кетони се припремају на други начин, пошто ова једињења имају ароматски радикал (фенил, на пример).
- Према Фриедел-Црафтс-у: у почетним реагенсима постоји ароматски угљоводоник и дихалоген супституисани кетон. Катализатор - АЛЦЛ 3 . Резултат је ароматски алдехид или кетон. Друго име за процес је ацилација.
- Оксидација толуена различитим агенсима.
- Добијање ароматских карбоксилних киселина.
Наравно, индустрија покушава да примени оне методе у којима су сировине што јефтиније и катализатори су мање токсични. За синтезу алдехида је оксидација алкена кисеоником.

Индустријске апликације и значење
Употреба алдехида и кетона врши се у индустријама као што су:
- фармацеутика;
- хемијска синтеза;
- медицина;
- парфимеријско подручје;
- прехрамбена индустрија;
- производња боја и лакова;
- синтеза пластике, тканина и још много тога.
Можете одредити више од једног подручја, јер се годишње синтетише само формалдехид око 6 милиона тона годишње! Његов 40% раствор се зове формалин и користи се за складиштење анатомских објеката. Он се бави и производњом лекова, антисептика и полимера.
Ацетиц алдехиде, т или етанал, такође масовно произведен производ. Годишња потрошња у свету износи око 4 милиона тона, што је основа многих хемијских синтеза на којима се формирају важни производи. На пример:
- сирћетна киселина и њен анхидрид;
- целулоза ацетат;
- лекови;
- бутадиен - основа гуме;
- етил алкохол ;
- ацетатна влакна.
Ароматски алдехиди и кетони су саставни део многих укуса, како хране тако и парфема. Већина њих има веома пријатне цветне, цитрусне, биљне ароме. То вам омогућава да производите на њиховој основи:
- освеживачи ваздуха различитих врста;
- тоалет и парфемска вода;
- разна средства за чишћење и детерџенте.
Неки од њих су ароматизирани прехрамбени адитиви дозвољени за конзумирање. Њихов природни садржај у етеричним уљима, воћу и смолама доказује могућност такве употребе.
Индивидуални представници
Такав алдехид, као цитрал, је течност са високим вискозитетом и јаком аромом лимуна. У природи се налази у етеричним уљима потоњег. Такође у саставу еукалиптуса, сирка, кебаба.
Добро познате области његове примене:
- педијатрија - снижавање интракранијалног притиска;
- нормализација крвног притиска код одраслих;
- компонента медицине за органе вида;
- део многих мириса;
- антиинфламаторни и антисептички;
- сировине за синтезу ретинола;
- укус за храну.