Алдехиди: хемијска својства, припрема, структура
Практично све хемикалије око нас тестирају људи на основу њихових потреба и захтева. Свако једињење има јединствен, инхерентан скуп карактеристика и својстава, од којих се бирају корисни и неопходни за нас у свакодневном животу. Дотични алдехиди такође нису изузетак.
Скромно дете органске хемије
Међу угљеничним једињењима који се називају органским, постоје добро познати, који, како кажу, су "широко познати". На пример, глукоза, етил алкохол или пластику. Алдехиди у овом смислу немају среће. О њима је познато само уским стручњацима, па чак и средњошколцима, који су тешко радили студирајући хемију за упис на универзитет. У ствари, таква једињења (као што су ацеталдехид) чије хемијске особине сматрамо, нашироко се користи иу индустријској производњи иу свакодневном животу.
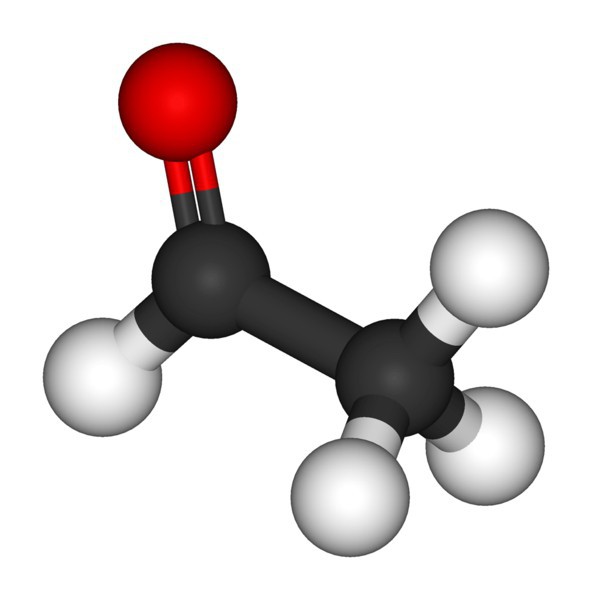
Аппле оф цонтентион
Нажалост, открића у науци често се не појављују ружичаста. Алдехиди, њихова хемијска структура и својства откривени су као резултат дугих спорова и дискусија међу научницима из деветнаестог века. И такви познати хемичари као што су Лиебиг и Добереинер чак су се и мало борили у шали, откривајући ко заправо поседује длан у добијању и изолацији ацетатног алдехида у свом чистом облику. Екстрахован је из паре етанола која је прошла преко платинске мреже, која служи као катализатор реакције. Једино што је могло да помири противнике било је безусловно прихватање свих хемичара имена нове класе супстанци - алдехида, што буквално значи "алкохоли без водоника". Она указује на методу њиховог добијања из алкохола елиминацијом два атома водоника.

Нећете бити збуњени ни са чим
Имајући у виду физичка и хемијска својства алдехида, лако је осигурати да су они довољно специфични. Дакле, формалдехид, који је отрован гас, има оштар, загушљив мирис. Њен 40% водени раствор, зван формалин, изазива необичан мирис у анатомским лабораторијама и мртвачницама, где се користи као средство против труљења, чувајући протеине органа и ткива.

Ацетатни алдехид, који је следећи у хомологној серији, је безбојна течност која је лако растворљива у води са непријатним мирисом труле јабуке. Алдехиди, хемијска својства карактерисана оксидационим и адицијским реакцијама, могу се претворити у супстанце генетски сродних класа: карбоксилне киселине или алкохоле. Размотрите их са специфичним примерима.
Алдехиде Бусинесс Цард
У органској хемији, као, у ствари, у неорганском, постоји нешто као "квалитативна реакција". Може се упоредити са сигналом који сигнализира да се ради управо о супстанцама одређене класе, на пример, са алдехидима. Они потврђују хемијска својства алдехида реагујући са раствором амонијака сребрног оксида и бакарним хидроксидом када се загревају (реакција огледала у сребру)
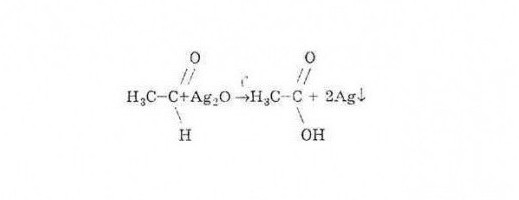
Производ реакције ће бити чистог сребра ослобођеног у облику огледалног слоја на зидовима цеви.
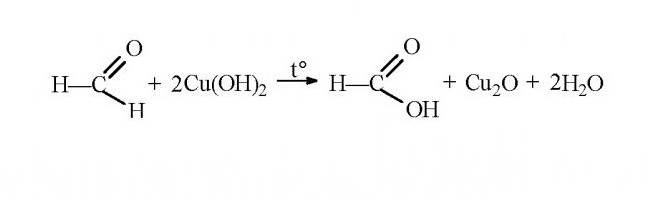
Као резултат, реакција таложи оксид бакра обојене циглом.
Двоструке супстанце
Сада је вријеме да се позабавимо таквим феноменом карактеристичним за све. органска материја укључујући и алдехиде, као изомерију. Она је потпуно одсутна у свету неорганске хемије. Све је једноставно тамо: само једно специфично једињење са инхерентним физичким и хемијским својствима одговара једној хемијској формули. На пример, формула ХНО 3 одговара једној супстанци, која се зове азотна киселина, са тачком кључања од 86 ° Ц, са оштрим мирисом, веома хигроскопним.
У области органске хемије, изомери су живи животи, у којима су формуле исте и својства су различита. На пример, формула Ц4Х8О има два потпуно различита алдехида: бутанал и 2-метил пропанал.
Њихове формуле:
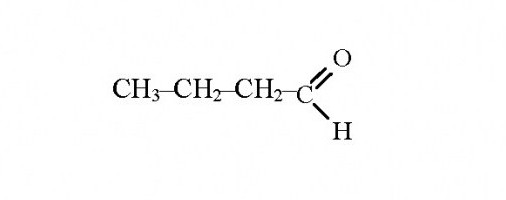
Изомерни алдехиди, чија хемијска својства зависе од њиховог састава и структуре, одличан су доказ генијалне теорије о структури органских једињења коју је створио руски научник М. Бутлеров. Његово откриће има исти фундаментални значај за хемију као и периодични закон Д Менделејева.
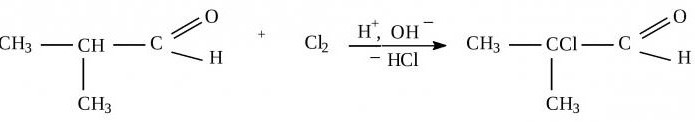
Јединствени угљеник
Одличан доказ теорије М. Бутлеров служи хемијским особинама алдехида. Органска хемија, захваљујући истраживању руског научника, коначно је била у стању да одговори на питање које је изазвало више од једне генерације научника својом комплексношћу, наиме: како објаснити разноликост органских једињења која задивљују неку машту, која се заснива на феномену изомерије. Размотримо структуру молекула два алдехидна изомера: бутанал и 2-метилпропанал, који имају исту молекулску формулу - Ц4Х8О, али различиту структурну и стога се разликују по физичким и хемијским својствима.
Скрећемо пажњу на две најважније карактеристике атома угљеника, које се уводе као постулати у теорију М. Бутлерова:
1. Царбон у органска једињења увек тетравалентно.
2. Атоми угљеника могу да се комбинују међусобно и формирају различите просторне конфигурације: неразгранати и разгранати ланци или циклуси.
Према валенцији, на њих су нанизани атоми других хемијских елемената: водоник, кисеоник, азот, формирајући тако читав гигантски арсенал постојећих органских једињења (и има их више од 10 милиона), а константно се повећава због нових супстанци добијених хемија органске синтезе.
Што је поларнији то боље
Настављајући са проучавањем алдехида, њихове хемијске структуре и својстава, задржаћемо се на феномену поларитета атома који чине алдехидне молекуле. Дакле, атом угљеника алдехидне групе у молекули ацеталдехида добија парцијални позитивни набој, а атом кисеоника - делимично негативан. Разлог њиховог појављивања је следећи: електронска густина π-везе је мобилнија од σ-везе.

У општој формули алдехида, где је Р угљоводонични радикал повезан са алдехидном групом, на атому кисеоника формира се парцијални негативни набој и парцијални позитивни набој на атому угљеника. Тако, функционална група алдехида постаје јако поларизована, што узрокује високу реактивност ових супстанци. Једноставно речено, што је више поларизованих атома у молекулу супстанце, то боље и брже улази хемијске реакције. Брза оксидациона способност водониковог атома у алдехидној групи и реактивност карбонилне групе обезбеђују алдехиде са карактеристичним реакцијама адиције и полимеризације.
Живот у пластичном свету
Алдехиди, чије су хемијске особине због способности поликондензације и реакције полимеризације, постали су преци фенопласта и аминопласта - основних материјала модерне полимерне индустрије. Формалдехид и ацеталдехид служе као сировина за његова предузећа. Дакле, фенолформалдехидне смоле су фенопласти - најважније супститути за жељезне и обојене метале. Формалдехид се добија оксидацијом метана загревањем на 600 ° Ц у мешавини са ваздухом, као и оксидацијом метанола загреваног на 300 ° Ц преко бакарног катализатора. Тако, алдехиди, препарати и хемијска својства, које сматрамо, важна су сировина у реакцијама органске синтезе.

Извуци закључке
Као што видимо, у евиденцији алдехида има довољно неопходних и важних супстанци, као што су, на пример, формалдехид и ацетатни алдехиди, чије хемијске особине особа успешно користи у различитим сферама своје животне активности.