Кристал је шта?
Најчешће стање свих постојећих супстанци Земље и Космоса је кристално стање. Шта је то? Које врсте кристала су подељене? Како можете да кувате кристал код куће, прочитајте чланак.
Дефиниција
Кристал је тело чврсте конзистенције вишеструке форме. Његова појава је резултат локације честица: атома, молекула, иона у одређеном реду. Њихов задатак је да формирају редове, равне решетке и просторне решетке.

Вишеслојни кристали могу бити:
- у облику коцки - пирита;
- призме са шиљатим крајевима - камени кристал;
- дванаест - гранат;
- октаедар - жељезна руда (магнетит);
- драго камење - дијаманти, топаз, рубини и други.
Величина ових формација је прилично велика.
Кристал је тело чији врх мора одговарати атому, јону, молекулу. Руб, односно, сваки ред честица, а лице - решетка. Ако су прави кристали увећани много пута, може се видети да су врх, ивица и лице састављени од многих честица, редова, решетки, које су поредане паралелно.
Ad
Какви су кристали?
Стручњаци су идентификовали различите врсте кристала:
- Идеал - представља апстрактни модел са исправном формом, потпуном симетријом и глатким ивицама. Другим речима, концепт идеалног кристала садржи комплетан скуп најбољих својстава и квалитета којима се карактерише.

- Прави кристали су тела која заиста постоје у природи, у којима унутрашња структура може имати дефекте, постоје лица која нису савршена, а симетрија је потпуно смањена. Али прави кристал, упркос свим манама, обдарен је главним својством које га чини кристалом - распоредом честица у природном поретку.
Кристал расте из соли
Од соли, можете узгајати кристале код куће. За то вам је потребна со, стаклена посуда, конац, оловка, вода. Па како узгајати кристал соли?
- У чаши воде, сол се сипа у порцијама и темељито меша све док се потпуно не отопи.
- Течност се стави на ватру и загреје на 90 ° Ц. Вода се прокључа, али не кува. Раствор се хлади и филтрира - не сме бити талога.
- Затим је конац везан за оловку, а до њега је кристал соли или дугме, које прво треба умочити у слану отопину и осушити.
- Врх конца са причвршћеним мамцем је уроњен у посуду са раствореном соли тако да не додирује дно и зидове.
- Капацитет покријте чистом салветом и ставите на топло место. Температура треба да буде константна.

Време током којег ће кристал расти ће бити другачије. То зависи од жељене величине.
Просторна кристална решетка
Ако уместо честица - јона и атома - ставимо тачке, онда је структура кристала простор који је испуњен тачкама које се налазе у регуларном поретку. Ако их повежете са линијама, добићете просторну решетку која се састоји од следећих елемената:
Ad
- чворови, који се називају тачке расподеле кристалних честица;
- редови представљени скупом чворова који се повремено понављају на једнаким растојањима (чворови леже дуж правих линија);
- интервалима, што је удаљеност од једног до другог еквивалентног чвора (ови интервали су занемарљиви);
- равна решетка, која представља чворове и редове који се налазе у једној равни.
Врсте кристалних решетки
Решетке су различите. То зависи од природе честица кристала и везе између њих. Типови кристалних решетки су:
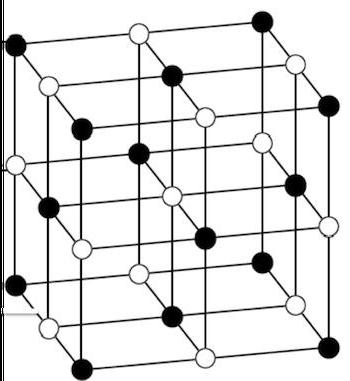
- Ион-решеткаста места садрже јоне позитивне и негативне. Они су међусобно повезани интеракцијом која се зове електростатика. Јони су једноставни и сложени. Ин кнотс натријум хлорид они су једноставни, а калијум сулфат - комплексан. У таквим кристалима иони су чврсто везани једни за друге, а супстанце се одликују тврдоћом, ватросталношћу, оне су нестабилне и растворљиве у води.
- Метал - такве решетке имају позитивне ионе, слободне електроне и атоме метала у свом саставу. Решетке формирају супстанце које карактерише метал бонд. Они су својствени једноставним металима и њиховим легурама. Метали, по правилу, имају различите тачке топљења, али сви, без изузетка, имају метални сјај, пластичност, кованост, добру електричну и топлотну проводљивост.
- Атомски - за локације које карактерише присуство појединачних атома, међусобно повезаних тзв ковалентне везе. Решетка овог типа има дијамант, графит, кварц, песак, камени кристал, итд. Ове супстанце су издржљиве и чврсте, имају високу тачку топљења и тачку кључања.
- Молекуларна - је решетка чији чворови садрже молекуле који су међусобно повезани слабом интеракцијом, названом интермолекуларна, иако су атоми у молекулима чврсто повезани. Молекуларни кристали цристал латтице имају ниску тврдоћу и чврстоћу, ниску тачку топљења, као и кључање. Многе молекуларне супстанце имају тенденцију да буду течне и гасовите, оне су нестабилне и могу мирисати. Супстанце са таквом везом укључују воду, амонијак, нафтален, киселине, глукозу, шећер, итд.
Разлози за промену облика природних кристала
Кристали мењају свој облик из разних разлога. Један од њих је кршење услова у којима се формирају. Дакле, ако се магма полако стврдне, онда ће кварцна зрна имати неправилне, закривљене контуре. Други пример је када се уништи темељ, његови фрагменти се руше водом. Стога се кристали таквих стијена као што су кварц, магнетит и гранат често налазе у пијеску.
Облик таквих неразвијених кристала је ружан, њихова лица су прекинута. Кристал је геометријски правилан облик који се протеже не само на површину кристала, већ и на његову унутрашњу структуру. Ту је раздаљина између честица, они не попуњавају читав простор, односно њихова локација има одређени поредак својствен само овој супстанци.
Ad
Занимљиве информације о кристалима
На територији бивше Совјетски савез 1958. године научници су пронашли огромни кристал кварца. Дужина му је била 7,5 м, ширина 1,5 м, маса 70 тона, на које су наишли берилски кристали масе 18 тона и дужине 5 метара, док су у налазима чешћи кристали микроскопских величина.

У источном дијелу Оренбуршке регије, имао сам среће да нађем камени кристал чији је кристал био 170 цм дуг, 80 цм широк и 784 кг масе. Иронично је назван "беба". Тренутно, овај кристал се налази на улазу у Уралски геолошки музеј у граду Екатеринбургу.