Хомогене реакције: описи и примери
За правилне хемијске реакције, важно је знати које су услове под којима се оне појављују. Хомогена средина реагенса омогућава да се одреди брзина њихове интеракције. Постоје посебни фактори који могу успорити или убрзати хомогене реакције.
Класификација
Хемијске интеракције могу се поделити у различите групе због присуства великог броја критеријума. 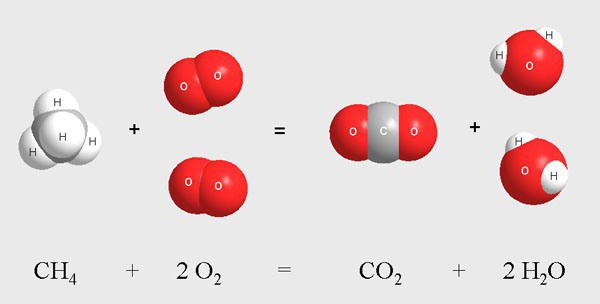
Постоје сљедећи знакови:
- Присуство дела реакционе фазе. Реакције могу бити хомогене или хетерогене.
- Промена у оксидативном степену реагујућих супстанци.
- Отпуштање или апсорпција топлоте.
- Тип промене у супстанцама које реагују у вези са једињењем, разградња, супституција или размена.
Хомогено окружење
То је хомогени систем у коме су хемијске и физичке карактеристике компонената у било којој тачки константне, а ако се мењају, онда на непрекидан темпо, без појаве оштрих скокова. Сви његови делови немају површинску сепарацију. Тако тече хомогено хемијске реакције.
Ad
Присуство неколико реагенса у хомогеној фази не може се визуелно одредити или механички раздвојити. Ова особина је могућа због равномјерне расподјеле композитних честица једне компоненте у другој.
Примери хомогених фаза укључују гасне смеше, смрзнуту воду и растворе у течном или чврстом облику.
Одређивање хомогених интеракција
Називају се и хомофазне реакције. То су процеси који се одвијају у региону једног хомогеног медија, а реагујуће компоненте и резултујући производи су у константном стању. 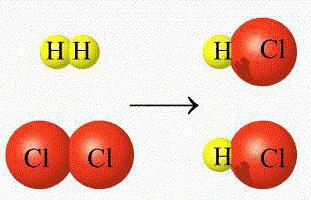
Хомогене реакције имају вредности које остају исте, и ако се мењају, онда са континуираном брзином.
Када се процес одвија у подручју раздвајања двије фазе, они се називају хетерогени.
Ако су реакције вишестепене, оне могу бити мешовитог типа. У њима се почетне фазе одвијају у хомогеном медију, а завршни процеси у хетерогеној фази. Такве интеракције најчешће се јављају у природи.
Ad
Хомогене реакције, примери једначина
То укључује процес хлорисања молекула метана у гасном окружењу. Ова реакција се одвија на високим температурама или када је изложена ултраљубичастом зрачењу. Као резултат мешања метана и хлора долази до фазне интеракције егзотермног типа.
Међупроизводи су гасовите супстанце, које укључују молекуле хлорометана, дихлорометана, трихлорометана, хлороводоника. Током реакције долази до постепене замене атома водоника у метану до атома хлора. Коначна супстанца је угљен тетраклорид.  Све фазе се одвијају у гасном средству назначеном стрелицом горе. Шематски, процес изгледа овако:
Све фазе се одвијају у гасном средству назначеном стрелицом горе. Шематски, процес изгледа овако:
Х2ЦХ2 + ЦлЦл2Х2ЦХЦл2 + ХЦл
Х2ЦХЦл + ЦлЦл2Х2ЦЦл2 + ХЦл
Х 2 ЦЦ 2 2 + ЦлЦл ХЦ ХЦЦл 3 ↑ + ХЦл
ХЦЦл 3 + ЦлЦл + ЦЦл 4 + ХЦл
Постоје и једнофазне хомогене реакције. Примери таквих интеракција су наведени испод.
Процеси хомофазе укључују:
- раздвајање пентавалентног азотног оксида у гасном средству под дејством високе температуре: Н 2 О 5 Н + Н 2 О 5 → НО2 + НО2 + НО2 + НО2 + О2;
- неутрализационог раствора натријум хидроксид раствор хлороводоничне киселине да се формира раствор натријум хлорид и вода: ХЦл + НаОХ → НаЦл + Х20;
- сагоревање етана са ослобађањем тетравалентног угљендиоксида и водене паре: С 2 Н 6 С + С 2 Н 6 7 + 7О 2 4 → 4СО 2 + 6Н 2 О ↑;
- конверзија молекулског кисеоника током олује у озон: 3О 2 2 → 2О 3 ↑.
Хомогене реакције се често јављају у течном медију. То укључује процесе халогенације, раздвајање различитих комплексних једињења на једноставнији или радикални, замену неких атома другим нуклеофилним или електрофилним типом, елиминацију делова молекула или њихово преуређење, продужење ланца услед полимеризације, оксидативне интеракције. Као резултат, формирају се течни производи.
Стопа реакције је хомогена
Ток процеса може имати различите временске интервале. Важна карактеристика ове интеракције је брзина хомогене реакције. Он представља нумеричку вредност која одређује промену концентрације било ког реагенса у одређеном временском периоду. 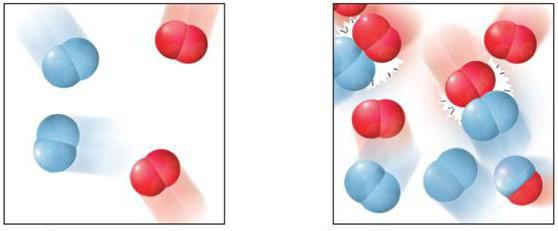
Може се окарактерисати на други начин: као вредност која успоставља промену броја интеракционе компоненте у датој запремини током одређеног времена. Главни услов је одсуство масовне промене у систему.
Ad
При израчунавању брзине реакције у хомогеном медију (означеном као Ви), користи се смањење или повећање моларне количине реактанта (Ц и ) током одређеног времена (т). Постоји посебна формула за израчунавање:
В и = ± Ц и / т.
За хемијски процес ХЦл + НаОХ → НаЦл + Х 2 О, брзина протока се може одредити смањењем концентрације сваког реагенса. (хлороводонична киселина или натријум хидроксид) или повећањем количине производа конверзије (натријум хлорид или вода) током временског периода под константним температурним условима.
Да би се одредила брзина хомогених реакција, концентрација се узима у моловима по литру, а време се мери у секундама. Израчун је следећи:
В и = ± Ц и / т = - [ХЦИ] / т = - [НаОХ] / т = [НаЦл] / т = [Х20] / т.
Фацторс Аффецтинг Спеед
Реакција је хомогена, у којој је брзина датог процеса директно пропорционална датој супстанци по јединици запремине. Што је више молекула укључено, то је бржа интеракција. 
Главни фактори који утичу на брзину процеса у хомогеном средству су концентрација реагенса и продуката реакције, њихова хемијска природа, температурни услови, притисак у реакционом волумену, као и присуство убрзивача који катализују промене.
Ad
Зависност брзине реакција од загревања утврдио је научник Вант-Хофф. Према његовим ријечима, свако повећање температуре за 10 ° повећава брзину у хомогеним реакцијама за 2 до 4 пута. У топлијем окружењу, молекули почињу да се активније активирају, сударају се међусобно, што доводи до њихове интеракције.
Временом се хомогене реакције одвијају различитим интензитетом, тако да њихове брзине могу бити истините (у одређеном тренутку) и просечне, што треба узети у обзир у прорачунима.