Оксид олова: формула, својства, метода добијања
У овом чланку бавићемо се оним што је олово оксид, показати његову формулу, узети у обзир хемијске и физичке карактеристике, а такође не заборавити да говоримо о томе како га добити. Опћенито, овај чланак ће се свидјети онима који желе или су већ упознати у кемији. На крају крајева, олово се налази свуда. Ако још увек не знате његов опсег, прочитајте чланак да бисте разумели пуни потенцијал овог хемијског елемента периодног система.
Начини да га добијете
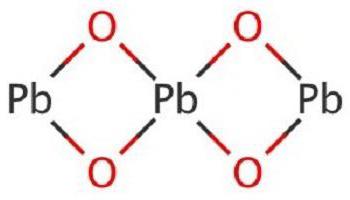
У почетку ћемо разумети оно што се назива оловни оксид. Традиционално се назива оловни оксид и група је бинарних супстанци које формирају елементи метала олова и неметалног кисеоника. Постоји шест главних облика ПбО: ПбО2, ПбО, Пб12О19, Пб12О17, Пб3О4. Свака од њих има своје структурне особине молекула, методе производње и опсег. Најчешћи облици су оксид олова (ИИ) и (ИВ).
Физичке карактеристике
Оксид олова, чија је формула ПбО, може бити у две врсте модификација: висока и ниска температура. Прелази са високе температуре на ниско-температурни облик јављају се спорије него у обрнутом редоследу. Као резултат, елемент може да остане у метастабилности на собној температури, ау процесу брушења може да промени облик модификације.

Испаравање се одвија једнако, најчешће у облику Пб2О2 и Пб4О4. Такође, ова група оксида је полупроводник. Према врсти проводљивости, у зависности од састава, али не прелазећи границе хомогености, оксиди су рупа и електронски. У боји су обично жуте, црвене и црне.
Хемијске особине и својства
Растварање се добро одвија у азотним и кисеоничним киселинама, растворљивост у сумпорној и хлороводоничној киселини се погоршава, јер се формирају ПбЦ12 и ПбСО4, који су слабо растворљиви. Када се раствори у алкалном медијуму, формирају се хексахидроксоплумбати (На2 [Пб (ОХ) 4]). Они су јаки оксидациони агенси, од којих неки могу да показују амфотерна својства - оксидују и апсорбују друге супстанце. Сви они могу оксидирати у различита стања, на примјер, на отвореном, ПбО на температури од 370 ступњева ће постати Пб12О17, на 540 ступњева Пб3О4 се формира, ау водику (Х2) и угљичном моноксиду (ЦО) метал се формира редукцијом.
Оксид олова ИИ
ПбО је неорганско једињење које је слабо растворљиво у води. То је бинарна супстанца у облику црвених или жутих кристала. У овом једињењу, олово показује другу валенцију, која одговара константној валенцији кисеоника. Налази се у природи са нечистоћама, на пример, у маски или оловном осигурачу.
Како добити олово у индустрији? Производи се проласком кисеоника кроз олово загрејано на температуру од 600 степени (2Пб + О2-2ПбО), загревањем оловног хидроксида на температурама од око 100-145 степени (Пб (ОХ) 2 -ПбО + ЦО2), и разлагањем нитрата (2Пб (НО3) ) 2–2Пб + 4НО2 + О2), загревање оловног карбоната (ПбЦО3 - ПбО + ЦО2), разлагање олова диоксида (2ПбО2 - ПбО + О2), и оксидација оловних сулфида (2ПбС + 3О2 - 2ПбО + 2СО2).
По својим својствима, ПбО (ИИ) је способан да формира кристале у две варијанте модификације које су стабилне на 489 степени и више.

Алфа модификација (оловни угљеник) је црвени кристал тетрагонског система, са просторном групом П 4 / нмм. Индекс растворљивости у води је α 0,279 22 . Бета модификација (масикот) показује метастабилност на собној температури, има жуту боју, кристалну форму, ромбичну синонију, просторну групу П бцм. Индекс растворљивости у води је β 0,513 22 г / 100 мл.
Оксид може довести до амфотерних особина у интеракцији са киселинама (ПбО + 2ХЦл - ПбЦл2 + Х2О) и алкалијама (ПбО + 2НаОХ - (400 степени) На2ПбО2 + Х2О). Може да оксидује, у интеракцији са кисеоником до Пб3О4, и у воденој суспензији са бромом оксидује до олова диоксида ПбО2. Опоравак метала настаје уз учешће угљен моноксид водоник и алуминијум. У стању влаге упија угљен диоксид при формирању базних соли.
Оксид олова ИВ
Оловни оксид 4, такође познат као оловни диоксид, има формулу ПбО2. То је оксид вишег степена. Као и остала оловна једињења са кисеоником је бинарна супстанца. То је тамно браон прах, прилично тежак, који има мирис озона. Раније се могла наћи под називом пероксид, или оловни пероксид.

ПбО2 се ископава у индустрији прерадом нитратна киселина црвено олово, праћено прањем, усисавањем и сушењем: Пб3О4 + 4ХНО3 - ПбО2 + 2Пб (НО3) 2 + 2Х2О.
Тачка топљења овог једињења је 290 степени, густина је 9.38 г / цм3, моларна маса је 239.1988 г / мол. Олово диоксид 4 је веома јак оксидациони агенс, може да замени хлор из концентроване хлороводоничне киселине грејањем (ПбО2 + 4ХЦл - ПбЦл2 + Цл2 + 2Х2О). Соли мангана (ИИ) се такође оксидују у перманганат (5Пб02 + 2МнС04 + 3Х2С04-5ПбС04 + 2ХМн04 + 2Х2О). То је врло отровна супстанца.
Апплицатион
Опсег оловног диоксида је најразличитији. Оловни оксид 4 налази своју примену обављајући функцију сикативног (уљане супстанце потребне за убрзавање процеса сушења боја), катализатора (супстанце неопходне за убрзавање протока) хемијске реакције између једињења која нису део коначног састава продуката било које реакције која се одвија) и оксидационог агенса (супстанце које укључују атоме способне за везивање слободних електрона за себе током хемијске реакције, оксидациони агенс се такође може назвати акцептором).

ПбО2 се широко користи у батеријама олово-сумпорне киселине, као позитивне масе електрона у галванским ћелијама. Често, али у малим количинама, може се користити као премаз за електроде за побољшање процеса електролизе. Олово диоксид 2 се користи у производњи редбеда, ПбО2 се може наћи у батеријама. Оловни оксид се широко користи у производњи оловних стакала и глазура. Пб3О4 се може наћи у оловним батеријама као кит и као пигмент за боје против корозије. Већина оловних оксида се користи у производњи радио-инжењеринга, гумених производа. Они су такође неопходни у процесу екстракције оловних соли током хемијске синтезе.