Физичко-хемијске особине толуена, једначине реакције
Толуен је метилбензен, који је безбојна течност која припада класи арена, који су органска једињења са ароматичним системом у композицији.
Кључна карактеристика ове супстанце може се сматрати њеним специфичним мирисом. Међутим, ово није једина "карактеристика" супстанце. Толуен има много својстава и карактеристика, и све их треба укратко описати.

Мало историје
Хемијска својства толуена почела су да се проучавају пре нешто више од 200 година, када су први пут добијена. Супстанцу је 1835. године открио француски апотекар и хемичар Пиерре Јосепх Пеллетиер. Научник је током дестилације борове смоле добио толуен.
Три године касније, француска физичарка Хенри Ст. Цлаир Девилле изолирала је ову супстанцу из балзама, који је донио из колумбијског града Толу. У част овог пића, у ствари, веза и добио своје име.
Опште информације
Шта је са карактеристикама и хемијским својствима толуена? Супстанца је испарљива покретна течност са јаким мирисом. Има благи наркотички ефекат. Реагује са неограниченом количином угљоводоника, у интеракцији са етрима и естрима, са алкохолима. Не мијеша се с водом.
Карактеристике су следеће:
- Супстанца је назначена формулом Ц7Х8.
- Његова моларна маса је 92,14 г / мол.
- Густина је 0,86694 г / цм3.
- Тачка топљења и врелишта су −95 и 110,6.
- Специфична топлота испаравања је 364 кЈ / кг.
- Температура критичног фазног прелаза је 320 ° Ц.
Ова супстанца је такође запаљива. Спаљено са задимљеним пламеном.
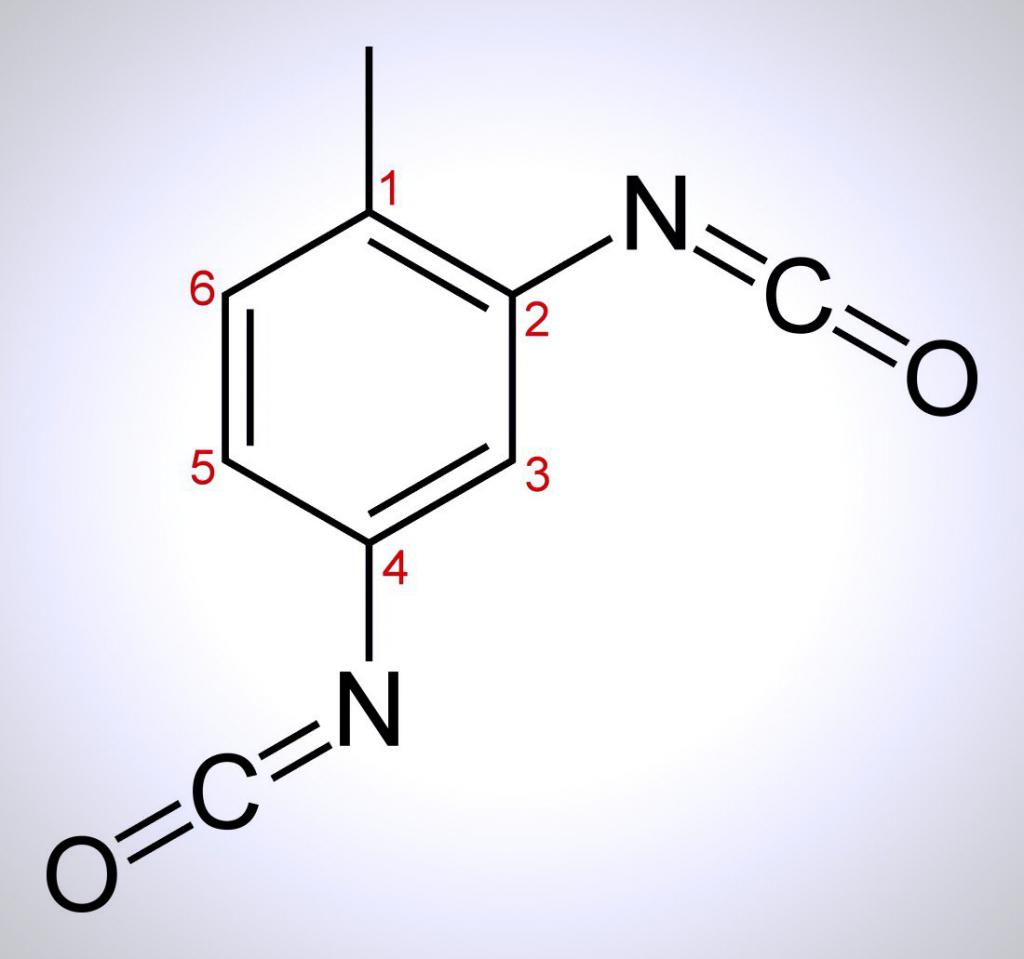
Основна хемијска својства
Толуен је супстанца коју карактеришу реакције електрофилне супституције. Они се јављају у такозваном ароматичном прстену, показујући абнормално високу стабилност. Ове реакције се одвијају углавном у пара и орто позицијама у односу на метил групу -ЦХ3.
Односи се на хемијска својства толуена, реакцију озонолизе и додавање (хидрогенирање). Под утицајем одређених оксидационих агенаса, метилна група постаје карбоксил. За ову сврху се најчешће користи алкални раствор калијум перманганата или неконцентрисан. нитратна киселина.
Такође треба напоменути да се толуен може спонтано запалити. Ово захтева температуру од 535 ° Ц. Блиц се одвија на 4 ° Ц.

Настајање бензојеве киселине
Способност супстанце о којој се расправља да учествује у овом процесу је такође последица њених хемијских својстава. Толуен, који реагује са јаким оксидационим средствима, формира најједноставнију монобазну бензојеву карбоксилну киселину која припада ароматичној серији. Његова формула је Ц6Х5ЦООХ.
Киселина има облик белих кристала, који се добро растварају у диетил етру, хлороформу и етанолу. Добија се следећим реакцијама:
- Толуен и калијум перманганат, у интеракцији у киселој средини. Формула је следећа: 5Ц6Х5ЦХ3 + 6КМнО4 + 9Х2С04 → 5Ц6Х5ЦООХ + 6МнСО4 + 3К2С04 + 14Х2О.
- Толуен и калијум перманганат, који делују у неутралном окружењу. Формула је следећа: Ц6Х5ЦХ3 + 2КМнО4 → Ц6Х5ЦООК + 2МнО2 + КОХ + Х20.
- Толуен, у интеракцији са светлосним халогенима, енергетски оксидациони агенси. Настаје према формули: Ц6Х5ЦХ3 + Кс2 → Ц6Х5ЦХ2Кс + ХКС.
Бензојева киселина добијена као резултат ових реакција користи се у многим областима. У основи се користи за добијање реагенса - бензоил хлорида, пластификатора бензоата, фенола.
Користи се иу конзервирању. Адитиви Е213, Е212, Е211 и Е210 су направљени на бази бензојеве киселине. Блокира ензиме и успорава метаболизам, инхибира раст квасца, плијесни и бактерија.
А бензојева киселина се користи у медицини за лечење кожних болести и као експекторанс.

Пријем супстанце
Реакционе једначине које показују горе наведене хемијске особине толуена нису све што бих желео да размотрим. Важно је говорити о процесу добијања ове супстанце.
Толуен је производ индустријске прераде бензинских фракција уља. Ово се назива и каталитичко реформирање. Супстанца се изолује селективном екстракцијом, након чега се врши дестилација - мешавина се раздваја протуструјним преносом топлоте и масе између течности и паре.
Често се овај процес замењује каталитичком дехидрогенацијом хептана. Ово је органски алкан са формулом ЦХ3 (ЦХ2) 5ЦХ3. Дехидрогенација се одвија преко метилциклохексана - циклоалкана са формулом Ц7Х14. То је моноциклични угљоводоник чија метилна група има један атом водоника супституисан.
Пречистити толуен на исти начин као и бензен. То је само ако се примени сумпорна киселина потребно је узети у обзир - ова супстанца је лакше сумпоризирана. То значи да је приликом чишћења толуена потребно одржавати нижу температуру. Испод 30 ° Ц, да будемо прецизни.

Толуен и бензен
Пошто су ове две супстанце сличне, вреди извршити поређење хемијских својстава. Бензен и толуен подлежу реакцијама супституције. Међутим, њихова брзина протока је различита. Пошто метил група у молекули толуена утиче на ароматични прстен, он брже реагује.
Међутим, бензен показује отпорност на оксидацију. Тако, на пример, када утиче калијум перманганат, ништа се не догађа. Али толуен у овој реакцији формира бензојеву киселину, као што је већ раније поменуто.
Истовремено, познато је да засићени угљоводоници не реагују са раствором калијум перманганата. Тако је оксидација толуена последица дејства бензенског прстена на метилну групу. Ову тврдњу потврђује теорија Бутлерова. У складу са тим, атоми и њихове групе у молекулима врше узајамни утицај.
Фриедел-Црафтс Реацтион
Много је горе речено о формули и хемијским особинама толуена. Али још није споменуто да је ова супстанца сасвим могуће добити из бензена, ако изводите Фриедел-Црафтсову реакцију. Ово је начин ацилације и алкилације ароматичних једињења помоћу киселих катализатора. То укључује бор трифлуорид (БФ 3 ), цинк хлорид (ЗнЦл2), алуминијум (АлЦл3) и гвожђе (ФеЦл3).
То је само у случају толуена, можете користити само један катализатор. А то је гвожђе трибромид, који је комплексно бинарно једињење неорганске природе са формулом ФеБр3. Реакција је следећа: Ц6Х6 + ЦХ3 Бр ФеБр3Ц6Х5ЦХ3 + ХБр. Тако се не комбинују само хемијска својства бензена и толуена, већ и способност да се добије једна супстанца из друге.

Опасност од пожара
Да не говорим о томе, говоримо о хемијским и физичким својствима толуена. На крају крајева, то је веома запаљива супстанца.
Спада у запаљиве течности класе 3.1. У ову категорију спадају дизел гориво, гасно уље и десензибилисани експлозиви.
Не дозволити да се у близини толуена јави отворени пламен, варнице или дим. Чак и мешавина пара ове супстанце са ваздухом је експлозивна. Ако се обављају дренажне радње, поштовање правила заштите од статичког електрицитета постаје од највеће важности.
Производни погони за рад у вези са толуеном имају снабдевање и одсисавање, а опрема - усисавање. Забрањена је употреба алата који могу дати искру. А ако се супстанца запали, треба је угасити само воденом маглом, механичком или хемијском пјеном. Изливени толуен се неутралише песком.
Опасност за људе
Карактеристике и хемијска својства толуена одређују његову токсичност. Као што је већ споменуто, његови парови имају наркотички учинак. Посебно је јака у повишеним концентрацијама. Особа која је удисала испарења има јаке халуцинације. Мало људи зна, али до 1998. ова супстанца је била део лепка Момент. Зато је био толико популаран међу зависницима.
Високе концентрације ове супстанце такође негативно утичу на нервни систем, слузокожу очију и кожу. Функција стварања крви је нарушена, јер је толуен врло отрован отров. Због тога се могу појавити болести као што су хипоксија и цијаноза.
Постоји чак и концепт толуенске токсикоманије. Има канцерогено дејство. На крају крајева, пар који пролази кроз кожу или дишне органе у људском телу, утиче на нервни систем. Понекад ти процеси не могу бити обрнути.
Поред тога, парови могу изазвати летаргију и пореметити функционисање вестибуларног апарата. Зато људи који раде са овом супстанцом раде у добро проветреним просторима, увек под напрезањем, и користе специјалне гумене рукавице.

Апплицатион
Да би се завршила тема о физичко-хемијским својствима толуена треба узети у обзир подручја у којима је ова супстанца активно укључена.
Углавном се користи као сировина за производњу нитротолуена, бензилхлорида, бензојеве киселине, као и других органска материја.
Ово једињење је такође ефикасан растварач за многе полимере (аморфне кристалне супстанце високе молекулске масе). Често се додаје у састав комерцијалних растварача за боје и лакове, неке лекове. Чак иу производњи експлозива ово једињење је применљиво. Тринитротолуен и тротилтол се добијају уз његово додавање.