Функција и структура протеина
Протеини су органска високо молекуларна једињења. Ове супстанце се такође називају протеини, полипептиди. Затим размотрите структуру и функцију протеина.
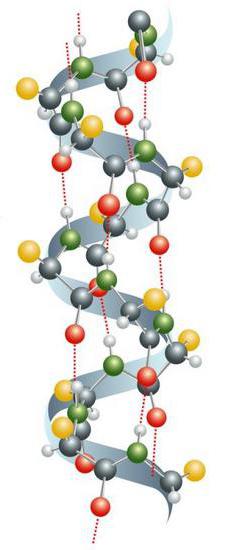
Опште информације
Хемијска структура протеина је представљена алфа-амино киселинама везаним у ланцу преко пептидне везе. У живим организмима, састав одређује генетски код. У процесу синтезе, у већини случајева, користи се 20 аминокиселина стандардног типа. Многе њихове комбинације формирају протеинске молекуле са широким спектром својстава. Аминокиселински остаци су често подвргнути пост-транслацијским модификацијама. Они се могу појавити пре него што протеин почне да обавља своје функције, као иу процесу своје активности у ћелији. У живим организмима, често неколико молекула формира комплексне комплексе. Пример за то је фотосинтетска асоцијација.
Ad
Додељивање везе
Протеини се сматрају важном компонентом исхране људи и животиња због чињенице да се у њиховим организмима не могу синтетисати све неопходне аминокиселине. Неке од њих би требале доћи протеинска храна. Главни извори једињења су месо, орашасти плодови, млеко, риба, житарице. У мањој мери, протеини су присутни у поврћу, печуркама и бобицама. Током варења ензима, конзумирани протеини се уништавају до амино киселина. Они се већ користе у биосинтези сопствених протеина у телу или пролазе даље пропадање - за енергију.
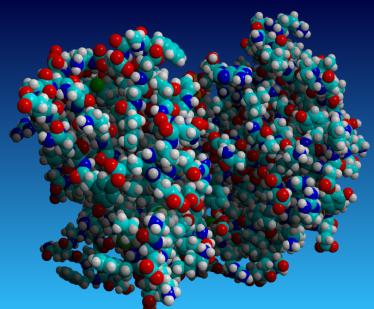
Хисторицал бацкгроунд
Секвенцу структуре инсулинског протеина први пут је одредио Фредериус Сенгер. За свој рад добио је Нобелову награду 1958. године. Сангер је користио методу секвенцирања. Коришћење дифракције рендгенско зрачење затим су добијене тродимензионалне структуре миоглобина и хемоглобина (крајем 1950-их). Радове су извели Јохн Кендрев и Мак Перутз.
Ad
Структура молекула протеина
Укључује линеарне полимере. Они су, пак, састављени од алфа-аминокиселинских остатака, који су мономери. Поред тога, протеинска структура може укључивати компоненте које имају не-амино киселинску природу, и аминокиселинске остатке модификованог типа. За означавање компоненти коришћене су 1- или 3-слово скраћенице. Једињење које садржи од два до неколико десетина остатака се често назива "полипептид". Као резултат интеракције алфа-карбоксилне групе једне аминокиселине са алфа-амино групом друге, појављују се везе (током формирања структуре протеина). У једињењу, Ц- и Н-крајеви су изоловани, у зависности од тога која група аминокиселинских остатака је слободна: - ЦООХ или -НХ2. Ин прогресс синтеза протеина на рибозому као први терминал, по правилу, метионински остатак; приступање наредног врши се на Ц-крај претходних.
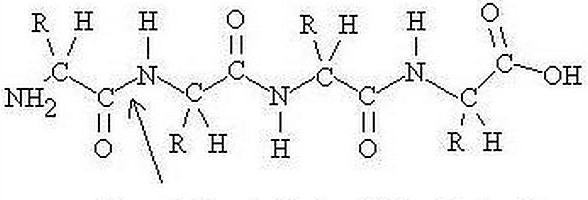
Нивои организације
Њих је понудио Линдрем-Ланг. Иако се ова подјела сматра помало застарјелом, она се и даље користи. Предложено је да се разликују четири нивоа организације повезивања. Примарна структура молекула протеина одређена је генетским кодом и карактеристикама гена. За више нивое карактеристично је формирање током савијања протеина. Просторна структура протеина одређена је у читавом ланцу аминокиселина. Ипак, то је прилично лабилно. На њега могу утицати спољни фактори. У том смислу, исправније је говорити о конформацији једињења, најкориснијој и пожељнијој енергији.
Ad
Ниво 1
Он је представљен секвенцом аминокиселинских остатака полипептидног ланца. По правилу се описује коришћењем једног или три слова. Примарну структуру протеина карактеришу стабилне комбинације аминокиселинских остатака. Они обављају одређене задатке. Такви "конзервативни мотиви" остају сачувани у току еволуције врста. Према њима, често се може предвидети проблем непознатог протеина. Процењујући степен сличности (хомологије) у ланцима аминокиселина различитих организама, могуће је одредити еволутивну дистанцу између таксона који чине ове организме. Примарна структура протеина одређена је секвенцирањем или почетним комплексом мРНК користећи табелу генетског кода.
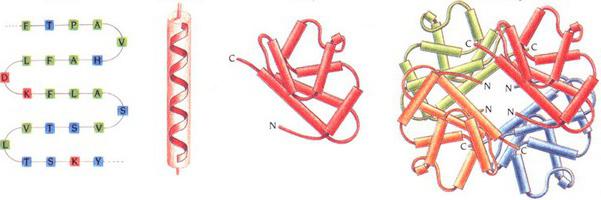
Локално уређење секције ланца
Ово је следећи ниво организације - секундарна структура протеина. Постоји неколико врста. Локално уређење ланчаног места полипептида стабилизовано је водоничним везама. Најпопуларнији типови су:
- Алпха хелик Они су представљени у облику густих свитака око дуге молекуларне оси. Један завој је сачињен од 3.6 аминокиселинских остатака. Висина хеликса је 0,54 нм. Ова секундарна протеинска структура се стабилизује интеракцијама Х- и О-пептидних група, које су једна за другом 4 јединице. Алфа хеликс може бити леворука или десна рука. Међутим, ово се најчешће детектује у протеинским једињењима. Електростатичке интеракције аргинина, лизина, глутаминска киселина. У непосредној близини, остаци леуцина, треонина, серина и аспарагина могу изазвати стеричну интерференцију са формацијом. Кршење алфа-хеликса (његов завој) је узроковано деловима пролина.
- Бета листе. Приказани су у облику неколико цик-цак полипептидних ланаца. У њима се формирају водикове везе између аминокиселина, релативно удаљених у примарној структури, или различитих протеинских ланаца. Везе су обично оријентисане Н-крајевима у супротном смеру (анти-паралелна оријентација). Приликом формирања бета листа, важна је мала величина бочних група аминокиселина.
- Неуређени фрагменти.
- 310- и π-хеликс и друго.

Просторна структура
Терцијарна структура протеина укључује елементе претходног нивоа. Стабилизирају их различите врсте интеракција. Хидрофобне везе су од највеће важности. У стабилизацији су укључени:
- Ковалентне интеракције.
- Јонске везе које се формирају између група аминокиселина које имају супротне набоје.
- Интеракције водоника.
- Хидрофобне везе. У процесу интеракције са околним Х20 елементима долази до савијања протеина тако да се из воденог раствора изолују бочне неполарне групе амино киселина. Хидрофилне групе (поларни) појављују се на површини молекула.
Терцијарна структура протеина одређена је магнетним (нуклеарним) резонантним методама, неким типовима микроскопије и другим методама.
Принцип полагања
Истраживања су показала да је између 2 и 3 нивоа погодно да се додели још један ниво. То се назива "архитектура", "стилски мотив". Одређује се релативним положајем компоненти секундарне структуре (бета ланци и алфа хеликса) унутар граница компактне глобуле, протеинске домене. Може постојати независно или бити укључен у састав већег протеина заједно са другим сличним. Утврђено је да су стилски мотиви прилично конзервативни. Налазе се у протеинима који немају ни еволутивне ни функционалне везе. Дефиниција архитектуре је основа рационалне (физичке) класификације.
Ad
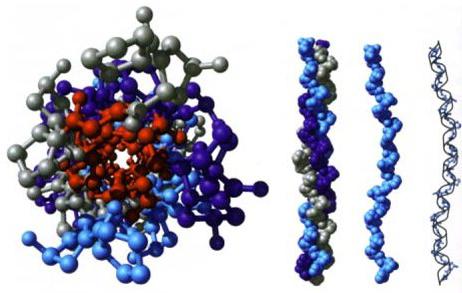
Организација домена
Са међусобним распоредом неколико полипептидних ланаца унутар једног протеинског комплекса, формира се квартарна протеинска структура. Елементи који су укључени у његов састав су формирани одвојено на рибозомима. Тек на крају синтезе почиње да се формира ова структура протеина. Може да садржи и различите и идентичне полипептидне ланце. Квартарна структура протеина стабилизована је због истих интеракција као на претходном нивоу. Неки комплекси могу укључивати неколико десетина протеина.
Структура протеина: одбрамбени циљеви
Полипептиди цитоскелета, који делују на неки начин као арматура, дају облик многим органоидима и учествују у његовој промени. Структурални протеини обезбеђују заштиту тела. На пример, овај протеин је колаген. Она чини основу међустаничне супстанце везивног ткива. Кератин такође има заштитну функцију. Формира основу рогова, перја, косе и других деривата епидермиса. Када се протеин веже за токсине у многим случајевима, јавља се детоксикација. То је задатак хемијске одбране тела. Посебно важну улогу у процесу неутрализације токсина у људском организму имају јетрени ензими. Они су способни да раздвоје отрове или их преведу у топљиви облик. То доприноси бржем транспорту из тела. Протеини присутни у крви и другим биолошким текућинама, пружају имунолошку заштиту, изазивајући реакцију на напад патогена и оштећења. Имуноглобулини (антитела и компоненте комплементарног система) су у стању да неутралишу бактерије, стране протеине и вирусе.
Ad
Регулациони механизам
Протеински молекули који не делују као извор енергије или као грађевински материјал контролишу многе интрацелуларне процесе. Дакле, због њих се врши регулација транслације, транскрипције, резања, активности других полипептида. Механизам регулације се заснива на ензимској активности или се манифестује специфичним везивањем за друге молекуле. На пример, фактори транскрипције, активатор полипептиди и репресор протеини су у стању да контролишу интензитет транскрипције гена. Истовремено, они интерагују са регулаторним секвенцама гена. Најважнија улога у контролисању тока интрацелуларних процеса приписана је протеинским фосфатазама и протеин киназама. Ови ензими активирају или инхибирају активност других протеина додавањем или цијепањем фосфатних група из њих.
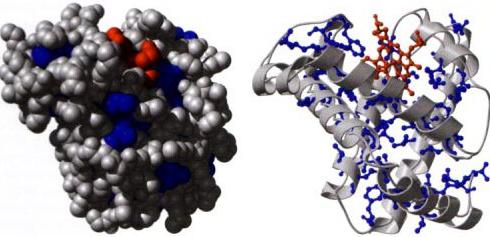
Задатак сигнализације
Често се комбинује са регулаторном функцијом. Ово је због чињенице да многи интрацелуларни, као и екстрацелуларни, полипептиди могу да преносе сигнале. Фактори раста, цитокини, хормони и друга једињења имају ову способност. Стероиди се транспортују крвљу. Интеракција хормона са рецептором делује као сигнал, због чега се активира одговор ћелије. Стероиди контролишу садржај једињења у крви и ћелијама, репродукцију, раст и друге процесе. Пример је инсулин. Регулише ниво глукозе. Интеракција ћелија се врши помоћу сигналних протеинских једињења која се преносе кроз међустаничну супстанцу.
Транспорт елемената
Растворљиви протеини укључени у кретање малих молекула имају висок афинитет за супстрат присутан у повишеним концентрацијама. Они такође имају могућност да га лако ослободе у подручјима са ниским садржајем. Пример је транспортни протеин хемоглобин. Помера кисеоник из плућа у друга ткива, а од њих - трансфере угљен диоксид. Неки мембрански протеини су такође укључени у транспорт малих молекула кроз ћелијске зидове, мењајући их. Цитоплазматски липидни слој је водоотпоран. То спречава дифузију напуњених или поларних молекула. Мембранске транспортне везе могу се подијелити на носаче и канале.
Редундантне везе
Ови протеини формирају такозване резерве. Они се акумулирају, на пример, у семену биљака, животињских јаја. Такви протеини делују као резервни извор материје и енергије. Нека једињења се користе од стране тела као аминокиселински резервоар. Они су, пак, прекурсори активних супстанци укључених у регулацију метаболизма.
Целл рецепторс
Такви протеини могу бити лоцирани или директно у цитоплазми или уграђени у зид. Један део везе прима сигнал. По правилу, то је обично хемијска супстанца, ау неким случајевима - механичко дејство (нпр. Истезање), светлост и други подражаји. У процесу излагања сигнала одређеном фрагменту молекула - полипептидног рецептора - почињу његове конформационе промене. Они изазивају промену у конформацији остатка, што преноси стимуланс на друге компоненте ћелије. Слање сигнала се може обавити на различите начине. Неки рецептори су способни да катализују хемијску реакцију, док други делују као ионски канали који се затварају или отварају под утицајем стимулуса. Нека једињења специфично везују посредне молекуле унутар ћелије.
Моторни полипептиди
Постоји читава класа протеина који обезбеђују кретање тела. Моторни протеини су укључени у контракцију мишића, кретање ћелија, активност флагела и цилија. Захваљујући њима, врши се и усмјерен и активан транспорт. Кинезини и динеини преносе молекуле дуж микротубула користећи АТП као извор енергије за хидролизу. Потоњи преносе органоиде и друге елементе ка центросому са периферних ћелијских места. Кинезини се крећу у супротном смеру. Динеини, поред тога, одговорни су за активност флагела и цилија.