Теорија електролитичке дисоцијације - једна од главних у хемији
Када се раствори у води, електролитске супстанце се разлажу у набијене честице - ионе. Супротно је моларизација или асоцијација. Формирање јона објашњава теорију електролитичке дисоцијације (Аррхениус, 1887). На механизам разлагања хемијских једињења током топљења и растварања утичу карактеристике типова хемијских веза, структура и природа растварача.
Електролити и непроводници
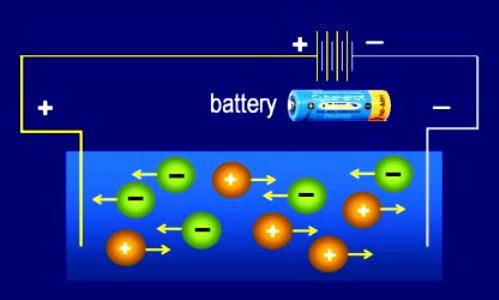
Разарање се дешава у растворима и растопи цристал латтицес и молекуле - електролитичка дисоцијација (ЕД). Распадање супстанци је праћено формирањем јона, појавом таквих својстава као што је електрична проводљивост. Није свако једињење способно да се дисоцира, већ само супстанце које се у почетку састоје од јона или високо поларних честица. Присуство слободних јона објашњава својство електролита за провођење струје. Базу, со, многе неорганске и неке органске киселине поседују ову способност. Неводници се састоје од ниско-поларних или неполаризованих молекула. Они се не разлажу на ионе, јер нису електролити (многи органски спојеви). Носиоци набоја су позитивни и негативни јони (катиони и аниони).
Улога С. Аррхениуса и других хемичара у проучавању дисоцијације
Теорију електролитичке дисоцијације доказао је 1887. године научник из Шведске С. Аррхениус. Али прве опсежне студије о својствима решења извео је руски научник М. Ломоносов. Доприносило је проучавању набијених честица насталих растварањем супстанци, Т. Гротгус и М. Фарадаи, Р. Ленз. Аррхениус је доказао да има много неорганских електролита и неких органска једињења. Шведски научник објаснио је електричну проводљивост раствора распадањем супстанце у ионе. Теорија Аррениусове електролитичке дисоцијације није придала важност непосредном учешћу молекула воде у овом процесу. Руски научници Менделеев, Каблуков, Коновалов и други су веровали да се одвија солватација - интеракција растварача и раствора. Када је реч о воденим системима, користи се назив „хидратација“. Ово је сложен физичко-хемијски процес, о чему сведоче формирање хидрата, термалних појава, промена боје материје и појава седимента.

Основне одредбе теорије електролитичке дисоцијације (ТЕД)
Многи научници су радили на разјашњавању теорије С. Аррхениуса. Било је неопходно побољшати га, узимајући у обзир савремене податке о структури атома, хемијској вези. Формулисане су главне одредбе ТЕД-а, које се разликују од класичних теза с краја КСИКС века:
- Процес топљења или растварања праћен је дисоцијацијом електролита у ионе. Дакле (на сугестију Фарадејевог) називају се честице са набојем ("+" или "-") које се разликују од неутралних атома у структури валентних љуски и стабилности, су обојене и безбојне. Иони могу бити једноставни: На + , Цл - , С 2- , Ал 3+ . Постоје набијене честице које се састоје од група атома: ЦО 2- , НХ 4+ . Из грчког језика назив "ион" се преводи као "лутање", што указује на случајност ширења ових честица.
- Утицај спољашњег електричног поља узрокује да се јони уредно крећу унутар простора електролита. Свака негативна честица је усмјерена на аноду (позитивна електрода). Иони са знаком "+" почињу да се крећу према катоди (негативна електрода).
- Истовремено, распадање у ионе и комбинација ових честица јављају се у растворима, тако да се дисоцијација односи на реверзибилне физичко-хемијске процесе.
Појава која се појављује мора се узети у обзир при састављању једнаџби: примијенити посебан знак реверзибилног процеса, израчунати негативне и позитивне набоје: морају се подударати у суми.
Механизам ЕД јонских супстанци
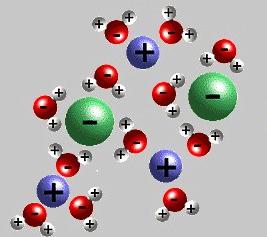
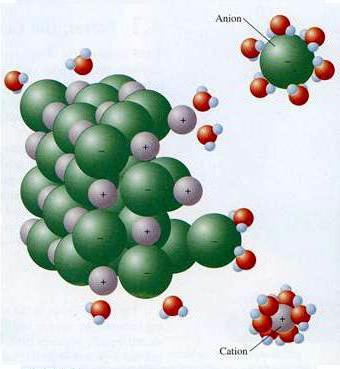
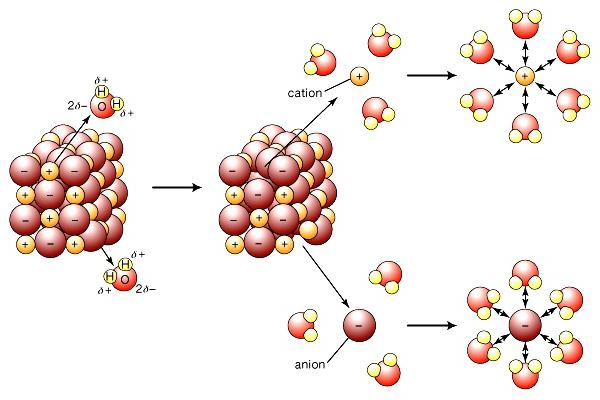
Модерна теорија електролитичке дисоцијације узима у обзир структуру електролитских супстанци и растварача. Када се растворе, везе између супротно набијених честица у ионским кристалима уништавају се дејством поларних молекула воде. Они буквално "вуку" јоне из масе у раствор. Распад је праћен формирањем солватне (у води - хидратација) љуске око јона. Поред воде, кетони, нижи алкохоли, имају већу диелектричну константу. Током дисоцијације натријум хлорид На + и Цл - иони региструју почетну фазу, што је праћено оријентацијом водених дипола у односу на површинске ионе у кристалу. У завршној фази, хидратизовани јони се ослобађају и дифундирају у течност.
Механизам једињења ЕД са ковалентно јако поларном везом
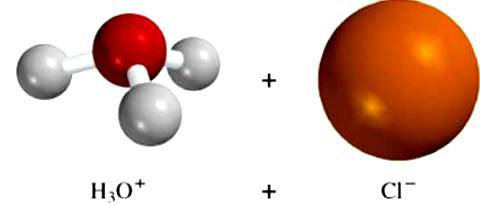
Молекули растварача утичу на кристалну структуру нејонских супстанци. На пример, ефекат водених дипола на хлороводоничну киселину доводи до промене типа везе у молекулу од ковалентног полара до јона. Супстанца дисоцира, хидрирани водонични и хлорни јони улазе у раствор. Овај пример доказује значај процеса који се јављају између честица растварача и раствореног једињења. Управо та интеракција доводи до формирања електролитних јона.
Теорија електролитичке дисоцијације и главне класе неорганских једињења
У светлу главних одредби ТЕД-а, електролит се може назвати киселином, а током распада који од позитивних јона може се детектовати само протон Х + . Дисоцијација базе праћена је формирањем или ослобађањем кристалне решетке само ОХ аниона и катиона метала. Нормална сол када се раствори даје позитиван метални ион и негативан - остатак киселине. Главну сол карактерише присуство два типа аниона: ОХ група и киселински остатак. У киселој соли катиона присутни су само водоник и метал.
Електролитска чврстоћа
Да би се окарактерисало стање неке супстанце у раствору, коришћена је физичка величина - степен дисоцијације (α). Нађите његову вредност од односа броја сломљених молекула до њиховог укупног броја у раствору. Дубина дисоцијације одређена је различитим условима. Важни диелектрични индикатори растварача, структура растворених једињења. Типично, степен дисоцијације опада са повећањем концентрације и повећава се са повећањем температуре. Често се степен дисоцијације одређене супстанце изражава у фракцијама јединице.
Класификација електролита
Теорија електролитичке дисоцијације на крају КСИКС века није садржала одредбу о интеракцији јона у раствору. Утицај молекула воде на дистрибуцију катјона и аниона је био незнатан за Арренија. Арренијове идеје о јаким и слабим електролитима су биле формалне. На основу класичних позиција може се добити α = 0.75–0.95 за јаке електролите. Експерименти су доказали иреверзибилност њихове дисоцијације (α → 1). Солубилне соли, сумпорне и хлороводонична киселина алкали. Делимично дисоциати сумпор, азот, флуоро флуор, фосфорна киселина. Слаби електролити су силицијумска, сирћетна, хидросулфурна и карбонска киселина, амонијум хидроксид, нерастворљиве базе. Вода се назива и слабим електролитима. Мали део Х 2 О молекула дисоцира, а јони су истовремено моларизовани.