Вода и њена физичка и хемијска својства. Структура воде
Најважнија супстанца наше планете, јединствена по својим својствима и саставу, је, наравно, вода. На крају крајева, захваљујући њој, постоји живот на Земљи, док није на другим познатим објектима Сунчевог система. Чврста, течна, у облику паре - она је неопходна и важна сваком. Вода и њена својства су предмет проучавања читаве научне дисциплине - хидрологије.
Количина воде на планети
Ако посматрамо индикатор количине овог оксида у свим агрегатним стањима, онда је то око 75% укупне масе на планети. Ово треба узети у обзир везану воду у органска једињења живих бића, минерала и других елемената.

Ако узмете у обзир само течно и чврсто стање воде, стопа ће пасти на 70,8%. Размотрите како се ти проценти расподељују, а који садрже дотичну супстанцу.
- Слана вода у океанима и морима, слана језера на Земљи 360 милиона км 2 .
- Слатка вода је неравномерно распоређена: у глечерима Гренланда, Арктика и Антарктика је обложена ледом од 16,3 милиона км 2 .
- 5,3 милиона км2 водиковог оксида је концентрисано у свежим ријекама, мочварама и језерима.
- Подземне воде су 100 милиона м 3 .
Зато астронаути из далеког свемира виде Земљу у облику плаве кугле са повременим деловима земље. Вода и њена својства, познавање карактеристика структуре су важни елементи науке. Осим тога, у новије вријеме човјечанство почиње искусити јасан недостатак свјеже воде. Можда ће такво знање помоћи у решавању овог проблема.
Ad
Састав воде и структура молекула
Ако узмемо у обзир ове показатеље, онда ће особине које ова манифестна материја испољити одмах постати јасне. Дакле, молекул воде се састоји од два атома водоника и једног атома кисеоника, стога има емпиријску формулу Х 2 О. Поред тога, електрони оба елемента играју важну улогу у конструкцији самог молекула. Да видимо каква је структура воде и њене особине.
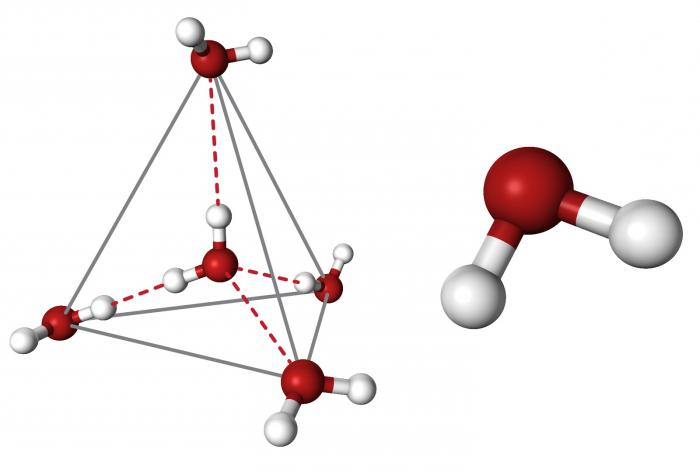
Очигледно је да је сваки молекул оријентисан око другог, и заједно чине заједничку кристалну решетку. Интересантно је да је оксид изграђен у облику тетраедра - атома кисеоника у центру, а два пара његових електрона и два атома водоника око су асиметрично. Ако повучете линију кроз центре језгра атома атома и повежете их, добићете тачно тетраедарски геометријски облик.
Ad
Угао између центра атома кисеоника и језгра водоника је 104,5 ° Ц. Веза је О-Х = 0,0957 нм. Присуство електронских парова кисеоника, као и његов већи електронски афинитет у односу на водоник, осигурава формирање негативно наелектрисаног поља у молекулу. Насупрот томе, језгра водоника формирају позитивно наелектрисани део једињења. Тако се испоставља да је молекул воде дипол. Ово одређује шта вода може бити, а њене физичке особине такође зависе од структуре молекула. За живе ствари, ове карактеристике играју виталну улогу.
Основна физичка својства
То се обично приписује кристалној решетки, тачки кључања и тачки топљења, посебним индивидуалним карактеристикама. Сви они и размислите.
- Структура кристалне решетке водиковог оксида зависи од агрегатног стања. Може бити чврст - лед, течност - главна вода у нормалним условима, гасовита - пара када се температура воде подигне изнад 100 ° Ц. Лед ствара лепе кристале са узорком. Роштиљ је опћенито лабав, али је спој врло јак, густоћа је ниска. Можете га видети на примеру снежних пахуљица или узорака мраза на стаклу. У обичној води решетка нема сталан облик, мења се и прелази из једног стања у друго.
- Молекул воде у свемиру има правилан облик лопте. Међутим, под дејством гравитације Земље, она је искривљена и у течном стању има облик брода.
- Чињеница да је структура водониковог оксида дипол одређује следећа својства: високу топлотну проводљивост и топлотни капацитет, који се може пратити у брзом загревању и дугом хлађењу супстанце, способности да се оријентише око јона и појединачних електрона, једињења. То чини воду универзалним растварачем (и поларним и неутралним).
- Састав воде и структура молекула објашњавају способност овог једињења да формира вишеструке водикове везе, укључујући и друга једињења која имају усамљене електронске парове (амонијак, алкохол и др.).
- Тачка кључања течне воде је 100 ° Ц, долази до кристализације на + 4 ° Ц. Лед је испод овог индикатора. Ако повећате притисак, онда тачку кључања воде драматично повећати. Тако се код високих атмосфера у њему може растопити олово, али истовремено не прокухава (изнад 300 ° Ц).
- Карактеристике воде су веома значајне за жива бића. На пример, једна од најважнијих је површинска напетост. То је формирање најтањег заштитног филма на површини водиковог оксида. Ради се о води у течном стању. Врло је тешко разбити овај филм механичким дјеловањем. Научници су утврдили да је потребна сила од 100 тона. Како је приметити? Филм је видљив када вода капље из славине полако. Може се видети да је као да је у некој врсти љуске, која се протеже до одређене границе и тежине и излази у облику кружне капљице, благо искривљене гравитацијом. Због површинског напона, многи предмети могу бити на површини воде. Инсекти са посебним уређајима могу слободно да се крећу по њему.
- Вода и њене особине су абнормалне и јединствене. По органолептичким карактеристикама ово једињење је безбојна течност без укуса и мириса. Оно што називамо укусом воде су минерали растворени у њој и друге компоненте.
- Проводљивост водиковог оксида у течном стању зависи од тога колико и које соли се у њему растварају. Дестилирана вода не садржи никакве нечистоће електрична струја не држи.
Лед је посебно стање воде. У структури овог стања, његови молекули су међусобно повезани водиковим везама и формирају предивну кристалну решетку. Али то је прилично нестабилно и лако се може разбити, растопити, односно деформирати. Између молекула, сачуване су многе шупљине, чије димензије прелазе величину самих честица. Због тога је густина леда мања од густине воденог оксида.
Ad

То је од велике важности за ријеке, језера и остала слатководна тијела. Заиста, у зимском периоду, вода у њима се не замрзава у потпуности, већ се само покрива густом корицом лакшег леда која плута. Ако ово својство није било карактеристично за чврсто стање водиковог оксида, резервоари би се замрзнули. Живот под водом био би немогућ.
Поред тога, чврсто стање воде је од великог значаја као извор велике количине свеже питке воде. Ово су глечери.
Посебно својство воде може се назвати феноменом троструке тачке. Ово је стање у којем лед, пара и течност могу постојати истовремено. Ово захтева услове као што су:
- високи притисак - 610 Па;
- температура 0,01 ° Ц.
Индекс транспарентности воде варира у зависности од нечистоћа. Течност може бити потпуно прозирна, опалесцентна, мутна. Валови жуте и црвене боје су апсорбовани, љубичасте зраке продиру дубоко.

Хемијска својства
Вода и њена својства су важно средство у разумијевању многих животних процеса. Дакле, они се добро проучавају. Дакле, хидрохемија је заинтересована за воду и њена хемијска својства. Међу њима су:
Ad
- Крутост То је својство које се објашњава присуством соли калцијума и магнезијума, њихових иона у раствору. Подељен је на константу (соли наведених метала: хлориди, сулфати, сулфити, нитрати), привремени (бикарбонати), који се елиминише кључањем. У Русији, вода је омекшана пре употребе хемијским средствима за бољи квалитет.
- Минерализација. Својство засновано на диполном моменту водиковог оксида. Захваљујући свом присуству, молекули су у могућности да припоје на себе многе друге супстанце, јоне и задрже их. Тако настају сарадници, клатрати и друга удружења.
- Редок својства. Као универзални растварач, катализатор, сарадник, вода је у стању да ступа у интеракцију са многим једноставним и комплексним једињењима. Код неких, он делује као оксидациони агенс, док други - обрнуто. Како реагенс за редукцију реагује са халогенима, солима, неким мање активним металима, са многим органска материја. Најновије трансформације проучавају органску хемију. Вода и њена својства, посебно хемијска, показују колико је свестрана и јединствена. Као оксидациони агенс, он реагује са активним металима, неким бинарним солима, многим органским једињењима, угљеником, метаном. Генерално, хемијске реакције које укључују ову супстанцу захтевају избор одређених услова. Од њих ће зависити исход реакције.
- Биохемијске особине. Вода је саставни део свих биохемијских процеса у телу, као растварач, катализатор и медијум.
- Интеракција са гасовима са формирањем клатрата. Редовна течна вода може апсорбовати чак и неактивне хемијске гасове и лоцирати их унутар шупљина између молекула унутрашње структуре. Таква једињења се називају клатрати.
- Код многих метала, водонични оксид формира кристалне хидрате, у којима је уграђен непромењен. На пример, бакар сулфат (ЦуСО4 * 5Х2О), као и уобичајени хидрати (НаОХ * Х20 и други).
- За воду су карактеристичне реакције једињења у којима настаје формирање нових класа супстанци (киселина, база, база). Они нису редокс.
- Електролиза. Под дејством електричне струје, молекул се разлаже на сложене гасове - водоник и кисеоник. Један од начина да их добијете у лабораторији и индустрији.
Са становишта Левисове теорије, вода је слаба киселина и слаба база у исто вријеме (амфолит). То јест, можемо рећи за неку врсту амфотерних у хемијским својствима.
Ad

Вода и њена корисна својства за жива бића
Тешко је прецијенити значај који водиков оксид има за сва жива бића. На крају крајева, вода је сам извор живота. Познато је да без ње особа није могла да живи недељу дана. Вода, њена својства и вриједност су једноставно колосални.
- То је универзално, то јест, способно да раствори и органска и неорганска једињења, растварач који делује у живим системима. Зато је вода извор и медиј за проток свих каталитичких биохемијских трансформација, са формирањем комплексних виталних комплексних једињења.
- Способност формирања водикових веза чини ову супстанцу универзалном у одржавању температуре без промјене агрегатног стања. Ако то није био случај, онда би се при најмањем паду степена претворио у лед у живим бићима, узрокујући смрт станице.
- За људе, вода је извор свих основних кућних потрепштина и потреба: кухање, прање, чишћење, купање, купање и пливање итд.
- Индустријска постројења (хемијска, текстилна, машинска, прехрамбена, рафинерија нафте и др.) Не би могла да обављају свој посао без учешћа водоничног оксида.
- Од давнина се сматрало да је вода извор здравља. Коришћен је и данас се користи као терапеутска супстанца.
- Биљке га користе као главни извор исхране, због чега производе кисеоник - гас кроз који живот постоји на нашој планети.
Постоји још десетина разлога зашто је вода најраспрострањенија, важна и неопходна супстанца за све живе и вештачки створене објекте. Донели смо само најочигледније, главне.

Хидролошки циклус воде
Другим ријечима, то је његова циркулација у природи. Веома важан процес који вам омогућава да непрекидно надопуњавате нестале залихе воде. Како иде?
Главни учесници су три: подземне воде (или подземне воде), површинске воде и океани. Кондензација атмосфере и изузетне падавине су такође важни. Такође активни учесници у процесу су биљке (углавном дрвеће) које могу апсорбовати велику количину воде дневно.
Дакле, процес је следећи. Подземне воде испуњавају подземне капиларе и јата на површину и на Светски океан. Тада биљке апсорбују површинске воде и транспортују се у околину. Испаравање се јавља и из огромних подручја океана, мора, ријека, језера и других водених тијела. Једном у атмосфери, шта вода ради? Кондензовао и просуо се као оборина (киша, снег, град).
Да се ти процеси нису десили, резерве воде, посебно слатке воде, дуго би се истекле. Зато људи посвећују велику пажњу заштити и нормалном хидролошком циклусу.
Појам тешке воде
У природи, водонични оксид постоји као мешавина изотополога. То је због чињенице да водоник формира три типа изотопа: протуј 1 Н, деутеријум 2 Н, трицијум 3 Н. Кисеоник, такође, не заостаје и формира три стабилне форме: 16 О, 17 О, 18 О. ово није само уобичајена вода пропијума састав Х20 (1Х и 16О), већ и деутеријум и тритијум.

У исто време, деутеријум ( 2 Н) је стабилан у структури и облику, који је укључен у готово све природне воде, али у малим количинама. То се зове тешка. Нешто се разликује од уобичајеног или лаког за све показатеље.
Тешка вода и њена својства карактерише неколико тачака.
- Кристализује се на температури од 3.82 ° Ц.
- Врелиште је посматрано на 101.42 ° Ц.
- Густина је 1.1059 г / цм3.
- Као растварач неколико пута лошији од лаке воде.
- Има хемијску формулу Д 2 О.
Када су спроводили експерименте који показују ефекат такве воде на живе системе, установљено је да у њему могу живети само одређени типови бактерија. Требало је времена да се колоније прилагоде и аклиматизују. Али, прилагодивши се, потпуно су обновили све виталне функције (репродукцију, исхрану). Поред тога, челик је веома отпоран на зрачење. Експерименти на жабама и рибама нису дали позитиван резултат.
Савремена поља примене деутеријума и тешке воде која се њиме формира су атомска и нуклеарна енергија. У лабораторијским условима таква вода се може добити обичном електролизом - формира се као нуспродукт. Сам деутеријум се формира поновљеном дестилацијом водоника у посебним уређајима. Његова примена се заснива на способности успоравања синтезе неутрона и протонских реакција. Управо изотопи тешке воде и водоника су основа за стварање нуклеарне и хидрогенске бомбе.
Експерименти о употреби деутеријске воде од стране људи у малим количинама показали су да се не задржавају дуго - комплетан закључак је примећен након две недеље. Користити га као извор влаге за живот је немогуће, али техничка вриједност је једноставно огромна.
Отопити воду и њену примјену
Особине такве воде од давнина су људи дефинисали као исцељење. Одавно је примећено да када се снег отопи, животиње покушавају да пију воду из формираних локви. Касније су њена структура и биолошки ефекти на људско тело темељито истражени.

Растопљена вода, њени знаци и својства су у средини између нормалног светла и леда. Изнутра се формирају не само молекулама, већ и скупом кластера формираних од кристала и гаса. То значи да су водоник и кисеоник унутар шупљина између структурних делова кристала. Генерално, структура талине воде је слична структури леда - структура је сачувана. Физичка својства таквог оксида водоника се мало разликују у поређењу са уобичајеним. Међутим, биолошки ефекти на тело су одлични.
Када се прва фракција замрзне, тежи део се претвара у лед - то су изотопи, соли и нечистоће деутеријума. Због тога, ово језгро треба уклонити. Али остало је чиста, структурирана и здрава вода. Какав је ефекат на тело? Следећи типови побољшања су именовани од стране научника из Истраживачког института у Доњецку:
- Убрзање процеса опоравка.
- Јачање имунитета.
- Код деце, након удисања са таквом водом, долази до опоравка и излечења прехладе, кашља, ринитиса и тако даље.
- Побољшано дисање, ларингеалне и мукозне мембране.
- Општа добробит особе, активност се повећава.
Данас постоји велики број присталица третмана топљеном водом, који пишу своје позитивне критике. Међутим, постоје научници, укључујући и лекаре, који не подржавају ове ставове. Они вјерују да таква вода неће бити штетна, али има мало користи.
Повер индустри
Зашто се својства воде могу промијенити и опоравити када се крећу у различита агрегатна стања? Одговор на ово питање је следећи: ова веза има сопствену меморију информација, која бележи све промене и доводи до обнове структуре и својстава у право време. Биоенергетско поље, кроз које пролази дио воде (оно које долази из свемира), носи снажан набој енергије. Овај образац се често користи у третману. Међутим, са медицинске тачке гледишта, не свака вода може имати благотворан ефекат, укључујући информативну.
Структурирана вода - шта је то?
То је таква вода, која има мало другачију структуру молекула, локацију кристалних решетки (као што се види у леду), али је и даље течна (отапање се односи и на овај тип). У овом случају, састав воде и њена својства нису знанствено различити од оних који су типични за обичан водиков оксид. Стога структурирана вода не може имати тако широк терапеутски ефекат који се приписује њеним езотеричарима и заговорницима алтернативне медицине.