Шта је баријум сулфат? Како добити баријум сулфат?
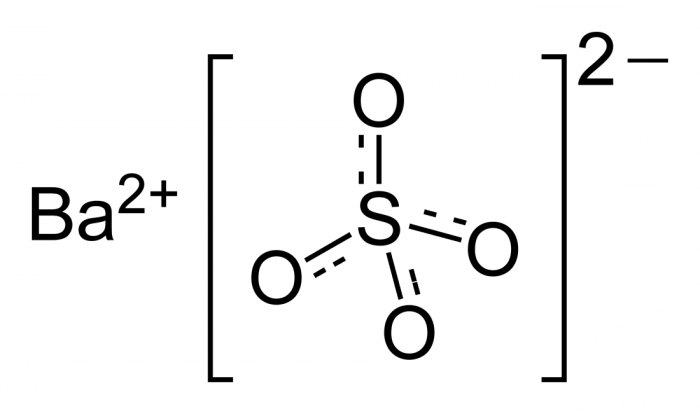
Баријум сулфат је неорганска супстанца са хемијском формулом БаСО 4 . То је бели прах, без мириса, нерастворљив у води. Његова белина и непрозирност, као и велика густина одређују главне области примене.
Титле хистори
Баријум се односи на земноалкалне метале. Потоњи се тако називају зато што, према Д.И. Менделејеву, њихова једињења формирају нерастворну масу Земље, а оксиди "имају земљани изглед". Баријум се природно налази у облику минерала барита, који је баријум сулфат са различитим нечистоћама.
Први пут су га открили шведски хемичари Сцхееле и Ган 1774. године као дио такозваног тешког спара. Отуда и име минерала (од грчког. "Барис" - тежак), а затим и сам метал, када га је 1808. године изоловао у свом чистом облику Хумпхри Деви.
Ad
Пхисицал пропертиес
Пошто је БаСО 4 сол сумпорне киселине, њена физичка својства су делимично одређена самим металом, који је мекан, хемијски активан и сребрно беле боје. Природни барит је безбојан (понекад бијели) и прозиран. Хемијски чист БаСО 4 има боју од беле до бледо жуте боје, није запаљив, са тачком топљења од 1580 ° Ц.

Колика је маса баријум сулфата? Његова моларна маса је 233,43 г / мол. Има неуобичајено високу специфичну тежину - од 4,25 до 4,50 г / цм3. Имајући у виду нерастворљивост у води, висока густина га чини неопходним као пунило за флуиде за бушење воде.
Хемијска својства
БаСО 4 је један од најрјеђих растварача у води. Може се добити из две високо растворне соли. Узети водени раствор натријум сулфата - На2С04. Његов молекул у води дисоцира на три иона: два На + и један СО 4 2- .
Ad
На 2 СО 4 → 2На + + СО 4 2- 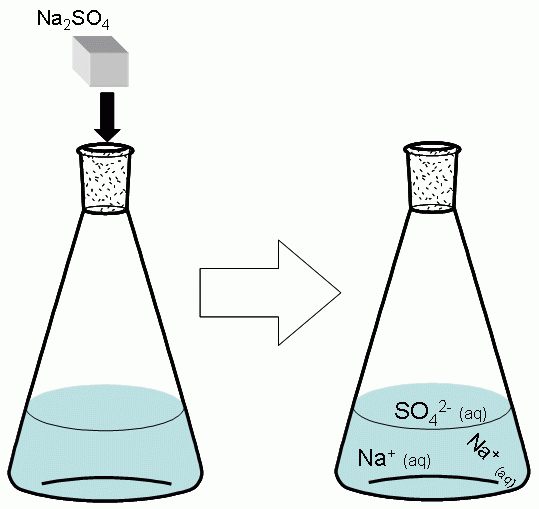
Узети и водени раствор баријум хлорида - БаЦл 2 , чији молекул дисоцира на три јона: један Ба 2+ и два Цл - .
БаЦл 2 → Ба 2+ + 2Цл -
Мешати водени раствор сулфата и смешу која садржи хлорид. Баријум сулфат се формира као резултат комбиновања у један молекул два јона истог магнитуде и супротног сигнала.
Ба 2+ + СО 4 2- → БаСО 4
Испод можете видјети потпуну једнаџбу ове реакције (тзв. Молекуларну).
На2С04 + БаЦл 2 → 2НаЦл + БаСО 4 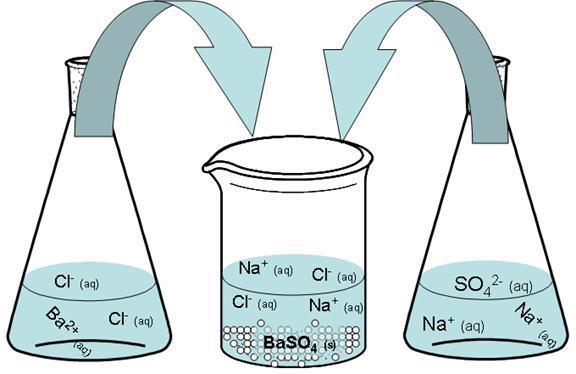
Резултат је нерастворљив преципитат баријум сулфата.
Цоммодити Барите
У пракси, сировина за добијање тржишног баријум сулфата, намењена за употребу у бушотинама за бушење нафтних и гасних бушотина, је, по правилу, минерални барит.
Термин "примарни" барит се односи на робне производе, који укључују сировине (добијене од рудника и каменолома), као и једноставне производе за обогаћивање методама као што су прање, седиментација, сепарација у тешким медијима, флотација. Већи дио сировог барита захтијева његово довођење на минималну чистоћу и густоћу. Минерални материјал који се користи као пунило је дробљен и просејан до уједначене величине тако да најмање 97% његових честица има величину до 75 микрона, а не више од 30% мање од 6 микрона. Примарни барит треба такође да буде довољно густ, тако да његова специфична тежина буде 4,2 г / цм 3 или више, али истовремено довољно мекана да не би оштетила лежајеве.
Ad
Припрема хемијски чистог производа
Минерални барит је често контаминиран разним нечистоћама, углавном жељезним оксидима, који га боје у различитим бојама. Прерађује се карботермном методом (загријавање коксом). Резултат је баријум сулфид.
БаСО 4 + 4 С → БаС + 4 СО
Ово друго, за разлику од сулфата, је растворљиво у води и лако реагује са кисеоником, халогенима и киселинама.
БаС + Х2СО4 → БаС04 + Х2С
Да бисте добили производ високе чистоће, користите сумпорна киселина. Баријум сулфат, који се формира овим процесом, често се назива бланфикс, који на француском значи "бела фиксирана". Често се налази у потрошачким производима, као што су боје.

У лабораторијским условима, баријум сулфат се формира комбиновањем баријумових јона и сулфатних јона у раствору (види горе). Пошто је сулфат најмање токсична баријева со због нерастворљивости, отпад који садржи његове друге соли се понекад третира натријум сулфат да вежемо сав баријум, који је прилично токсичан.
Од сулфата до хидроксида и назад
Историјски, барит се користи за производњу баријум хидроксида Ба (ОХ) 2 , који је потребан за рафинирање шећера. То је генерално веома интересантно и широко коришћено једињење у индустрији. Лако се раствара у води, формира раствор познат као баритна вода. Погодно је користити за везивање сулфатних јона у различитим композицијама формирањем нерастворног БаСО4.
Ad
Видели смо горе да када се загрева у присуству кокса из сулфата, лако се добија водорастворни баријум сулфид - БаС. Овај, у контакту са топлом водом, формира хидроксид.
БаС + 2Х2О → Ба (ОХ) 2 + Х2С
Баријум хидроксид и натријум сулфат, узети у раствору, када се помешају, дају нерастворљив преципитат баријум сулфата и каустични натријум.
Ба (ОХ) 2 + На2С04 = БаС04 + 2НаОХ

Показало се да се природни баријум сулфат (барит) прво индустријским методама претвара у баријум хидроксид, а затим служи за добијање истог сулфата приликом чишћења различитих система соли од сулфатних јона. На исти начин, реакција ће се одвијати при чишћењу од СО 4 иона - раствора бакар сулфата. Ако направите мешавину баријум хидроксида + бакар сулфата, резултат је бакар хидроксид и нерастворни баријум сулфат.
ЦуСО 4 + Ба (ОХ) 2 → Цу (ОХ) 2 + БаСО 4 ↓
Чак иу реакцији са самом сумпорном киселином, његови сулфатни јони ће бити потпуно везани баријумом.
Користи се у исплаци
Око 80% глобалне производње бариј сулфата, пречишћеног и брушеног барита се троши као компонента бушотинских флуида у стварању нафтних и гасних бушотина. Додатак повећава густину течности убризганог у бунар, са циљем боље отпорности на високи формацијски притисак и спречавање пробијања.
Када се бунар избуши, бит пролази кроз другачију формацију, од којих свака има своје карактеристике. Што је већа дубина, већи постотак барита мора бити присутан у структури отопине. Додатна предност је што је баријум сулфат немагнетна супстанца, тако да не омета различита мерења у бунару са електронским уређајима.
Ad
Индустрија боје и папира
Већина синтетичких БаСО 4 се користи као компонента белог пигмента за боје. Тако се бланц фиксиран у смеши са титанијум диоксидом (ТиО 2 ) продаје као бела уљана боја која се користи у сликарству.
Комбинација БаСО 4 и ЗнС (цинков сулфид) производи неоргански пигмент назван литопон. Користи се као премаз за одређене врсте фотографског папира.
У скорије време, баријум сулфат се користи за осветљавање папира дизајнираног за инкјет штампаче.
Примена у хемијској индустрији и обојеној металургији
У производњи полипропилена и полистирена БаСО 4 користи се као пунило у пропорцији до 70%. Има ефекат повећања отпорности пластике на киселине и базе, а такође им даје и непрозирност.
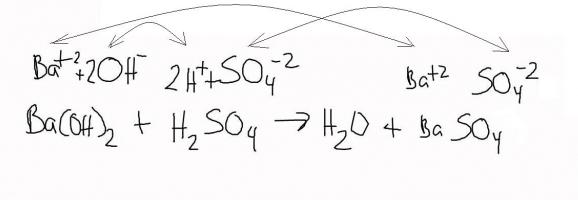
Користи се и за производњу других спојева баријума, посебно карбоната, који се користи за производњу ЛЕД стакла за телевизијске и рачунарске екране (историјски у катодним цевима).
Калупи који се користе у металном ливењу често премазују баријум са сулфатом да би се спречило приањање на растопљени метал. То се ради у производњи анодних бакарних плоча. Они се бацају у бакрене калупе обложене слојем баријум сулфата. Када се течни бакар очврсне као готова анодна плоча, може се лако уклонити из калупа.
Пиротехнички уређаји
Пошто спојеви баријума испаљују зелено светло када се запале, соли ове супстанце често користе пиротехничке формуле. Иако су нитрат и хлорат чешћи од сулфата, овај последњи се нашироко користи као компонента пиротехничких стробоскопа.
Радиоцонтраст медицатион
Баријум сулфат је радиопакуе агент који се користи за дијагностицирање одређених медицинских проблема. Пошто су такве материје непрозирне к зраке (блокирајте их као резултат њихове високе густине), онда се делови тела у којима су локализовани појављују као беле мрље на рендгенском филму. Ово ствара потребну разлику између једног (дијагностичког) органа и других (околних) ткива. Контраст ће помоћи доктору да види било које посебне услове који могу постојати у овом органу или делу тела.

Баријум сулфат се узима уста или ректално са клистиром. У првом случају, једињење једњака, желуца или танког црева чини непрозирним за рендген. Тако се могу фотографисати. Ако се супстанца примењује помоћу клистира, тада се може видети и фиксирати црево или црево помоћу рендгенских снимака.
Доза баријум сулфата ће бити различита за различите пацијенте, све зависи од врсте теста. Лијек је доступан у облику специјалне медицинске баријеве суспензије или таблета. Различити тестови који захтевају контраст и рендгенску опрему захтевају различите количине суспензије (у неким случајевима, неопходно је узети лек у облику таблета). Контраст треба користити само под директним надзором лекара.