Колоидна раствора: методе припреме и употребе
Многи људи који се не баве хемијом, слушајући фразу "колоидна рјешења", представљају нешто попут гела, вискозне смјесе. Чињеница је да је у почетку ово име настало од грчке речи, преведено као "лепљиво". Када балансни систем није уравнотежен, сол се преципитира, налик на желе.
У правилу, колоидни раствори су апсолутно транспарентна течност. У зависности од композиције, он може бити безбојан или обојен. На први поглед, сол се не разликује од истинских решења. Проучавање ове врсте супстанце се бави читавом секцијом - колоидном хемијом.

Опште карактеристике
Свако решење је једнофазни систем који садржи две или више компоненти. Насупрот томе, суспензија или емулзија су мање стабилне. У течним растворима током складиштења може да се таложи ако се, на пример, ставе у непропусно затворену посуду и испари течност. У другим случајевима, то је инертан систем где компоненте не реагују једна са другом, и стога може остати непромењен дуже време.
Ad
Својства колоидних раствора

Молекули супстанце су равномерно распоређени по растварачу, али константно праве Бровновско (осцилаторно) кретање. Као резултат тога долази до потпуног мешања компоненти система. Својства колоидних отопина у овом процесу су мало другачија. Честице таквог система називају се мицеле. Они споро дифундирају из једног слоја течности у други (100 пута). Разлог за ниску брзину је већа количина мицела у поређењу са молекулима правих раствора.
У зависности од величине честица, њихових количина, колоидни раствори се разликују по вискозности. Често постоје системи који улазе у гел стање са смањењем температуре. Присуство превеликих мицела и прекорачење границе растворљивости доводи до замућења.
Ad
Колоидне честице, за разлику од молекула, имају веће величине и стога могу да распрше светлост. Дакле, могуће је разликовати ова рјешења од истинитих. Када пролазите кроз такав систем, зраке ће бити видљиве.
Мицелле струцтуре
Припрема колоидних раствора заснива се на формирању мицела, које морају остати да очувају својства система у стабилном стању. Честица има комплексну структуру, састоји се од нуклеуса, који је формиран од стране мало растворне супстанце. Слој потенцијално-одредујућих јона је расподељен око њега. Обично су исте као у слабо растворљивој супстанци која се налази у центру мицеле (Панетх - Фаиенце правило). Такви иони одређују наелектрисање језгра.
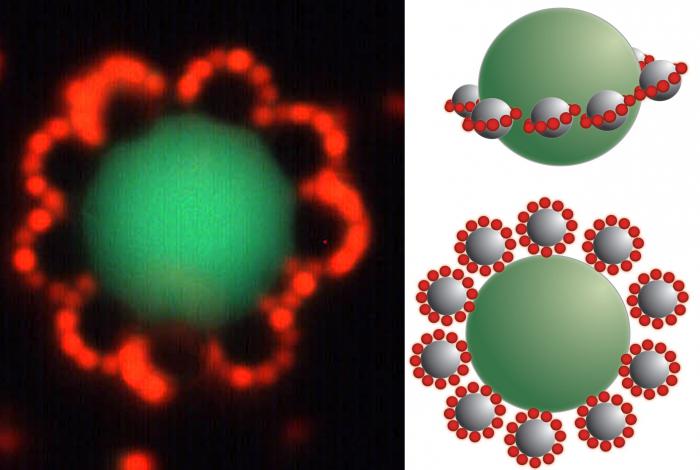
На пример, у интеракцији калијум јодида и сребрни нитрат формирају се мицеле. Језгро таквих честица је сребрни јодид (АгИ). Ако преовладава друга компонента, тада јони који одређују потенцијал ће бити Аг + , ако је први И - . Следећи слој је противион за супстанцу која је узета у вишку. Они формирају две зоне. Први се налази близу површине језгра, дио је адсорбованог слоја. Друга је дио дифузијског слоја, састоји се од иона који се слободно крећу близу површине.
Ad
Колоидна честица је нуклеус са адсорбованим слојем који укључује јоне који одређују потенцијал и контраионе. Ова формација има наплату. Микеле укључују колоидну честицу и дифузиони слој контра-јона и неутралан је.
Како настаје мицела
Било која метода добијања колоидних раствора заснива се на интеракцији слабо растворних једињења са електролитом. На пример, АгНО 3 (сребрни нитрат) са КИ (калијум јодид). Као резултат реакције, добијају се АгИ и КНО3 (калијум нитрат). Структура мицеле се може схематски приказати. Постоје 2 опције за формирање колоидних честица горе наведених једињења:
- Са вишком АгНО 3 - {н (АгИ) мАг + (мк) НО 3 ¯} кНО 3 ¯.
- Са сувишком КИ - {н (АгИ) мпи (мк) К + } кК + .
Прво, указано је на нуклеус, затим на потенцијално детерминисане јоне и контраионе адсорбованог и дифузионог слоја. Електрокинетички потенцијал, који одређује набој колоидне честице, означен је словом "к". Настаје услед разлике у површинској енергији језгра честице са потенцијалним јонима.
Стабилност

Колоидни раствори могу да остану непромењени дуго времена. Стабилност таквих система је посљедица истоименог мицелног набоја који доводи до њиховог одбијања један од другог. Међутим, са превеликим величинама и великом концентрацијом, честице се могу сударити и спојити. Стабилност колоидних раствора је релативни појам. Могу се довољно дуго чувати непромијењени.
Ad
Коагулација колоидних раствора је процес лепљења мицела једна на другу. Са стабилним стањем система, овај феномен се одвија полако, што му омогућава да дуго траје (до 100 година) у једнофазном стању. Овај феномен се назива агрегативна нестабилност.
Стопа коагулације
Брзина агрегације честица и као резултат тога раздвајање фаза зависи од многих фактора, укључујући величину и концентрацију мицела, температуру складиштења. Убрзање процеса коагулације резултат је додавања електролита. Овај феномен се уочава у хидрофилним системима. Познати начини успоравања процеса агрегације честица. На пример, мешање липофилног колоида са хидрофилним. На губитак стабилности сола може утицати загревање или хлађење, механичко напрезање.
Коагулација колоидних раствора помоћу електролита
Постоје одређени обрасци утицаја електролита на колоидни раствор. Дакле, да бисте започели процес, потребна вам је одређена концентрација, а не испод одређеног нивоа - праг коагулације. Електролит је супстанца која је способна за провођење електрична струја као резултат дисоцијације у раствору или топљења у јоне. Стање колоидног раствора је под утицајем иона, чија је набоја супротна од оне у мицели. Радња је појачана степеном набоја (Сцхулзе-Гарди правило).
Други фактор који одређује степен утицаја јона је њихова хидрабилност. Честице са истим набојем имају различит ниво деловања на процес коагулације. Код одвајања колоидног раствора, коагулациони јони су присутни у седименту. Када се додаје мешавина електролита, њене компоненте могу ослабити ефекте једних на друге (антагонизам) или, обрнуто, појачати (синергизам). Ретко посматран независан (адитивни) ефекат.
Ad
Начини да дођете

Методе за добијање колоидних раствора су редуковане на два. Једна опција је дисперзија (мљевење) великих честица до величина које одговарају колоидном. Такав процес се може извести, на пример, коришћењем ултразвучних уређаја (механичко брушење). Мноштво дисперзних метода је формирање колоидних честица као резултат додавања електролита, који се адсорбују на површини колоидних језгара и преносе честице у отопљено стање.
Супротно дисперзионој методи је метода кондензације, која се састоји у агрегацији малих честица у веће. Овај феномен се јавља, на пример, приликом замене растварача. Како се овај ефекат може постићи? Дошло је до наглог смањења растворљивости услед промена у окружењу. Даље, супстанца формира колоидну честицу. Молекули растварача су укључени у његово формирање, са којим се боље мешају. Овај ефекат, на пример, постиже се постепеним додавањем колофонијума раствореног у етанолу у воду.
Различите реакције кондензације, укључујући оне описане горе, такође се примењују на методе агрегације. Други примери могу бити хидролиза соли метали, нарочито феро-хлорид (ФеЦл3), реакција неутрализације која је резултат интеракције баријум хидроксида (Ба (ОХ) 2 ) са сумпорном киселином (Х2С04).
Солубилизатион
Вредност колоидних раствора у људском животу је велика због способности сурфактаната да повећају растварање хидрофобних једињења у води. Овај феномен се назива "солубилизација". У својој сржи, овај процес представља растварање једињења у мицелама. Због ове појаве, прахови су способни да уклоне контаминацију из тканина, што резултира стабилним емулзијама угљоводоника и боја у води.
Солубилизација се може одвијати на различите начине. Дакле, неполарни угљоводоници продиру у језгро мицела, док су једињења са хидрофилним и хидрофобним деловима (амини, алкохоли) уграђена тако да је прва споља, а друга дубоко у колоидну честицу. Ту је и феномен реверзне солубилизације, која се састоји у отапању воде у уљима. У случају нејонских површински активних супстанци, идентификован је други метод повећања растворљивости хидрофобних једињења - везивање за површину мицеле кроз хемијске везе (посебно водоник).
Свеприсутна дистрибуција
Колоидна раствора су увек присутна унутар и око особе. То су крв, лимфа, љепила и боје које се често користе у различитим грађевинским и завршним радовима. Гелови се добијају из колоидних раствора као резултат коагулације и таложења. То укључује, на пример, желе, мармеладу, агар-агар, желатин, карагенане. Потоњи се користе за побољшање структуре производа, посебно пасте. Свуда у људском телу постоје колоидни раствори обогаћени протеинима.
Употреба у медицини

У медицини се свуда користе колоидни раствори. Ево неколико примера њихове употребе. Колоидно сребро, које је мала метална честица распршена у води, користи се у третману опекотина, чир на желуцу и дуоденум, за прање слузнице носа у циљу спречавања ширења вирусних инфекција.
Фармацеутска индустрија нуди велики избор колоидних раствора за различите сврхе. Међу њима су универзални лекови који се могу користити као зарастање рана за опекотине, хемороиде; антиинфламаторни - са прехладом, боловима у грлу, синуситисом; аналгетици - за ублажавање зубобоље и не само за то. Ово укључује миленијумско колоидно раствор. Гел садржи алое, протеин пшенице, гинсенг, витамин Е и друге корисне додатке. Многи фармацеутски производи за спољну употребу су у ствари колоидни раствори. За зглобове, на пример, користи се "Артро Цомплек", који садржи тако корисну компоненту као што је хрскавица ајкула.
Примена у животу и индустрији
Колоидни раствори чине основу за прање и чишћење сурфактаната. Контаминанти продиру кроз мицеле и тако се уклањају са површине.
Други важан аспект употребе површински активних средстава за формирање мицела је производња полимера, посебно латекса, поливинил алкохола и лепкова биљног порекла. Разне пластике, кожне замене се заснивају на емулзији. Сурфактанти се такође користе за чишћење канализација и воде за пиће.
Предности козметике на бази колоидних раствора су продирање активних супстанци кроз структуру људске коже и косе. Таква средства се ефикасно користе против старења. То укључује, посебно, Миленијумски Нео гел. Колоидни раствор помаже компонентама које се у њему налазе да досегну дубље слојеве коже, заобилазећи епидерму.