Метил алкохол: својства, припрема и употреба
Увод
Ви сте увече дошли с посла, пресвукли се, а затим, посматрајући вашу навику, сјели у столицу испред телевизора и укључили канал с вијестима у етеру. Спикер прво емитује нешто неразумљиво, а затим издаје нешто попут: "И коначно, главна вест дана. У таквом и таквом граду било је масовно тровање метил алкохолом. Неколико десетина људи је погинуло, јер је још много њих хоспитализовано." Ваш слух је одмах ухватио име непознате супстанце - "метил алкохол". Већина људи сазна за његово постојање на овај начин. Неки ће брзо заборавити ову фразу, а неки ће хтјети сазнати више о њој. Овде ћу им у овом чланку описати све особине метилног алкохола.
Ad
Дефиниција
Метил алкохол (формула ЦХ3ОХ) је најједноставнији монохидрични алкохол, први представља хомологну серију ових потоњих.
Име
Може се другачије назвати у различитим изворима: метил хидроксид, метанол, дрвени алкохол, карбинол и метил хидрат.
Производња метил алкохола
До шездесетих година двадесетог века за синтезу метилног алкохола коришћене су само цинк-хромне хемикалије, међутим, касније је ово искуство почело да се спроводи на катализаторима који садрже бакар. Али данас се добија каталитичком синтезом из угљен моноксида (ИИ) и водоника при температури од 250 ° Ц, притиску од 7 мегапаскала и одређених катализатора (цинков оксид и бакар оксид). Пре тога, метил алкохол је добијен сувом дестилацијом дрвета. Али данас је овај метод секундаран. У ту сврху могу се користити и отпад од прераде и угљен за коксирање.
Ad
Пропертиес 
Метанол је безбојна течност без мириса. етил алкохол. Вода, етанол и етар се могу мешати са њом у било којој вези. Компримује се и загрева када се помеша са водом. Он такође има репутацију снажног растварача и често може да замени етил алкохол. Ако је растворен у анхидрованом метанолу бакар сулфат, постаје плавичасто-зелена. Због тога се такав безводни витриол не може користити за отварање трагова воде у метил алкохолу. Метанол не може да формира азеотропну смешу са водом, због тога се смеше воде и метил алкохола могу раздвојити дестилацијом дестилацијом. Метанол се комбинује са многим солима да би се формирали солвати. Када реагује са каустичном алкалијом може дати алкохолате.
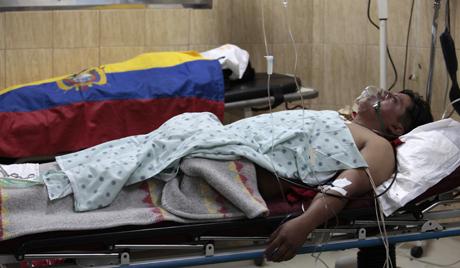 Метил алкохол: тровање
Метил алкохол: тровање
Метанол је најјачи отров, захваћен је његов нервни и кардиоваскуларни систем. Тровање је последица "смртоносне синтезе" - метаболичке оксидације у организму, чији је производ веома токсични формалдехид. До тешког тровања долази када се прогута 5-10 мл метилног алкохола, а ако је 30 или више грама, слепило и / или смрт су неизбежни. Симптоми благог тровања су главобоља, општа слабост, слабост, зимица, мучнина и повраћање. Због тога производи који угрожавају живот су чак и са најмањом концентрацијом метанола. Антидот за тровање овом супстанцом је етил алкохол. Примењује се интравенским или оралним путем. Међутим, то не би требало да радите сами - са погрешном дијагнозом и дозирањем, ситуација ће се само погоршати. Дакле, ако сумњате на тровање метил алкохолом, хитно је потребно позвати лекара.
Ad
Апплицатион 
У гасној индустрији, борба против формирања хидрата није потпуна без метилног алкохола. Са њом се производе формалдехид, формалин, сирћетна киселина и бројни естри. Метанол се користи у производњи растварача за лакове. Може послужити и као додатак течним горивима за моторе са унутрашњим сагоревањем и као гориво за мотоцикле и аутомобиле. Од метил алкохола добијате биодизел. Такође у парфимерији, он је денатурни адитив за етанол. Горивне ћелије раде само због оксидације метанола у угљен моноксид (Ив) на катализатору.
Закључак
Сада знате све о метил алкохолу. И, као што видите, упркос токсичности, може бити веома корисно за особу, само уз пажљиво руковање.