Хемијске и физичке особине арена
Има их органска једињења молекула који садрже мали број атома водоника, иако је њихов угљенични скелет прилично велик. Такве супстанце се сматрају високо незасићеним, међутим, оне не улазе у реакције карактеристичне за алкене или алкине. На пример, немојте да мењате боје. калијум перманганат или бромовом водом. Први хемичари из ове групе једињења били су супстанце са пријатним мирисом, тако да су се називале ароматичним. Постоји још једно име - арене. Номенклатуру, изомерију, добијање и њихове физичке особине ћемо проучити у овом чланку.

Шта је бензол
Најједноставнији представник арена је бензен. Молекуларна формула супстанце - Ц6Х6. Између осталих ароматски угљоводоници То је од највеће практичне важности. Једињење је 1825. године открио енглески физичар М. Фарадаи у саставу светлећег гаса. То је безбојна течност, лакша од воде (густина 0,88 г / цм3). Има карактеристичан мирис, отрован. Тачка кључања - 80, замрзава на 5.5. Физичке особине арена, као и других органских супстанци, зависе не само од квалитативног и квантитативног састава, већ и од структуре њихових молекула.
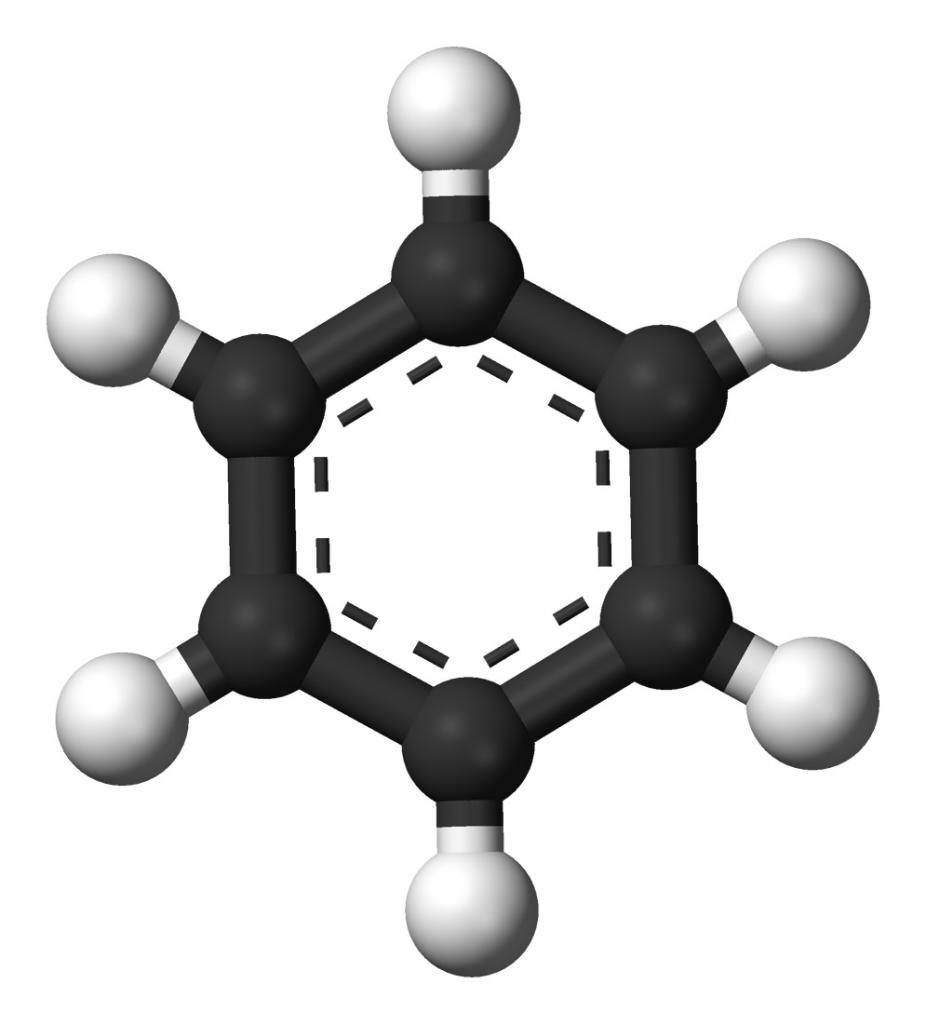
Загрљај ароматичног језгра
Прву структурну формулу супстанце предложио је њемачки кемичар Кекуле. У њему, атоми угљеника леже у истој равни и формирају правилан шестерокут између њих. Честице угљеника у молекулу повезане су два типа ковалентне везе: Међутим, експерименти нису потврдили присуство пи-веза у бензену, јер супстанца није оксидисана раствором брома и калијум перманганата. Објашњење ове контрадикције је електронска структура материје. У његовом молекулу постоји посебан тип хемијске везе, назван ароматичан или пола. Он је представљен заједничким електронским облаком који се састоји од шест међусобно преклапајућих п-електрона. Смештена изнад и испод равни молекула, веза има облик прстена и назива се ароматично језгро. Једна и пол веза одређује физичке особине арена, као и њихову способност супституције и реакције додавања.
Механизам процеса замене
Систем ароматичног језгра има повећану електронску густину и може бити изложен нападима електрофилних честица са дефицитом негативних набоја. Резултат таквог ефекта ће бити замена атома водоника другим честицама, на пример, у молекулу бензена. Физичке особине арена и посебности хемијских процеса су веома различите од оних алкана или алкена. Штавише, за разлику од других класа органских једињења, арене се не могу описати једном општом формулом. Дакле, за нафтален, формула ће бити следећа: Ц н Х 2 н -12 , за бензен –Ц н Х 2 н -6 , за дифенил - Ц н Х 2 н -14.
Хлорисање, бромирање и нитрирање ароматичних угљоводоника одвија се једним механизмом електрофилне супституције, у којој групе хлора, брома или нитро имају улогу нападајућег електрофилног средства.
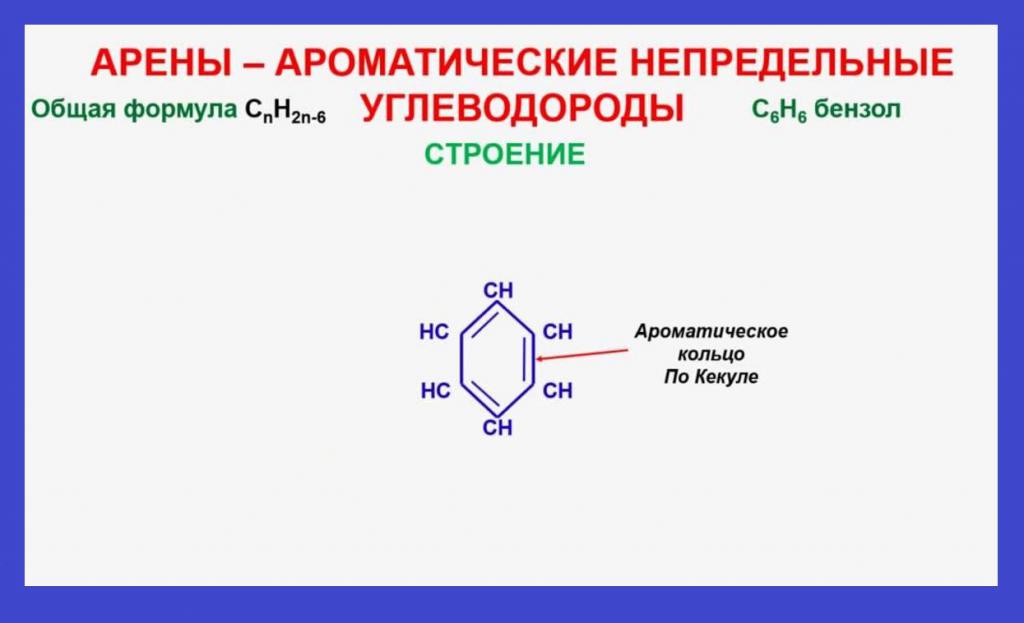
Зашто реакције додавања захтевају тешке услове?
Главна карактеристика структуре молекула ароматичног једињења је присуство у молекулима бензенског прстена, који се састоји од шест преклапајућих п-електрона. Од тога зависе главне хемијске карактеристике и физичке особине арена. Да би се прекинула комуникација од пола и пол потребна је додатна значајна количина енергије. Добија се применом следећих параметара: ултраљубичасто зрачење, висока температура и притисак у реакционој смеши, као и употреба катализатора. На пример, хлор се везује за бензен само када је озрачен ултравиолетном светлошћу, стварајући хексахлороциклохексан (хексахлоран). Користи се за дораду дрвета током његовог дуготрајног складиштења, као иу пољопривреди као средство за борбу против инсеката штеточина.

Ц6Х6 + 3Цл2 --- светло ---> Ц6Х6Цл6 - адиција
Алкилбензени
Ако су атоми водоника у молекулу бензена замењени угљоводоничним радикалима, на пример, метил-ЦХ3 или етил-Ц2Х5, тада добијени ароматски угљоводоници неће бити једноставна сума својстава алкана и арена. Физичка својства и хемијске реакције карактеристичне за ова једињења ће имати бројне разлике. Дакле, толуен и етилбензен су безбојне течности са осебујним мирисом, лакшим од воде и нерастворљивим у њему. Али супстанце су добро растворене у органским растварачима, на пример, ацетону или дихлорометану. И сами се могу користити као растварачи. Ароматски угљоводоници такође имају специфичне карактеристике. Површинска напетост, коефицијент дифузије, вискозност су физичка својства арена, укратко описујући њихове карактеристике као органски растварачи.
Ароматиц нитратион
Под дејством азотне киселине и у присуству сулфатне киселине као катализатора, арене се нитрирају. Реакција бензена са азотном смешом ће бити како следи.
Нитробензен је бледо жута уљаста течност са карактеристичним мирисом бадема. Користи се као растварач и служи као сировина за производњу анилина.
У реакцији азотне киселине са толуеном настаје експлозив - тринитротолуен или тротил. Као пирогени спојеви се користе и неки други. органска материја са бензенским језграма које садрже вишеструке везе у бочним ланцима.
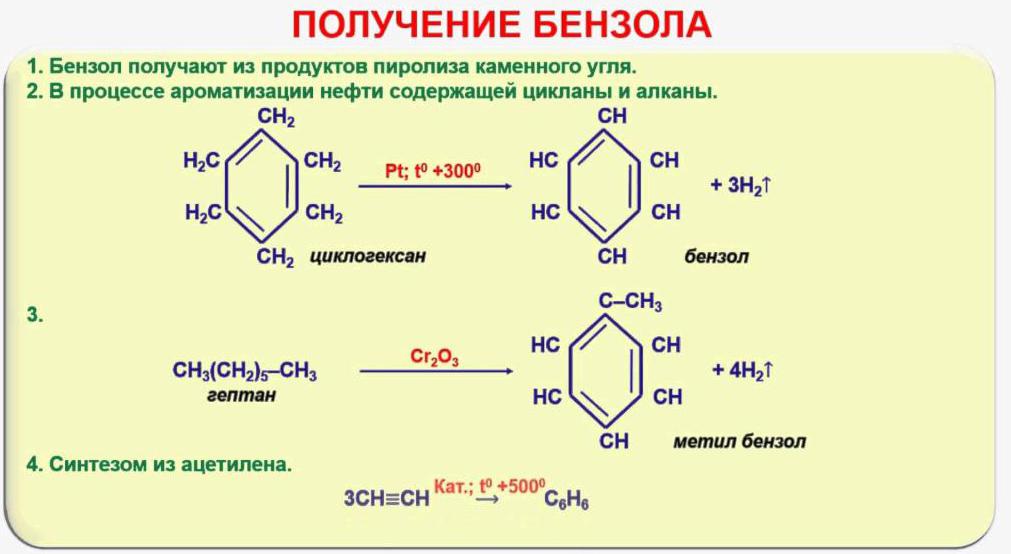
Добијање и примена арена
Физичке особине арена: високи топлотни капацитет, запаљивост, способност растварања других супстанци, широко се користе у различитим привредним секторима. Бензен, толуен, нафтален, антрацен и други ароматски угљоводоници добијају се из нафте или угљеног катрана насталог током коксирања угља. С обзиром на то да је потражња индустрије за аренама огромна, они се такођер копају методом каталитичке ароматизације угљиководика који су дио нафте и имају ацикличку структуру. У овом случају долази до реакције дехидрогенације - елиминације атома водоника, због чега се, на пример, бензен може добити из хексана. У хемији органске синтезе наставља се примена методе добијања бензена из ацетилена. Реакција се изводи загревањем етина на 600 ° Ц и назива се тримеризација. Хемијске и физичке особине арена користе хемија у процесу добијања пластике, лакова, боја.

Бензен се користи као додатак гориву. У пољопривреди, једињења - халогени деривати ароматичних угљоводоника, служе као инсектициди - средства за сузбијање инсеката. Нитро једињења, на пример, тринитротолуен, користе се у војној индустрији као експлозиви. Многе арене су добри растварачи.
У нашем чланку смо проучавали хемијске и физичке особине арена и идентификовали области примене ових једињења у индустрији.