Угљоводоници су једињења угљеника са водоником која не садрже друге елементе. Класификација угљоводоника
Шта су угљоводоници? Како су класификовани? Које значајке имају? Покушајмо заједно да нађемо одговоре на питања.
Угљоводоници су органска једињења који садрже водоник и угљеник. Сматрају се органским једињењима у основној хемији.
Класификација
У зависности од стања везе између угљеника главног ланца, уобичајено је поделити све Ц к Х и на неколико типова. Једињења угљеника са угљеником су карактеристична за засићене угљоводонике.
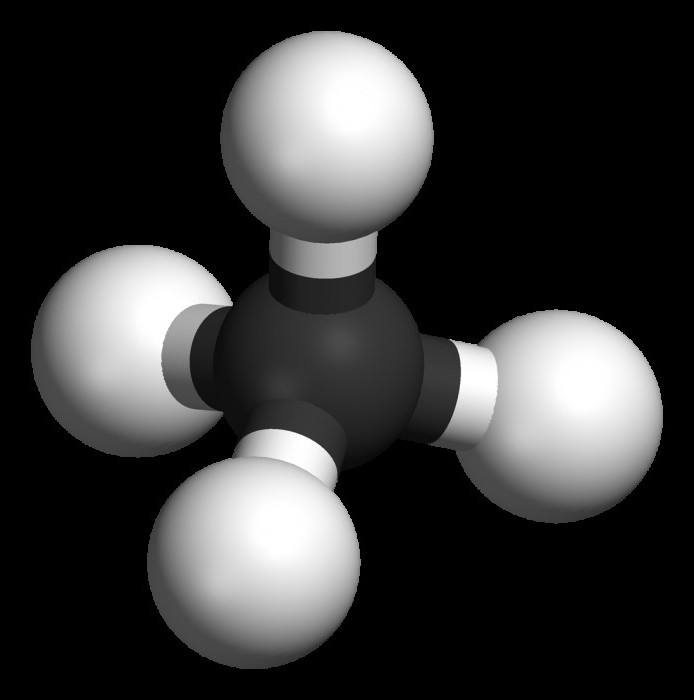
Алканес
Гранични угљоводоници су једињења опште формуле ЦнХ2н + 2 . Међу њиховим карактеристикама можемо навести одсуство затворене структуре, као и појединачне (једноставне) везе. Зову се ацикличка једињења у органској хемији.
Ad
Типичан представник ове класе је метан - ЦХ 4 . Он је тај који започиње хомологну серију алкана, поседује сва својства која су својствена другим представницима парафина.
Први представници ове класе угљоводоника су гасовити материјали са ниском растворљивошћу у води, специфичним мирисом.
Међу основним хемијским својствима које поседују представници хомологне серије алкана, издвајамо радикалну супституцију.
Халогенирање се одвија на повишеним температурама или у присуству ултраљубичастог зрачења. Реакција се одвија у неколико фаза, које карактерише постепена замена атома водоника са халогеном. Карактеристике угљоводоника одређеног броја метана објашњавају се засићењем везе између атома угљеника. Они нису у стању да уђу у реакције додавања, док добро сагоревају у кисеонику из ваздуха да формирају угљен-диоксид, водену пару и ослобађају довољно топлотне енергије.
Ad
Међу главним гранама примене представника ове класе угљоводоника издвајамо употребу као гориво, као и опцију сировина за производњу многих других органских једињења.
Алкенес
Незасићени угљоводоници су једињења која имају једну или више вишеструких (незасићених) веза између атома угљеника. Алкени имају општу формулу ЦнХ2н . Типичан представник ове класе је етилен.
Ови природни угљоводоници су део уља. С обзиром да молекул садржи двоструку везу, реакције адиције су карактеристичне за алкене. На пример, могу ући у халогенацију, хидратацију.
Ако се двострука веза налази у првом положају, на пример у бутену-1, додавање водоник халогенида и хидратација (реакција са водом) се одвија према Марковниковом правилу. Његова суштина је у томе што се током хидрохалогенације и хидратације водоник везује за атом угљеника који је максимално засићен њиме.
Хидроксилна група или халогени атом је везан за Ц атом који није засићен водоником. Квалитативна реакција на незасићеној (двострукој) вези је избељивање бромове воде или калијум перманганат.

Цицлоалканес
Такви угљоводоници су циклична једињења која су интеркласни изомери фор алкенес. Они имају општу формулу Ц н Х 2н , једноструке везе. С обзиром да се ова класа одликује затвореном структуром, оне улазе у реакције адиције, праћене уништењем затвореног циклуса, претварајући се у засићене алкане. Главни извори таквих једињења су природни и повезани гас, нафта. Упркос цикличној структури, у сп3 хибридизујућим молекулима, валентни угао је 109 ° 28 '.
Ad
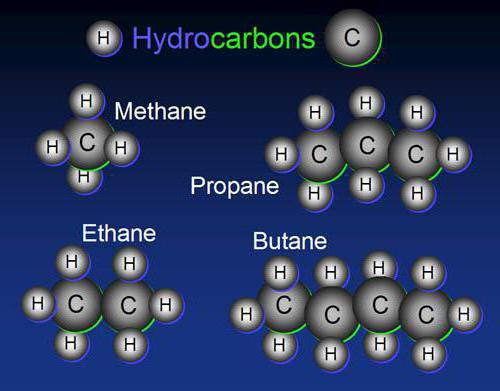
Алкадиенс
Шта још карактерише органска хемија? Угљоводоници ове класе имају општу формулу ЦпХ2н-2 . Сви представници диенских угљоводоника имају две двоструке везе. Незасићеност диена одређује њихове основне хемијске особине. Аналогно са алкенима, диенска једињења улазе у реакцију додавања.
Као они хемијске реакције које су карактеристичне за ова једињења, примећујемо полимеризацију. Почетни мономер у поступку је представник диена, а продукт интеракције је синтетичка гума. Када се сумпор додаје добијеном полимеру, јавља се вулканизација, праћена формирањем гуме.
Алкинес
За ова незасићена органска једињења карактеристична општа формула ЦнХ2н-2 , можемо приметити присуство троструке везе између атома угљеника. Ако се налази иза првог атома угљеника, квалитативна реакција на њено присуство је замена комплексним једињењем сребра.
Као и за алкене, диене, алкини се лако придружују трострукој вези. Карактерише их хидрогенација, хидрохалогенација, халогенација, реакције хидратације.

Ароматична једињења
Бензен је први представник ове класе. Она има општу формулу ЦнХ 2н-6 . За разлику од свих других угљоводоника, ово једињење има ароматични прстен. У њеном формирању учествују слободни електрони сваког атома угљеника. Три електрона Ц формирају хибридне облаке, а четврти електрон се не подвргава хибридизацији. Он формира ароматични прстен, који је равномерно распоређен по молекулу. Једнака дистрибуција прстена по структури објашњава њену хемијску стабилност. Бензен сам улази у замену и додавање само у тешким условима.
Ad
Толуен, који је његов хомолог, карактерише извесна промена у електронској густини, стога има већи капацитет за супституцију. Угљоводонични радикал је оријентант типа 1, долазећи супституенти (халоген, нитро група) заузимају орто, пара позиције.
Закључак
Без обзира на то који су елементи структуре различити представници угљиководика, они имају одређени број атома угљика и водика у свом саставу. Постоји одређена тенденција да се промене физичке особине Ц к Х и представника. Први представници било које класе имају гасовито стање, како се релативна молекуларна тежина повећава, посматра се систематска транзиција у течности, затим у чврстом облику.