Натријум ацетат (својства и употреба)
Ова хемијска супстанца је обично позната под називом „врући лед“. Заправо, натријум ацетат (Ц2Х3О2На) је вештачки кристал оних соли које су део сирћетне киселине. Ова супстанца је широко распрострањена у природи. То је део многих биљне ћелије и животињског порекла, тако да се натријум ацетат може наћи у многим воћама и јагодама. Такође, његово формирање се јавља током бактеријске ферментације, што доводи до његовог појављивања у ферментисаним млечним производима.
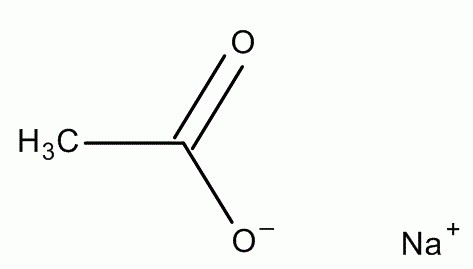
Цхемицал Пропертиес
Не без разлога, натријум ацетат је назван "врући лед", јер је веома топао у процесу егзотермне кристализације. Ова супстанца има кристалну структуру. Готово је безбојан и има благи мирис сирћетне киселине. Његови кристали имају карактеристичну особину: врло слабо се растварају у етру и алкохолу, али се током интеракције са водом врло брзо претварају у раствор натријум ацетата. Тако је 76 г ове супстанце растворено у 100 мл Х20. Натријум ацетат има низак ниво токсичности и није запаљив. Специфична топлота њеног топљења је 264-289 к, а температура разлагања: 324 ° Ц. Натријум ацетат, чија трихидрат има тачку топљења од 58 ° Ц, када се загрева на 100 ° Ц у посуди која се налази у кључалој води, раствара се у својој кристалној води (растопљена). Дакле, претвара се у рјешење. Када се охлади, присутна је засићеност ове супстанце у води. Такав раствор се изузетно охлади до температуре од 20-24 ° Ц без формирања његове чврсте фазе. Након клика на метал у посуди формира се центар за кристализацију. У процесу раста, овај раствор се трансформише у чврсту фазу натријум ацетат трихидрата. Овај процес прати значајну производњу топлоте (264-289 кЈ / кг).
Начини добијања натријум ацетата
 Ова супстанца се може добити, како у индустрији, тако иу лабораторији, и код куће. У великим количинама, натријум ацетат се производи сувом дестилацијом одређених врста дрвета. У лабораторијама, ова супстанца се добија у процесу интеракције сирћетне киселине са таквим натријумовим једињењима као карбонат, хидрокарбонат, хидроксид.
Ова супстанца се може добити, како у индустрији, тако иу лабораторији, и код куће. У великим количинама, натријум ацетат се производи сувом дестилацијом одређених врста дрвета. У лабораторијама, ова супстанца се добија у процесу интеракције сирћетне киселине са таквим натријумовим једињењима као карбонат, хидрокарбонат, хидроксид.
Како направити натријум ацетат код куће
 Чак и особа која је далеко од дубоког знања из области хемије може сам набавити ову супстанцу. За то су вам потребна само два елемента: сода за печење и сирћетна киселина. Једначина хемијске реакције при комбиновању ових производа има следећи облик:
Чак и особа која је далеко од дубоког знања из области хемије може сам набавити ову супстанцу. За то су вам потребна само два елемента: сода за печење и сирћетна киселина. Једначина хемијске реакције при комбиновању ових производа има следећи облик:
- НаХЦ03 + ЦХ3ЦООХ = ЦХ3ЦООНа + Х2ЦО3.
Другим речима, добијање ацетата код куће се зове "сода сода". Као резултат ове хемијске реакције, добија се нестабилно једињење које се одмах разлаже у воду и угљен диоксид. Током испаравања добијеног раствора, формира се кристални натријум ацетат. По правилу, да би се добила, сода и киселина се узимају у односима: 84 г натријум бикарбоната са 750 г сирћета (8%) или 86 г сирћетне есенције (70%). У овом другом случају испаравање није потребно. Као резултат реакције, добијено је око 80 г натријум ацетата.
Други називи натријум ацетат
Најчешће се за означавање ове супстанце користе следећи синоними: натријумова со сирћетне киселине, натријум ацетат, натријум етаноат.

Употреба натријум ацетата као додатка храни
Ова супстанца се користи у разним индустријама. Тако се у прехрамбеној индустрији користи као конзерванс под ознаком Е262. Данас производња неких прехрамбених производа није без ње. На тај начин се у брашно додаје натријум ацетат да би се заштитили пекарски производи од такозване "болести кромпира" узроковане бактеријом Бациллус месентерицус која ствара споре, а која је веома честа у природи. Производњом чипса користи се и овај адитив за давање пријатног укуса и мириса. Е262 се додаје и конзервираном поврћу, јер његово дјеловање на производе омекшава врло оштар окус оцтене киселине. Многи људи су веома опрезни због разних врста адитива у храни. У ствари, Е262 је због своје ниске токсичности одобрен за употребу у свим европским земљама. Руска Федерација такође није утврдила максималну дневну дозу натријум ацетата.
Употреба у медицини
Такође није неуобичајено користити ову супстанцу у медицинске сврхе. Доступан је као део многих лекова. Нарочито се може наћи у многим диуретским препаратима. Натријум ацетати се користе као алкализирајућа средства у матаболичкој ацидози и хипонатремији.
Употреба супстанце у другим индустријама

Поред горе наведених апликација, натријум ацетат се користи у текстилној индустрији и грађевинарству. Ова супстанца се користи за неутрализацију већ потрошених сумпорна киселина улазак у канализацију. Натријум ацетат се користи као фоторезист у обради тканина анилинске боје. Такође се користи у процесу штављења коже са хромовим солима (јеткање). Натријум ацетат током производње синтетичке гуме успорава сушење хлоропрена. Користи се као додатак антифризу за све врсте бетона у производњи монолитних конструкција. Ова супстанца се користи у производњи такозваних "хемијских" грејача и грејача. То је због његове способности да загрева до прилично високих температура. Натријум ацетат је главна компонента широко распрострањене мешавине која се зове "топли лед". Ова супстанца се такође користи у производњи анхидрида сирћетне киселине, сапуна, ацетил хлорида, бакар ацетата, винил ацетата и других хемикалија. Користи се као катализатор поликондензације и компонента киселих фиксатора за фотографије. Користи се за производњу електролита и пуферних раствора у галванизацији.

Негативна својства супстанце
Иако натријум ацетат и ниска токсичност, његова прекомерна употреба још увек може проузроковати значајне штете по људско здравље. Дакле, не препоручује се особама које пате од таквих болести: артеријска хипертензија, вегетативно-васкуларна дистонија, дисбактериоза. То би требало да значајно ограничи потрошњу производа који садрже Е262 и оних који имају проблеме са цревима, уринарном тракту, јетри, жучној кесици. То је због чињенице да се натријум ацетат у цревима често претвара у токсичне нитрате, који су канцерогени. Зато лекари упозоравају да прекомерна конзумација производа који садрже Е262 може довести до настанка малигних тумора, тровања и алергијских реакција. Натријум ацетат се не може користити у производњи дјечјих прехрамбених производа, тако да је присутност на пакирању Е262 означавања озбиљан разлог да се не купи.
Знаци тровања натријум ацетат
То су: вртоглавица, главобоља, бледа кожа, акутни бол у абдомену, некоординација, отежано дисање, грчеви, несвестица.
Интеракција натријум ацетата са другим супстанцама
Комбинација ове хемикалије са мравља киселина даје адукте. Као резултат комбинације са азотним оксидом настају натријум нитрит и ацетатни анхидрит. Супстанце као што је натријум ацетат + концентрована сумпорна киселина дају сирћетну киселину у једињењу.